Was ist Hospira Zoledronsäure?
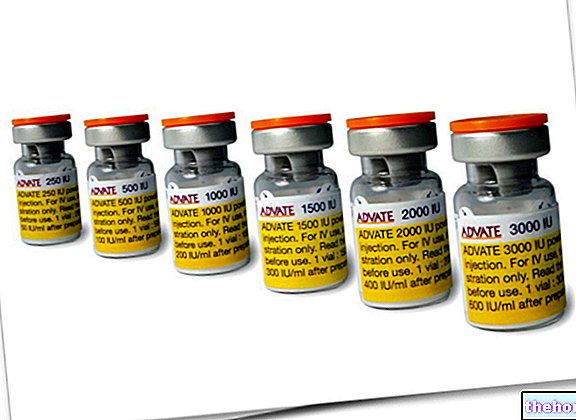
Zoledronsäure Hospira ist ein Arzneimittel, das den Wirkstoff Zoledronsäure enthält. Es ist als Konzentrat (4 mg / 5 ml) zum Anmischen zu einer Infusionslösung (Tropf in eine Vene) und als Infusionslösung (4 mg / 100 ml und 5 mg / 100 ml) erhältlich.
Zoledronsäure Hospira ist ein „Generika“ und ein „Hybrid“-Arzneimittel. Dies bedeutet, dass es einem oder mehreren „Referenzarzneimitteln“ ähnelt, die bereits in der Europäischen Union (EU) zugelassen sind. Das Referenzarzneimittel für das 4 mg/5 ml Konzentrat und die 4 mg/100 ml Lösung ist Zometa Adasta ist das Referenzarzneimittel für die 5 mg/100 ml Lösung.
Wofür wird Zoledronsäure Hospira angewendet?
Zoledronsäure Hospira Konzentrat 4 mg / 5 ml und 4 mg / 100 ml Lösung werden zur Vorbeugung von Knochenkomplikationen bei Erwachsenen mit fortgeschrittenem Knochenkrebs angewendet. Dazu gehören Frakturen (Knochenbrüche), Wirbelsäulenkompressionen (wenn das Rückenmark durch Knochen komprimiert wird), Knochenerkrankungen, die eine Strahlentherapie (Bestrahlungsbehandlung) oder eine Operation erfordern, und Hyperkalzämie (hoher Kalziumspiegel im Blut). Arzneimittel können auch verwendet werden, um eine durch Tumore verursachte Hyperkalzämie zu behandeln.
Zoledronsäure Hospira 5 mg/100 ml Lösung ist angezeigt zur Behandlung von Osteoporose (einer Erkrankung, die Knochen brüchig macht) bei postmenopausalen Frauen und Männern Es wird bei Patienten mit einem Risiko für Frakturen (Knochenbrüche) angewendet, auch bei Patienten, die kürzlich eine Hüftfraktur in einer leichten traumatischen Episode wie einem Sturz erlitten hat und bei Patienten, deren Osteoporose mit einer Langzeitbehandlung mit Glukokortikoiden (einer Art von Steroid) in Verbindung steht. Die 5 mg / 100 ml Lösung wird auch zur Behandlung des Morbus Paget des Knochens bei Erwachsenen verwendet, der durch eine Veränderung des normalen Knochenwachstums gekennzeichnet ist.
Das Arzneimittel ist nur auf ärztliche Verschreibung erhältlich.
Wie wird Zoledronsäure Hospira angewendet?
Zur Vorbeugung von Knochenkomplikationen und zur Behandlung einer durch Tumoren verursachten Hyperkalzämie beträgt die übliche Dosis von Zoledronsäure Hospira eine 4 mg Infusion über mindestens 15 Minuten. Bei Anwendung zur Vorbeugung von Knochenkomplikationen kann die Infusion alle 3-4 Wochen wiederholt werden und die Patienten sollten zusätzlich Kalzium- und Vitamin-D-Präparate einnehmen.
Zur Behandlung von Osteoporose und Morbus Paget des Knochens sollte Zoledronsäure Hospira als mindestens 15-minütige Infusion verabreicht werden. Die Anwendung kann bei Patienten, die wegen Osteoporose behandelt werden, jährlich wiederholt werden. Patienten, die eine Hüftfraktur erlitten haben, sollten Zoledronsäure Hospira erst nach Ablauf von zwei Wochen nach der Frakturreparatur erhalten. Bei Morbus Paget wird normalerweise nur eine Infusion von Zoledronsäure Hospira verabreicht Wenn die Krankheit jedoch erneut auftritt, können weitere Infusionen erwogen werden. Die Wirkung jeder Infusion hält mindestens ein Jahr an. Die Patienten müssen vor und nach der Behandlung ausreichend hydratisiert werden; sie sollten auch geeignete Vitamin-D- und Kalziumergänzungen erhalten. Die Anwendung von Paracetamol oder Ibuprofen (entzündungshemmende Arzneimittel) kurz nach der Einnahme von Zoledronsäure Hospira kann Symptome wie Fieber, Gliederschmerzen, grippeähnliche Symptome, Gelenkschmerzen und Kopfschmerzen für drei Tage nach der Infusion lindern.
Für alle Informationen lesen Sie die Packungsbeilage.
Wie wirkt Zoledronsäure Hospira?
Der Wirkstoff in Zoledronsäure Hospira, Zoledronsäure, ist ein Bisphosphonat. Es blockiert die Wirkung von Osteoklasten, den Körperzellen, die für den Abbau von Knochengewebe verantwortlich sind, und reduziert den Knochenverlust bei Osteoporose und die Krankheitsaktivität bei der Paget-Krankheit. Die Verringerung des Knochenverlusts trägt dazu bei, dass die Knochen weniger anfällig für Brüche sind, was bei Krebspatienten mit Knochenmetastasen einen Vorteil in Bezug auf die Frakturprävention bietet.
Krebspatienten können hohe Kalziumspiegel im Blut haben, die aus den Knochen freigesetzt werden. Durch die Hemmung des Knochenabbaus hilft Zoledronsäure Hospira, die im Blut freigesetzte Calciumkonzentration zu senken.
Wie wurde Zoledronsäure Hospira untersucht?
Das Unternehmen legte Daten zu Zoledronsäure aus der wissenschaftlichen Literatur vor.Es waren keine weiteren Studien erforderlich, da Zoledronsäure Hospira als Infusion verabreicht wird und denselben Wirkstoff wie die Referenzarzneimittel Zometa und Aclasta enthält.
Was sind die Vorteile und Risiken von Zoledronsäure Hospira?
Da Zoledronsäure Hospira als Infusion verabreicht wird und denselben Wirkstoff wie die Referenzarzneimittel enthält, werden Nutzen und Risiken als die gleichen wie bei den Referenzarzneimitteln angenommen.
Warum wurde Zoledronsäure Hospira zugelassen?
Der CHMP kam zu dem Schluss, dass Zoledronsäure Hospira in Übereinstimmung mit den EU-Anforderungen nachweislich vergleichbare Eigenschaften wie Zometa und Aclasta aufweist. Daher war der CHMP der Ansicht, dass der Nutzen wie im Fall von Zometa und Aclasta die identifizierten Risiken überwiegt empfahl die Erteilung einer Marktzulassung für Zoledronsäure Hospira.
Weitere Informationen zu Zoledronsäure Hospira
Am 19. November 2012 hat die Europäische Kommission eine „Marketing Authorization“ für Zoledronsäure Hospira ausgestellt, die in der gesamten Europäischen Union gültig ist.
Die vollständige EPAR-Version von Zoledronic Acid Hospira finden Sie auf der Website der Agentur: ema.Europa.eu/Find Medicine / Human Medicines / European Public Assessment Reports. Für weitere Informationen zur Therapie mit Zoledronsäure Hospira lesen Sie die Packungsbeilage (im EPAR enthalten) oder wenden Sie sich an Ihren Arzt oder Apotheker.
Die vollständige EPAR-Version des Referenzarzneimittels ist auch auf der Website der Agentur zu finden.
Letzte Aktualisierung dieser Zusammenfassung: 11-2012.
Die auf dieser Seite veröffentlichten Informationen zu Hospira Zoledronsäure können veraltet oder unvollständig sein. Informationen zur korrekten Verwendung dieser Informationen finden Sie auf der Seite Haftungsausschluss und nützliche Informationen.