Wirkstoffe: Brinzolamid, Timolol
AZARGA 10 mg / ml + 5 mg / ml Augentropfen, Suspension
Warum wird Azarga verwendet? Wofür ist das?
AZARGA enthält zwei Wirkstoffe, Brinzolamie und Timolol, die gemeinsam den Augeninnendruck senken.
AZARGA wird zur Behandlung von hohem Augeninnendruck, auch Glaukom oder okulärer Hypertonus genannt, bei Patienten über 18 Jahren angewendet, deren hoher Augeninnendruck mit einem Arzneimittel allein nicht wirksam kontrolliert werden kann.
Kontraindikationen Wenn Azarga nicht angewendet werden sollte
Verwenden Sie AZARGA . nicht
- wenn Sie allergisch gegen Brinzolamid, gegen Arzneimittel, die Sulfonamide genannt werden (z. B. Arzneimittel zur Behandlung von Diabetes und Infektionen sowie Diuretika (Tabletten zur Förderung der Diurese), gegen Timolol, Betablocker (Arzneimittel zur Senkung des Blutdrucks oder zur Behandlung von Herzerkrankungen) oder einen der sonstigen Bestandteile dieses Arzneimittels (aufgelistet in Abschnitt 6)
- wenn Sie Atemwegsprobleme wie Asthma, schwere chronisch obstruktive Bronchitis (schwere Lungenerkrankung, die Keuchen, Atembeschwerden und/oder lang anhaltenden Husten verursachen kann) oder andere Arten von Atemproblemen haben oder in der Vergangenheit hatten.
- bei starkem Heuschnupfen
- wenn Sie einen langsamen Herzschlag, Herzinsuffizienz oder Herzrhythmusstörungen (unregelmäßiger Herzschlag) haben.
- wenn Sie zu viel Säure in Ihrem Blut haben (ein Zustand, der als hyperchlorämische Azidose bezeichnet wird).
- wenn Sie schwere Nierenprobleme haben.
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Azarga . beachten?
AZARGA Tropfen nur in die Augen geben.
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie AZARGA anwenden, wenn Sie an:
- koronare Herzkrankheit (Symptome können Brustschmerzen oder Engegefühl, Keuchen oder Würgen umfassen), Herzinsuffizienz, niedriger Blutdruck.
- Veränderungen der Herzfrequenz, wie z. B. eine langsame Herzfrequenz.
- Atembeschwerden, Asthma oder chronisch obstruktive Lungenerkrankung.
- Durchblutungsstörungen (wie Raynauld-Krankheit oder Raynauld-Syndrom)
- Diabetes, da Timolol die Anzeichen und Symptome eines niedrigen Blutzuckerspiegels maskieren kann
- Schilddrüsenüberfunktion, da Timolol die Anzeichen und Symptome einer Schilddrüsenerkrankung maskieren kann
- Muskelschwäche (Myasthenia gravis)
- Informieren Sie Ihren Arzt vor einer Operation, dass Sie AZARGA anwenden, da Timolol die Wirkung einiger Arzneimittel, die während der Narkose angewendet werden, verändern kann.
- wenn Sie in der Vorgeschichte eine Atopie (eine Neigung zur Entwicklung einer allergischen Reaktion) und schwere allergische Reaktionen haben, können Sie bei der Anwendung von AZARGA mit größerer Wahrscheinlichkeit eine allergische Reaktion entwickeln und eine Adrenalinbehandlung ist möglicherweise nicht wirksam genug, um die Reaktion zu behandeln wenn Sie eine andere Behandlung haben, informieren Sie bitte Ihren Arzt oder das medizinische Fachpersonal, dass Sie AZARGA einnehmen.
- wenn Sie Leberprobleme haben.
- wenn Sie trockene Augen oder Hornhautprobleme haben.
- wenn Sie Nierenprobleme haben.
Kinder und Jugendliche
AZARGA wird nicht für Kinder und Jugendliche unter 18 Jahren empfohlen.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Azarga® verändern?
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel anwenden, kürzlich andere Arzneimittel angewendet haben oder beabsichtigen andere Arzneimittel einzunehmen.
AZARGA kann mit anderen Arzneimitteln, die Sie einnehmen, interagieren, einschließlich anderer Augentropfen zur Behandlung des Glaukoms. Informieren Sie Ihren Arzt, wenn Sie blutdrucksenkende Arzneimittel wie Parasympathomimetika und Guanethidin oder andere Herzmedikamente einschließlich Chinidin (zur Behandlung von Herzproblemen und einigen Arten von Malaria), Amiodaron oder anderen Arzneimitteln zur Behandlung von Herzrhythmusstörungen einnehmen oder beabsichtigen, diese einzunehmen und Glykoside bei Herzinsuffizienz.
Informieren Sie Ihren Arzt auch, wenn Sie Arzneimittel zur Behandlung von Diabetes oder zur Behandlung von Magengeschwüren oder Antimykotika, antivirale Arzneimittel oder Antibiotika oder Antidepressiva, die als Fluoxetin und Paroxetin bekannt sind, einnehmen oder einnehmen möchten.
Wenn Sie einen anderen Carboanhydrasehemmer (Acetazolamid oder Dorzolamid) einnehmen, informieren Sie bitte Ihren Arzt.
Warnungen Es ist wichtig zu wissen, dass:
Schwangerschaft und Stillzeit
Sie sollten AZARGA nicht anwenden, wenn Sie schwanger sind oder schwanger werden, es sei denn, Ihr Arzt hält dies für erforderlich. Sprechen Sie mit Ihrem Arzt, bevor Sie AZARGA anwenden.
Wenden Sie AZARGA nicht an, wenn Sie stillen, da Timolol in die Muttermilch übergehen kann. Fragen Sie Ihren Arzt um Rat, bevor Sie Arzneimittel während der Stillzeit anwenden.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Fahren Sie nicht und bedienen Sie keine Maschinen, bis Ihre Sicht klar ist. Unmittelbar nach der Anwendung von AZARGA kann Ihre Sicht für einige Zeit verschwommen sein.
Einer der Wirkstoffe kann die Fähigkeit verringern, Operationen durchzuführen, die geistige Aufmerksamkeit und / oder körperliche Koordination erfordern. Wenn dieses Symptom bei Ihnen auftritt, seien Sie beim Führen von Fahrzeugen oder beim Bedienen von Maschinen vorsichtig.
AZARGA enthält Benzalkoniumchlorid
AZARGA enthält ein Konservierungsmittel (Benzalkoniumchlorid), das weiche Kontaktlinsen verfärben und Augenreizungen verursachen kann. Tragen Sie daher während der Einnahme von AZARGA keine Kontaktlinsen. Warten Sie nach der Anwendung von AZARGA 15 Minuten, bevor Sie Ihre Kontaktlinsen wieder einsetzen.
Dosis, Methode und Zeitpunkt der Anwendung Wie ist Azarga anzuwenden: Dosierung
Wenden Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker an. Fragen Sie im Zweifelsfall Ihren Arzt oder Apotheker.
Wenn Sie die zuvor zur Behandlung des Glaukoms verwendeten Augentropfen mit AZARGA wechseln, sollten Sie die Anwendung des anderen Arzneimittels abbrechen und am nächsten Tag mit der Anwendung von AZARGA beginnen. Fragen Sie im Zweifelsfall Ihren Arzt oder Apotheker.
Zur Begrenzung der Arzneimittelmenge, die nach dem Auftragen der Augentropfen ins Blut gelangt, ist Folgendes hilfreich:
- Halten Sie das Augenlid geschlossen und üben Sie gleichzeitig für mindestens 2 Minuten einen leichten Druck mit einem Finger auf den inneren Augenwinkel in der Nähe der Nase aus.
Die empfohlene Dosis beträgt zweimal täglich einen Tropfen in das/die betroffene(n) Auge(n).
Wenden Sie AZARGA nur dann an beiden Augen an, wenn Ihr Arzt es Ihnen sagt. Verwenden Sie das Arzneimittel für die von Ihrem Arzt empfohlene Dauer.
Wie man es benutzt
- Holen Sie sich die Flasche und einen Spiegel.
- Wasch deine Hände.
- Vor Gebrauch gut schütteln.
- Schrauben Sie den Flaschenverschluss ab. Wenn sich der Sicherheitsring nach dem Entfernen der Kappe gelöst hat, entfernen Sie ihn, bevor Sie das Produkt verwenden.
- Nehmen Sie die Flasche, drehen Sie sie um und halten Sie sie zwischen Daumen und Zeigefinger.
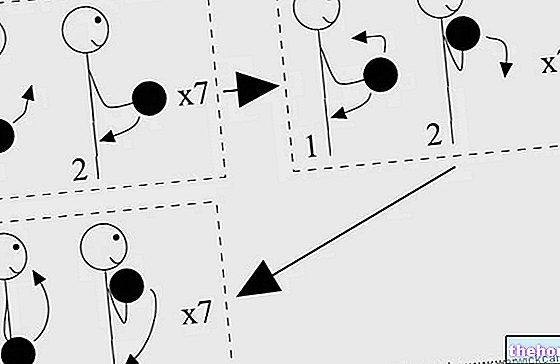
- Du neigst deinen Kopf nach hinten. Ziehen Sie das Unterlid mit einem sauberen Finger nach unten, so dass zwischen Lid und Auge eine „Tasche“ entsteht, in die der Tropfen gelangt (Abbildung 1).
- Halten Sie die Spitze der Flasche nah an Ihr Auge und benutzen Sie den Spiegel, wenn es hilft.
- Berühren Sie nicht Ihre Augen oder Augenlider, umliegende Bereiche oder andere Oberflächen mit der Flaschenspitze.Dies könnte die Augentropfen infizieren.
- Drücken Sie vorsichtig auf den Flaschenboden, um jeweils einen Tropfen AZARGA freizugeben.
- Drücken Sie nicht fest auf die Flasche: Sie ist so konzipiert, dass sie mit leichtem Druck auf den Boden arbeitet (Abbildung 2).
- Drücken Sie nach der Anwendung von AZARGA mit dem Finger 2 Minuten lang auf den Augenwinkel in der Nähe der Nase (Abbildung 3). Dies hilft zu verhindern, dass sich AZARGA auf den Rest des Körpers ausbreitet.
- Wenn Sie die Tropfen in beide Augen geben müssen, wiederholen Sie die Schritte für das andere Auge.
- Schrauben Sie die Kappe nach Gebrauch sofort wieder auf.
- Beenden Sie eine Flasche, bevor Sie die nächste öffnen.
Wenn ein Tropfen Ihr Auge verfehlt, versuchen Sie es erneut.
Wenn Sie andere Augentropfen oder Augensalben anwenden, lassen Sie zwischen dem Einträufeln jedes Arzneimittels mindestens 5 Minuten Zeit. Augensalben sollten zuletzt angewendet werden.
Wenn Sie die Einnahme von AZARGA vergessen haben, fahren Sie mit der nächsten Dosis wie geplant fort. Nehmen Sie nicht die doppelte Dosis ein, wenn Sie die vorherige Einnahme vergessen haben. Verwenden Sie zweimal täglich nicht mehr als einen Tropfen in das/die betroffene(n) Auge(n).
Wenn Sie die Einnahme von AZARGA ohne Rücksprache mit Ihrem Arzt abbrechen, wird Ihr Augeninnendruck nicht kontrolliert und es kann zu Sehverlust kommen.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
Überdosierung Was ist zu tun, wenn Sie zu viel Azarga eingenommen haben?
Wenn Sie eine größere Menge von AZARGA eingenommen haben, als Sie sollten, spülen Sie Ihre Augen sofort mit lauwarmem Wasser aus.Verwenden Sie die Tropfen erst, wenn die nächste Dosis fällig ist.
Sie können eine verringerte Herzfrequenz, einen verringerten Blutdruck, eine Herzinsuffizienz, Atembeschwerden und eine Beeinträchtigung Ihres Nervensystems feststellen.
Nebenwirkungen Was sind die Nebenwirkungen von Azarga
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Beenden Sie die Anwendung dieses Arzneimittels und wenden Sie sich sofort an Ihren Arzt, wenn Sie einen Hautausschlag, schwere Hautreaktionen oder starke Rötung oder Juckreiz der Augen entwickeln. Dies können Anzeichen einer allergischen Reaktion sein (Häufigkeit ist nicht bekannt).
Sie können die Tropfen normalerweise weiter verwenden, es sei denn, die Auswirkungen sind schwerwiegend. Wenn Sie sich Sorgen machen, sprechen Sie mit Ihrem Arzt oder Apotheker. Brechen Sie die Anwendung von AZARGA nicht ab, ohne vorher mit Ihrem Arzt gesprochen zu haben.
Häufige Nebenwirkungen (kann bis zu 1 von 10 Behandelten betreffen)
- Wirkungen am Auge: verschwommenes Sehen, Anzeichen und Symptome einer Augenreizung (zB Brennen, Reizung, Juckreiz, Tränen, Rötung), Augenschmerzen.
- Allgemeine Nebenwirkungen: Geschmacksstörungen
Gelegentliche Nebenwirkungen (kann bis zu 1 von 100 Behandelten betreffen)
- Auswirkungen am Auge: Hornhauterosion (Schädigung der vorderen Oberfläche des Augapfels), intraokulare Entzündung, Lichtempfindlichkeit, abnorme Augenempfindlichkeit, Augenausfluss, trockenes Auge, müde Augen, Verkrustung der Augenlider.
- Allgemeine Nebenwirkungen: niedriger Blutdruck, Husten, Schlafstörungen (Schlaflosigkeit).
Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
- Auswirkungen auf das Auge: Sehstörungen, Schädigung des Sehnervs, erhöhter Augeninnendruck, Ablagerungen auf der Augenoberfläche, Hornhautstörungen, verminderte Augenempfindlichkeit, Entzündung oder Infektion der Bindehaut, abnormales, doppeltes oder eingeschränktes Sehen, verstärkte Augenpigmentierung, Wachstum auf der Augenoberfläche, vermehrtes Tränen, Augenschwellung, Lichtempfindlichkeit, vermindertes Wachstum oder Anzahl der Wimpern, Herabhängen der oberen Augenlider (das Auge bleibt halb geschlossen), Entzündung der Augenlider und der Augenliddrüsen, Entzündung der Hornhaut und Ablösung der Schicht unter der Netzhaut, die die Blutgefäße enthält, nach Filteroperationen, was zu Sehstörungen und verringerter Hornhautempfindlichkeit führen kann.
- Herz und Kreislauf: Veränderungen des Rhythmus oder der Herzfrequenz, verlangsamte Herzfrequenz, Herzklopfen, eine Art von Herzrhythmusstörung, Brustschmerzen, verminderte Herzfunktion, Herzinfarkt, erhöhter Blutdruck, verminderte Durchblutung des Gehirns, Schlaganfall, Ödeme (Flüssigkeit) Ansammlung von Flüssigkeit), kongestive Herzinsuffizienz (Herzerkrankung mit Kurzatmigkeit und Schwellung der Füße und Beine durch Flüssigkeitsansammlung), Schwellung der Extremitäten, niedriger Blutdruck, Farbveränderung der Finger und Füße und gelegentlich anderer Bereiche der Körper (Raynaud-Phänomen), kalte Hände und Füße.
- Atemwege: Verengung der Atemwege in der Lunge (vorwiegend bei Patienten mit Vorerkrankungen), Kurzatmigkeit oder Atembeschwerden, Erkältungssymptome, Verstopfung der Brust, Infektionen der Nasenwege, Niesen, verstopfte Nase, trockene Nase, laufende Nase, Blutungen Nase, Asthma, Rachenreizung.
- Nervensystem und allgemeine Erkrankungen: Depression, Albträume, Gedächtnisverlust, Kopfschmerzen, Nervosität, Reizbarkeit, Müdigkeit, Zittern, abnorme Empfindungen, Ohnmacht, Schwindel, Schläfrigkeit, allgemeine oder schwere Schwäche, ungewöhnliche Empfindungen wie Kribbeln.
- Magen: Übelkeit, Erbrechen, Durchfall, Blähungen oder Bauchschmerzen, Halsentzündung, Gefühl von trockenem oder anormalem Mund, Verdauungsstörungen, Magenschmerzen
- Blut: Bluttests, die abnormale Leberfunktionswerte, erhöhte Chlorwerte im Blut, verringerte Anzahl roter Blutkörperchen im Blut zeigen
- Allergie: verstärkte Allergiesymptome, generalisierte allergische Reaktionen einschließlich Schwellungen unter der Haut, die in Bereichen wie Gesicht und Gliedmaßen auftreten können und die die Atemwege verstopfen können, was zu Schluck- oder Atembeschwerden führt, Nesselsucht, lokalisierter und generalisierter Hautausschlag, Juckreiz, schweres plötzliches Leben -bedrohliche allergische Reaktionen.
- Ohr: Ohrensausen, Schwindelgefühl oder Schwindel
- Haut: Hautausschlag, Rötung oder Entzündung der Haut, verminderte oder abnormale Hautempfindlichkeit, Haarausfall, silbrig-weißer Hautausschlag (psorasiformer Hautausschlag) oder Verschlechterung der Psoriasis.
- Muskel: generalisierte Rücken-, Gelenk- oder Muskelschmerzen, die nicht durch körperliche Anstrengung verursacht wurden, Muskelkrämpfe, Schmerzen in den Extremitäten, Muskelschwäche/-schwäche, verstärkte Anzeichen und Symptome einer Myasthenia gravis (Muskelerkrankung).
- Nieren: rückenschmerzähnliche Nierenschmerzen im unteren Rückenbereich, häufiges Wasserlassen
- Fortpflanzung: sexuelle Dysfunktion, verminderte Libido, männliche sexuelle Schwierigkeiten.
- Stoffwechsel: niedriger Blutzuckerspiegel
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind. Sie können Nebenwirkungen auch direkt über das in Anhang V aufgeführte nationale Meldesystem melden. Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
Ablauf und Aufbewahrung
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Verwenden Sie dieses Arzneimittel nicht nach dem auf der Flasche und dem Karton nach „Verwendbar bis“ angegebenen Verfallsdatum Das Verfallsdatum bezieht sich auf den letzten Tag des Monats.
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Um Infektionen vorzubeugen, entsorgen Sie die Flasche 4 Wochen nach dem ersten Öffnen und verwenden Sie eine neue Flasche. Schreiben Sie das Öffnungsdatum in das dafür vorgesehene Feld auf dem Flaschen- und Kartonetikett.
Werfen Sie Arzneimittel nicht in das Abwasser oder den Hausmüll. Fragen Sie Ihren Apotheker, wie Sie Arzneimittel, die Sie nicht mehr verwenden, entsorgen. Dies trägt zum Schutz der Umwelt bei.
Frist "> Weitere Informationen
Was AZARGA enthält
- Die Wirkstoffe sind Brinzolamid und Timolol. Ein ml Suspension enthält 10 mg Brinzolamid und 5 mg Timolol (als Maleat).
- Die sonstigen Bestandteile sind Benzalkoniumchlorid (siehe Abschnitt 2 „AZARGA enthält Benzalkoniumchlorid“), Carbopol 974P, Dinatriumedetat, Mannit (E421), gereinigtes Wasser, Natriumchlorid, Tyloxapol, Salzsäure und/oder Natriumhydroxid. Kleine Mengen Salzsäure und / oder Natriumhydroxid werden hinzugefügt, um den normalen Säuregehalt (pH-Wert) aufrechtzuerhalten.
Wie AZARGA aussieht und Inhalt der Packung
AZARGA ist eine Flüssigkeit (weiße bis cremefarbene einheitliche Suspension), die in einer Packung mit einer 5-ml-Kunststoffflasche mit Schraubverschluss oder in einer Packung mit drei 5-ml-Flaschen erhältlich ist.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu erhalten, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS -
AZARGA 10 MG / ML + 5 MG / ML AUGENTROPFEN, SUSPENSION
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG -
Ein ml Suspension enthält 10 mg Brinzolamid und 5 mg Timolol (als Timololmaleat).
Hilfsstoff(e) mit bekannter Wirkung:
Ein ml Suspension enthält 0,10 mg Benzalkoniumchlorid.
Die vollständige Auflistung der sonstigen Bestandteile finden Sie in Abschnitt 6.1.
03.0 DARREICHUNGSFORM -
Augentropfen, Suspension (Augentropfen).
Weiße bis cremefarbene einheitliche Suspension, pH 7,2 (ungefähr).
04.0 KLINISCHE INFORMATIONEN -
04.1 Anwendungsgebiete -
Senkung des Augeninnendrucks (IOD) bei erwachsenen Patienten mit Offenwinkelglaukom oder okulärer Hypertonie, bei denen eine Monotherapie zu einer unzureichenden Senkung des Augeninnendrucks führt (siehe Abschnitt 5.1).
04.2 Dosierung und Art der Anwendung -
Dosierung
Anwendung bei Erwachsenen, einschließlich älterer Menschen
Die Dosis beträgt zweimal täglich einen Tropfen AZARGA in den Bindehautsack des betroffenen Auges.
Die systemische Resorption wird durch Verschluss des Tränennasengangs oder durch Senken des Augenlids für 2 Minuten reduziert.Auf diese Weise kann eine Reduzierung systemischer Nebenwirkungen und eine Steigerung der lokalen Aktivität erreicht werden (siehe Abschnitt 4.4).
Wenn Sie eine Dosis vergessen haben, setzen Sie die Behandlung mit der nächsten Dosis wie geplant fort. Die Dosis sollte zweimal täglich einen Tropfen pro betroffenem Auge nicht überschreiten.
Wenn AZARGA als Ersatz für ein anderes Antiglaukom-Arzneimittel verwendet wird, sollte das andere Arzneimittel abgesetzt und die AZARGA-Therapie am nächsten Tag begonnen werden.
Besondere Bevölkerungsgruppen
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von AZARGA bei Kindern und Jugendlichen im Alter von 0 bis 18 Jahren ist noch nicht erwiesen.
Es liegen keine Daten vor.
Leber- und Nierenfunktionsstörung
Studien mit AZARGA oder Augentropfen, die Timolol 5 mg/ml enthalten, wurden bei Patienten mit Leber- oder Nierenfunktionsstörung nicht durchgeführt. Bei Patienten mit eingeschränkter Leberfunktion oder bei Patienten mit eingeschränkter Nierenfunktion ist keine Dosisanpassung erforderlich.
AZARGA wurde bei Patienten mit schwerer Nierenfunktionsstörung (Kreatinin-Clearance hyperchlorämische Azidose (siehe Abschnitt 4.3) nicht untersucht. Da Brinzolamid und sein Hauptmetabolit überwiegend über die Nieren ausgeschieden werden, ist AZARGA bei Patienten mit schwerer Nierenfunktionsstörung kontraindiziert (siehe Abschnitt 4.3).
AZARGA sollte bei Patienten mit schwerer Leberfunktionsstörung mit Vorsicht angewendet werden (siehe Abschnitt 4.4).
Art der Verabreichung
Für die ophthalmologische Anwendung.
Die Patienten sollten darauf hingewiesen werden, die Flasche vor der Anwendung gut zu schütteln.Wenn sich der Sicherheitsring nach dem Abnehmen des Verschlusses gelöst hat, entfernen Sie ihn, bevor Sie das Produkt verwenden.
Um eine Kontamination der Tropfflaschenspitze und der Lösung zu vermeiden, ist darauf zu achten, dass die Augenlider, umliegenden Bereiche oder andere Oberflächen nicht mit der Tropfspitze der Flasche berührt werden. Weisen Sie die Patienten an, die Flasche bei Nichtgebrauch fest verschlossen zu halten.
Bei gleichzeitiger Anwendung von mehr als einem topischen Augenarzneimittel sollten die Arzneimittel im Abstand von mindestens 5 Minuten verabreicht werden.
Augensalben sollten zuletzt verabreicht werden.
04.3 Kontraindikationen -
• Überempfindlichkeit gegen die Wirkstoffe oder einen der sonstigen Bestandteile.
• Überempfindlichkeit gegen andere Betablocker
• Überempfindlichkeit gegen Sulfonamide (siehe Abschnitt 4.4.)
• Reaktive Atemwegserkrankung, einschließlich Asthma bronchiale und eine „Anamnese von Asthma bronchiale, schwere chronisch-obstruktive Lungenerkrankung“.
• Sinusbradykardie, Sick-Sinus-Syndrom, sino-atrialer Block, atrioventrikulärer Block zweiten oder dritten Grades, der nicht mit einem Schrittmacher kontrolliert wird. Manifeste Herzinsuffizienz oder kardiogener Schock.
• Schwere allergische Rhinitis
• Hyperchlorämische Azidose (siehe Abschnitt 4.2).
• schwere Nierenfunktionsstörung.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung -
Systemische Effekte
• Brinzolamid und Timolol werden systemisch resorbiert. Aufgrund der beta-adrenergen Komponente von Timolol können die gleichen Arten von kardiovaskulären, pulmonalen und anderen Nebenwirkungen wie bei Beta-Substanzen auftreten.-systemisch verabreichte adrenerge Blocker. Die Inzidenz systemischer Nebenwirkungen nach topischer ophthalmischer Anwendung ist geringer als nach systemischer Anwendung Zur Verringerung der systemischen Resorption siehe Abschnitt 4.2.
• Bei mit AZARGA behandelten Patienten können bei allen Sulfonamid-Derivaten Überempfindlichkeitsreaktionen auftreten, da das Arzneimittel systemisch resorbiert wird.
Herzerkrankungen
Bei Patienten mit kardiovaskulären Erkrankungen (z. B. koronarer Herzkrankheit, Prinzmetal-Angina und Herzinsuffizienz) und Hypotonie sollte eine Betablocker-Therapie kritisch bewertet und eine Therapie mit anderen Wirkstoffen in Betracht gezogen werden. Bei Patienten mit Herz-Kreislauf-Erkrankungen sollten Anzeichen einer Verschlechterung dieser Erkrankungen und unerwünschte Reaktionen überwacht werden.
Aufgrund der negativen Wirkung auf die Überleitungszeit sollten Betablocker bei Patienten mit einem Herzblock ersten Grades mit Vorsicht angewendet werden.
Gefäßerkrankungen
Patienten mit schweren peripheren Durchblutungsstörungen/-störungen (z. B. schwere Formen der Raynauld-Krankheit oder des Raynauld-Syndroms) sind mit Vorsicht zu behandeln.
Hyperthyreose
Betablocker können auch die Anzeichen einer Hyperthyreose maskieren.
Muskelschwäche
Es wurde berichtet, dass Betablocker blockierende Arzneimittel die Muskelschwäche im Zusammenhang mit einigen Symptomen einer Myasthenie (z. B. Diplopie, Ptosis und generalisierte Schwäche) verstärken.
Atemwegserkrankungen
Atemwegsreaktionen, einschließlich Tod durch Bronchospasmus, wurden bei Patienten mit Asthma nach Anwendung einiger ophthalmischer Betablocker berichtet.
Bei Patienten mit leichter bis mittelschwerer chronisch-obstruktiver Lungenerkrankung sollte AZARGA mit Vorsicht angewendet werden und nur, wenn der potenzielle Nutzen das potenzielle Risiko überwiegt.
Hypoglykämie / Diabetes
Betablocker sollten bei Patienten mit spontaner Hypoglykämie oder bei Patienten mit labilem Diabetes mit Vorsicht angewendet werden, da Betablocker die Anzeichen und Symptome einer akuten Hypoglykämie maskieren können.
Störungen des Säure-Basen-Haushalts
AZARGA enthält Brinzolamid, ein Sulfonamid. Bei topischer Anwendung können dieselben Arten von Nebenwirkungen auftreten, die Sulfonamiden zuzuschreiben sind. Bei oraler Anwendung von Carboanhydrasehemmern wurden Säure-Basen-Störungen berichtet. Dieses Arzneimittel sollte bei Patienten, bei denen das Risiko einer Nierenfunktionsstörung aufgrund des möglichen Risikos einer metabolischen Azidose besteht, mit Vorsicht angewendet werden. Beenden Sie die Anwendung dieses Arzneimittels, wenn Anzeichen schwerer Reaktionen auftreten oder Überempfindlichkeit werden beobachtet.
Geistige Wachsamkeit
Orale Carboanhydrasehemmer können die Fähigkeit beeinträchtigen, Aufgaben auszuführen, die geistige Wachheit oder körperliche Koordination erfordern.AZARGA wird systemisch resorbiert und kann daher nach topischer Anwendung auftreten.
Anaphylaktische Reaktionen
Während der Beta-Einnahme-Blockern können Patienten mit einer Vorgeschichte von Atopie oder einer schweren anaphylaktischen Reaktion auf eine Vielzahl von Allergenen auf wiederholten Kontakt mit solchen Allergenen reaktiver sein und möglicherweise nicht auf die üblichen Adrenalindosen zur Behandlung anaphylaktischer Reaktionen ansprechen.
Ablösung der Aderhaut
Nach Verabreichung einer Therapie zur Verringerung der Kammerwasserproduktion (z. B. Timolol, Acetazolamid) nach Filtrationsverfahren wurde über eine Aderhautablösung berichtet.
Chirurgische Anästhesie
Beta-blockierende ophthalmologische Präparate können die systemische Beta-Agonist-Wirkung von zB Adrenalin blockieren Der Anästhesist sollte informiert werden, wenn der Patient Timolol einnimmt.
Begleittherapie
Die Wirkung von Betablockern auf den Augeninnendruck oder bekannte systemische Wirkungen können verstärkt werden, wenn Timolol an Patienten verabreicht wird, die bereits einen systemischen Betablocker erhalten. Das Ansprechen dieser Patienten sollte sorgfältig überwacht werden Wirkstoffe oder zwei Carboanhydrasehemmer wird nicht empfohlen (siehe Abschnitt 4.5).
Bei Patienten, die AZARGA und einen oralen Carboanhydrasehemmer erhalten, können additive Wirkungen auf die bekannten systemischen Wirkungen von Carboanhydrasehemmern auftreten. Die gleichzeitige Anwendung von AZARGA und oralen Carboanhydrasehemmern wurde nicht untersucht und wird nicht empfohlen (siehe Abschnitt 4.5).
Augeneffekte
Es liegen nur begrenzte Erfahrungen mit AZARGA bei der Behandlung von Patienten mit pseudoexfoliativem oder Pigmentglaukom vor. Bei der Behandlung dieser Patienten ist Vorsicht geboten und eine engmaschige Überwachung des IOD wird empfohlen.
AZARGA wurde bei Patienten mit Engwinkelglaukom nicht untersucht und seine Anwendung bei diesen Patienten wird nicht empfohlen.
Betablocker für die Augen können trockene Augen verursachen. Patienten mit Hornhauterkrankungen sollten mit Vorsicht behandelt werden.
Die mögliche Rolle von Brinzolamid auf die Hornhautendothelfunktion von Patienten mit geschwächter Hornhaut (insbesondere bei Patienten mit niedrigen Endothelzellzahlen) wurde nicht untersucht. Patienten mit Kontaktlinsen wurden nicht speziell untersucht und bei diesen Patienten wird eine sorgfältige Überwachung während der Anwendung empfohlen von Brinzolamid, da Carboanhydrasehemmer die Hornhauthydratation beeinträchtigen können und das Tragen von Kontaktlinsen das Risiko für die Hornhaut erhöhen kann Eine sorgfältige Überwachung von Patienten mit Hornhautbeeinträchtigung sowie von Patienten mit Diabetes mellitus oder Hornhautdystrophien wird empfohlen.
AZARGA kann beim Tragen von Kontaktlinsen unter genauer Beobachtung verwendet werden (siehe unter "Benzalkoniumchlorid")
Benzalkoniumchlorid
AZARGA enthält Benzalkoniumchlorid, das Augenreizungen verursachen kann und bei weichen Kontaktlinsen bekanntermaßen eine verfärbende Wirkung hat. Der Kontakt mit weichen Kontaktlinsen sollte vermieden werden. Den Patienten sollte geraten werden, die Kontaktlinsen vor der Anwendung zu entfernen. Anwendung von AZARGA und 15 Minuten warten nach dem Einträufeln der Dosis, bevor Sie sie wieder einführen.
Es wurde auch berichtet, dass Benzalkoniumchlorid punktförmige Keratopathie und/oder toxische ulzerative Keratopathie verursacht. Bei häufiger oder längerer Anwendung ist eine engmaschige Überwachung erforderlich.
Leberfunktionsstörung
AZARGA sollte bei Patienten mit schwerer Leberfunktionsstörung mit Vorsicht angewendet werden.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen -
Es wurden keine Arzneimittelwechselwirkungsstudien mit AZARGA durchgeführt.
AZARGA enthält Brinzolamid, einen Carboanhydrasehemmer und wird, obwohl topisch verabreicht, systemisch resorbiert.Bei oraler Anwendung von Carboanhydrasehemmern wurden Säure-Basen-Störungen berichtet. Bei Patienten, die AZARGA erhalten, sollte die Möglichkeit von Wechselwirkungen in Betracht gezogen werden.
Bei Patienten, die mit oralen Carboanhydrasehemmern und Augentropfen, die Brinzolamid enthalten, behandelt werden, besteht die Möglichkeit einer additiven Wirkung auf die bekannten systemischen Wirkungen der Carboanhydrasehemmung Die gleichzeitige Anwendung von Augentropfen, die Brinzolamid und oralen Carboanhydrasehemmern enthalten, wird nicht empfohlen.
Cytochrom P-Isoenzyme-450 für den Metabolismus von Brinzolamid verantwortlich sind CYP3A4 (das wichtigste), CYP2A6, CYP2B6, CYP2C8 und CYP2C9. Es wird erwartet, dass CYP3A4-Inhibitoren wie Ketoconazol, Itraconazol, Clotrimazol, Ritonavir und Troleandomycin den Metabolismus von Brinzolamid über CYP3A4 hemmen. Bei gleichzeitiger Anwendung von CYP3A4-Inhibitoren ist Vorsicht geboten. Da die Elimination jedoch hauptsächlich über die Niere erfolgt, ist eine Akkumulation von Brinzolamid unwahrscheinlich. Brinzolamid ist kein Inhibitor von Cytochrom-P-Isoenzymen-450.
Additive Effekte wie Hypotonie und/oder ausgeprägte Bradykardie können auftreten, wenn ein Betablocker in der Augenlösung gleichzeitig mit oralen Calciumkanalblockern, Betablockern, Antiarrhythmika (einschließlich Amiodaron), Digitalisglykosiden, Parasympathomimetika, Guanethidin verabreicht wird.
Betablocker können die Reaktion auf Adrenalin zur Behandlung anaphylaktischer Reaktionen verringern. Besondere Vorsicht ist bei Patienten mit Atopie oder Anaphylaxie in der Anamnese geboten (siehe Abschnitt 4.4).
Die hypertensive Reaktion auf ein plötzliches Absetzen von Clonidin kann sich bei Einnahme von Betablockern verstärken. Bei gleichzeitiger Anwendung dieses Arzneimittels mit Clonidin ist Vorsicht geboten.
Während einer kombinierten Behandlung mit CYP2D6-Inhibitoren (z. B. Chinidin, Fluoxetin, Paroxetin) und Timolol wurde über eine Beta-Potenzierung berichtet.-systemische Blockade (z. B. verringerte Herzfrequenz, Depression). Vorsicht ist geboten.
Die Betas-Blocker können die hypoglykämische Wirkung von Antidiabetika verstärken-Blocker können die Anzeichen und Symptome einer Hypoglykämie maskieren (siehe Abschnitt 4.4).
Bei gleichzeitiger Anwendung von ophthalmischen Betablockern und Adrenalin (Epinephrin) wurde gelegentlich über Mydriasis berichtet.
04.6 Schwangerschaft und Stillzeit -
Schwangerschaft
Es liegen keine ausreichenden Daten zur ophthalmischen Anwendung von Brinzolamid und Timolol bei Schwangeren vor. Tierexperimentelle Studien mit Brinzolamid haben nach systemischer Anwendung eine Reproduktionstoxizität gezeigt, siehe Abschnitt 5.3. AZARGA sollte während der Schwangerschaft nicht angewendet werden, wenn dies nicht unbedingt erforderlich ist systemische Resorption siehe Abschnitt 4.2.
Epidemiologische Studien haben keine Missbildungen gezeigt, aber das Risiko einer intrauterinen Wachstumsverzögerung, wenn Betablocker oral verabreicht werden. Darüber hinaus wurden bei Neugeborenen nach Gabe von Betablockern bis zum Zeitpunkt der Entbindung Anzeichen und Symptome von Betablockerwirkungen (z. B. Bradykardie, Hypotonie, Atemnot und Hypoglykämie) beobachtet. Wenn AZARGA bis zur Entbindung verabreicht wird, sollte das Neugeborene in den ersten Lebenstagen sorgfältig überwacht werden.
Fütterungszeit
Es ist nicht bekannt, ob ophthalmisches Brinzolamid beim Menschen in die Muttermilch übergeht. Tierexperimentelle Studien haben gezeigt, dass Brinzolamid nach oraler Verabreichung in die Muttermilch übergeht, siehe Abschnitt 5.3.
Betablocker gehen in die Muttermilch über. Bei therapeutischen Dosen von Timolol in Augentropfen ist es jedoch unwahrscheinlich, dass ausreichende Mengen in der Muttermilch vorhanden sind, um beim Säugling klinische Symptome von Betablockern hervorzurufen. Zur Verringerung der systemischen Resorption siehe Abschnitt 4.2.
Ein Risiko für Säuglinge kann jedoch nicht ausgeschlossen werden. Die Entscheidung, das Stillen oder die Behandlung mit AZARGA abzubrechen, sollte unter Berücksichtigung des Nutzens des Stillens für das Baby und des Nutzens der Therapie für die Frau getroffen werden.
Fruchtbarkeit
Präklinische Daten zeigen keinen Einfluss von Brinzolamid oder Timolol auf die männliche oder weibliche Fertilität. Bei der Anwendung von AZARGA sind keine Auswirkungen auf die männliche oder weibliche Fertilität zu erwarten.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen -
AZARGA hat einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Vorübergehendes verschwommenes Sehen sowie andere Sehstörungen können die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen beeinträchtigen.Wenn zum Zeitpunkt der Instillation verschwommenes Sehen auftritt, sollte der Patient warten, bis das Sehvermögen wieder klar ist, bevor er ein Fahrzeug führt oder Maschinen bedient.
Carboanhydrasehemmer können die Fähigkeit beeinträchtigen, Operationen durchzuführen, die geistige Aufmerksamkeit und/oder körperliche Koordination erfordern (siehe Abschnitt 4.4).
04.8 Nebenwirkungen -
Zusammenfassung des Sicherheitsprofils
In klinischen Studien waren die häufigsten Nebenwirkungen verschwommenes Sehen, Augenreizung und Augenschmerzen, die bei etwa 2 bis 7 % der Patienten auftraten.
Tabelle der Nebenwirkungen
Die folgenden Nebenwirkungen wurden in klinischen Studien und nach der Markteinführung mit AZARGA und den Einzelkomponenten Brinzolamid und Timolol berichtet. Sie werden nach folgender Konvention klassifiziert: sehr häufig (> 1/10), häufig (> 1/100 bis 1 / 1.000 bis 1 / 10.000 bis
1 beobachtete Nebenwirkungen von Azarga
2 zusätzliche Nebenwirkungen, die mit Timolol allein beobachtet wurden
3 zusätzliche Nebenwirkungen, die mit Brinzolamid allein beobachtet wurden
Beschreibung ausgewählter Nebenwirkungen
Dysgeusie (bitterer oder ungewöhnlicher Geschmack im Mund nach dem Einträufeln) war eine häufig systemisch auftretende Nebenwirkung im Zusammenhang mit der Anwendung von AZARGA während klinischer Studien. Dies ist wahrscheinlich auf die Passage der Augentropfen in den Nasopharynx durch den Tränennasenkanal zurückzuführen und ist auf Brinzolamid zurückzuführen. Ein nasolakrimaler Verschluss oder ein leichter Verschluss des Augenlids nach dem Einträufeln kann dazu beitragen, das Auftreten dieser Wirkung zu verringern (siehe Abschnitt 4.2).
AZARGA enthält Brinzolamid, einen Sulfonamid-Hemmer der Carboanhydrase mit systemischer Resorption Gastrointestinale, nervöse, hämatologische, renale und metabolische Wirkungen werden im Allgemeinen mit systemischen Carboanhydrase-Hemmern in Verbindung gebracht. Die gleichen Nebenwirkungen, die oralen Carboanhydrasehemmern zuzuschreiben sind, sind bei topischer Anwendung möglich.
Timolol wird in den systemischen Kreislauf aufgenommen. Dies kann ähnliche Nebenwirkungen wie bei systemischen Betablockern auftretenden Arzneimitteln verursachen. Die aufgeführten Nebenwirkungen umfassen Reaktionen, die in der Klasse der ophthalmischen Betablocker vorkommen. Zusätzliche Nebenwirkungen im Zusammenhang mit der Anwendung der einzelnen Komponenten, die bei AZARGA auftreten können, sind in der obigen Tabelle aufgeführt. Die Inzidenz systemischer Nebenwirkungen nach topischer ophthalmischer Anwendung ist geringer als nach systemischer Anwendung. Zur Verringerung der systemischen Resorption siehe Abschnitt 4.2.
Kinder und Jugendliche
Die Anwendung von AZARGA bei Kindern und Jugendlichen unter 18 Jahren wird aufgrund fehlender Daten zur Sicherheit und Wirksamkeit nicht empfohlen.
Meldung von vermuteten Nebenwirkungen
Die Meldung vermuteter Nebenwirkungen, die nach der Zulassung des Arzneimittels aufgetreten sind, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem in Anhang V zu melden.
04.9 Überdosierung -
Im Falle einer versehentlichen Einnahme können die Symptome einer Betablocker-Überdosierung Bradykardie, Hypotonie, Herzinsuffizienz und Bronchospasmus umfassen.
Im Falle einer Überdosierung mit AZARGA Augentropfen sollte die Behandlung symptomatisch und unterstützend erfolgen. Durch Brinzolamid können Elektrolytstörungen, die Entwicklung einer Azidose und mögliche Auswirkungen auf das Zentralnervensystem auftreten. Die Serumelektrolytspiegel (insbesondere Kalium) und der pH-Wert im Blut sollten überwacht werden. Studien haben gezeigt, dass Timolol nicht ohne weiteres dialysiert wird.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN -
05.1 "Pharmakodynamische Eigenschaften -
Pharmakotherapeutische Gruppe: Augenheilmittel, Antiglaukom-Präparate und Miotika.
ATC-Code: S01ED51.
Wirkmechanismus
AZARGA enthält zwei Wirkstoffe: Brinzolamid und Timololmaleat. Diese beiden Komponenten reduzieren den erhöhten Augeninnendruck (IOD) hauptsächlich durch eine Verringerung der Kammerwassersekretion, jedoch durch unterschiedliche Wirkmechanismen. Die kombinierte Wirkung dieser beiden Wirkstoffe führt zu einer weiteren Senkung des IOD im Vergleich zur einmaligen Einnahme jeder Komponente.
Brinzolamid ist ein starker Inhibitor der humanen Carboanhydrase II (CA-II), das vorherrschende Isoenzym im Auge. Die Hemmung der Carboanhydrase auf der Ebene der Ziliarfortsätze des Auges verringert die Kammerwassersekretion, vermutlich aufgrund einer Verlangsamung der Bildung von Bicarbonationen mit einer daraus resultierenden Verringerung des Natrium- und Flüssigkeitstransports.
Timolol ist ein nicht-selektiver adrenerger Blocker, der keine intrinsische sympathomimetische Aktivität, keine direkte myokarddämpfende Aktivität oder membranstabilisierende Aktivität aufweist. Untersuchungen zur Tonographie und Fluorophotometrie am Menschen weisen darauf hin, dass seine vorherrschende Wirkung mit einer Verringerung der Kammerwasserbildung und einer leichten Erhöhung der Abflussfähigkeit zusammenhängt.
Pharmakodynamische Wirkungen
Klinische Wirkungen:
In einer zwölfmonatigen kontrollierten klinischen Studie an Patienten mit Offenwinkelglaukom oder okulärer Hypertonie, die nach Ansicht des Prüfarztes von einer Kombinationstherapie profitieren könnten und deren mittlerer Augeninnendruck zu Studienbeginn zwischen 25 und 27 mmHg lag, konnte der mittlere Augeninnendruck senkende Effekt von AZARGA, das zweimal täglich verabreicht wurde, lag im Bereich von 7 bis 9 mmHg. Die Nichtunterlegenheit von AZARGA gegenüber Dorzolamid 20 mg/ml + Timolol 5 mg/ml bei der durchschnittlichen IOD-Senkung wurde zu allen Zeitpunkten bei allen Besuchen nachgewiesen.
In einer sechsmonatigen kontrollierten klinischen Studie bei Patienten mit Offenwinkelglaukom oder okulärer Hypertonie und einem mittleren Augeninnendruck zu Studienbeginn zwischen 25 und 27 mmHg wurde die durchschnittliche Augeninnendrucksenkungswirkung von zweimal täglich verabreichtem AZARGA zwischen 7 und 9 mmHg und bis zu 3 mmHg höher als bei zweimal täglich verabreichtem Brinzolamid 10 mg / ml und bis zu 2 mmHg höher als bei zweimal täglich verabreichtem Timolol 5 mg / ml. Zu allen Zeitpunkten wurde eine statistisch stärkere Verringerung des mittleren IOD im Vergleich zu Brinzolamid und Timolol beobachtet bei allen Besuchen.
In drei kontrollierten klinischen Studien waren die Augenbeschwerden nach der Instillation von AZARGA signifikant geringer als die nach der Instillation von 20 mg/ml Dorzolamid + 5 mg/ml Timolol empfundenen Beschwerden.
05.2 "Pharmakokinetische Eigenschaften -
Absorption
Nach topischer Anwendung am Auge werden Brinzolamid und Timolol durch die Hornhaut und in den systemischen Kreislauf resorbiert. In einer pharmakokinetischen Studie erhielten gesunde Probanden 2 Wochen lang zweimal täglich orales Brinzolamid (1 mg), um die Zeit bis zum Erreichen des Steady State vor Beginn der Behandlung mit AZARGA zu verkürzen. Nach Verabreichung von AZARGA zweimal täglich über 13 Wochen betrugen die mittleren Konzentrationen der roten Blutkörperchen (RBC) von Brinzolamid 18,8 ± 3,29 µM, 18,1 ± 2,68 µM bzw. 18, 4 ± 3,01 µM nach 4, 10 bzw. 15 Wochen, was zeigt, dass Steady-State-Konzentrationen von Brinzolamid in Erythrozyten wurden aufrechterhalten.
Im Steady State nach Verabreichung von AZARGA ist der Mittelwert von Cmax und AUC0-12 h im Plasma war Timolol um 27 % bzw. 28 % niedriger (Cmax: 0,824 ± 0,453 ng/ml; AUC0-12h: 4,71 ± 4,29 ng h/ml), im Vergleich zur Verabreichung von 5 mg/ml Timolol (Cmax: 1,13 ± 0,494 ng/ml; AUC0-12h: 6,58 ± 3,18 ngh/ml). Die niedrigere systemische Exposition gegenüber Timolol nach Gabe von AZARGA ist klinisch nicht relevant Nach Gabe von AZARGA wurde der mittlere Cmax-Wert von Timolol nach 0,79 ± 0,45 Stunden erreicht.
Verteilung
Die Plasmaproteinbindung von Brinzolamid ist mäßig (ungefähr 60 %). Brinzolamid wird aufgrund seiner hohen Bindungsaffinität an CA-II und in geringerem Maße an CA-I in roten Blutkörperchen sequestriert. Sein Metabolit N-Aktives Desethylbrinzolamid reichert sich in roten Blutkörperchen an, indem es hauptsächlich an CA-I bindet. Die Affinität von Brinzolamid und dem Metaboliten zu CA, das in den roten Blutkörperchen und im Gewebe enthalten ist, führt zu niedrigen Plasmakonzentrationen.
Verteilungsdaten im Augengewebe von Kaninchen zeigten, dass Timolol bis zu 48 Stunden nach der Verabreichung von AZARGA im Kammerwasser gemessen werden kann. Im Steady State wird Timolol im menschlichen Plasma bis zu 12 Stunden nach der Verabreichung nachgewiesen
Biotransformation
Die Stoffwechselwege von Brinzolamid beinhalten N.-Dealkylierung, O-Dealkylierung und Oxidation seiner N-Seitenkette-Propyl. Dann-Desethyl-brinzolamid ist ein beim Menschen gebildeter Hauptmetabolit von Brinzolamid, der in Gegenwart von Brinzolamid auch an CA-I binden und sich in roten Blutkörperchen anreichern kann.n vitro zeigten, dass am Metabolismus von Brinzolamid hauptsächlich das CYP3A4-Isoenzym sowie mindestens vier weitere Isoenzyme (CYP2A6, CYP2B6, CYP2C8 und CYP2C9) beteiligt sind.
Timolol wird auf zwei Arten metabolisiert. Ein Weg erzeugt eine Ethanolamin-Seitenkette am Thiadiazol-Ring und der andere erzeugt eine Ethanol-Seitenkette am Morpholin-Stickstoffatom und eine zweite ähnliche Seitenkette mit einer Carbonylgruppe neben dem Stickstoff. Der Metabolismus von Timolol wird hauptsächlich durch das CYP2D6-Isoenzym vermittelt.
Beseitigung
Brinzolamid wird hauptsächlich über die Nieren ausgeschieden (ca. 60 %). Ungefähr 20 % der Dosis wurden als Metabolit im Urin wiedergefunden. Brinzolamid und N-Desethylbrinzolamid sind die Hauptbestandteile, die neben Spuren (-desmethyl .
Timolol und seine Metaboliten werden hauptsächlich über die Nieren ausgeschieden. Ungefähr 20 % einer Timolol-Dosis werden unverändert mit dem Urin ausgeschieden, der Rest wird als Metaboliten mit dem Urin ausgeschieden. Die t1 / 2 von Timolol im Plasma beträgt 4,8 Stunden nach der okulären Verabreichung von AZARGA.
05.3 Präklinische Daten zur Sicherheit -
Brinzolamid
Basierend auf den konventionellen Studien zur Sicherheitspharmakologie, Toxizität bei wiederholter Gabe, Genotoxizität und zum kanzerogenen Potenzial lassen die präklinischen Daten keine besonderen Gefahren für den Menschen durch Brinzolamid erkennen.
Entwicklungstoxizitätsstudien an Kaninchen mit oralen Brinzolamid-Dosen von bis zu 6 mg / kg / Tag (214-fache der empfohlenen klinischen Tagesdosis von 28 µg / kg / Tag) zeigten trotz signifikanter Toxizität keine Wirkung auf die fetale Entwicklung. Ähnliche Studien an Ratten zeigten eine leicht reduzierte Verknöcherung des Schädels und des Brustbeins von Föten von Müttern, denen Brinzolamid in Dosen von 18 mg / kg / Tag (das 642-fache der empfohlenen klinischen Tagesdosis) verabreicht wurde, jedoch nicht bei Dosen von 6 mg / kg / Tag . Diese Ergebnisse traten bei Dosen auf, die eine metabolische Azidose mit einer Verringerung des mütterlichen Körpergewichtswachstums und des fetalen Gewichts verursachten.
Eine Verringerung des Gewichts der Fötusdosis-Bei Welpen von Müttern, die Brinzolamid oral erhielten, wurde eine variabel zu lesende Abnahme (ca-6%) bei 2 mg/kg/Tag bis zu ca. 14% bei 18 mg/kg/Tag. Während der Laktation betrug der Wert ohne nachteilige Wirkung bei den Nachkommen 5 mg/kg/Tag.
Timolol
Basierend auf den konventionellen Studien zur Sicherheitspharmakologie, Toxizität bei wiederholter Gabe, Genotoxizität und zum kanzerogenen Potenzial lassen die präklinischen Daten von Timolol keine besonderen Gefahren für den Menschen erkennen. bei 50 mg / kg / Tag oder dem 3500-fachen der klinischen Tagesdosis von 14 µg / kg / Tag) und einer Erhöhung der fetalen Resorptionen bei Kaninchen (bei 90 mg / kg / Tag oder dem 6400-fachen der klinischen Tagesdosis).
06.0 PHARMAZEUTISCHE INFORMATIONEN -
06.1 Hilfsstoffe -
Benzalkoniumchlorid
Mannit (E421)
Carbopol 974P
Tyloxapol
Dinatriumedetat
Natriumchlorid
Salzsäure und/oder Natriumhydroxid (zur pH-Einstellung)
Gereinigtes Wasser
06.2 Inkompatibilität "-
Nicht relevant.
06.3 Gültigkeitsdauer "-
2 Jahre.
4 Wochen nach dem ersten Öffnen.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung -
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks -
Opake 5 ml runde Flaschen aus Polyethylen niedriger Dichte mit Tropfer und weißem Polypropylen-Schraubverschluss (DROP-TAINER) mit 5 ml Suspension.
Kartons mit 1 oder 3 Flaschen. Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
06.6 Gebrauchs- und Handhabungshinweise -
Keine besonderen Anweisungen.
07.0 INHABER DER "MARKETING GENEHMIGUNG" -
Alcon Laboratories (UK) Ltd.
Gewerbepark Frimley
Frimley
Camberley
Surrey, GU16 7SR
08.0 NUMMER DER VERMARKTUNGSBERECHTIGUNG -
EU / 1/08/482 / 001-002
038837011
038837023
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG -
Datum der Erstzulassung: 25. November 2008
Datum der letzten Verlängerung: 26. August 2013
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs -
D.CCE März 2015