Definition von Osmose
Osmose ist der spontane Durchgang eines Lösungsmittels (das in biologischen Systemen normalerweise Wasser ist) von einer Lösung, in der die gelösten Stoffe stärker verdünnt sind, zu einer, in der sie stärker konzentriert sind; diese Bewegung - die durch eine semipermeable Membran erfolgt - setzt sich fort, bis eine Gleichgewichtssituation erreicht ist, in der beide Lösungen die gleiche Konzentration gewinnen und beibehalten.
Praxisbeispiel

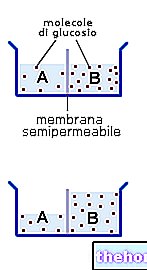
Um das Konzept der Osmose besser zu verdeutlichen, stellen wir uns vor, wir haben einen Behälter, der durch eine semipermeable Membran in zwei Kompartimente gleichen Volumens (A und B) unterteilt ist (d. h. nur für das Lösungsmittel - in diesem Fall Wasser - und nicht für das gelösten Stoff) Kammer A befindet sich eine wässrige Lösung, in der ein Esslöffel Glukose gelöst wurde, während wir in Teil B eine wässrige Lösung gleichen Volumens haben, in der drei Esslöffel Glukose gelöst wurden (sie ist daher konzentrierter). Unterschied erzeugt einen Konzentrationsgradienten für Glukose an den Seiten der Membran, und da dieser Zucker ihn nicht passieren kann, wird das Gleichgewicht mit dem Durchgang von Wasser von der Kammer A (wo die Glukose stärker verdünnt ist) in die Kammer B (wo sie reichlich vorhanden ist) erreicht ). Wenn Sie es vorziehen, kann man auch sagen, dass das Wasser durch Osmose von der konzentrierteren Lösung (A) in die weniger konzentrierte (B) übergeht.
Dieser Strömung folgend, steigt der Wasserspiegel in B und sinkt in A, wodurch ein gewisser Niveauunterschied zwischen beiden entsteht. Dieses Phänomen endet, wenn die beiden Lösungen die gleiche Konzentration erreichen und diese dann konstant halten.
Hypotonische, isotonische und hypertonische Lösungen
Nimmt man zwei Lösungen mit unterschiedlicher molarer Konzentration (unterschiedliche Anzahl von darin gelösten Partikeln), wird die Lösung mit der niedrigsten molaren Konzentration als hypotonisch und die konzentriertere als hypertonisch definiert. Zwei Lösungen sind stattdessen isotonisch (oder äquimolar), wenn sie die gleiche Konzentration haben.
In dem eben gemachten Beispiel ist Lösung B hypertonisch (daher enthält sie mehr gelöste Stoffe) als die andere (als hypotonisch definiert); daher bewegt sich das Lösungsmittel unter normalen Bedingungen durch Osmose von der hypotonischen in die hypertonische Lösung. Wir haben über Standardbedingungen gesprochen, weil es möglich ist, mit den Gesetzen der Physik zu spielen, das eigentliche Konzept der Osmose umzukehren und den Übergang des Lösungsmittels von der am stärksten verdünnten Konzentration zur am stärksten zu begünstigen (Umkehrosmose).
Osmotischer Druck und Umkehrosmose
Wie bisher ausgedrückt, setzt sich der Nettofluss des Lösungsmittels - erzeugt durch Osmose - fort, bis die beiden Lösungen die gleiche Konzentration erreicht haben. Nun, dieser Bewegung kann entgegengewirkt, gestoppt oder sogar umgekehrt werden, indem Druck auf das Fach mit der höchsten Konzentration ausgeübt wird.

Im vorigen Beispiel genügt es, einen Kolben in Kammer B zu platzieren (wobei wir uns an eine höhere Konzentration erinnern) und ihn mit einer gewissen Kraft nach unten zu drücken, um den Durchgang des Wassers in Richtung A zu begünstigen; in diesem Fall sprechen wir von umgekehrt Osmose.
Der osmotische Druck ist der Druck, der dem Durchgang des Lösungsmittels durch die semipermeable Membran genau entgegenwirkt; folglich ist es der notwendige Druck, um der Osmose entgegenzuwirken.
Für das bisher Gesagte haben zwei isotonische Lösungen den gleichen osmotischen Druck; Es sollte daher betont werden, dass der osmotische Druck ausschließlich von der Anzahl der in der Lösung vorhandenen Teilchen und nicht von deren Beschaffenheit abhängt.
Osmose und der menschliche Körper
Die Plasmamembranen, die die Zellen des menschlichen Körpers umgeben, sind in der Tat semipermeable Membranen, die den direkten Durchgang kleiner Moleküle (wie Wasser und Harnstoff) durch Osmose ermöglichen, jedoch nicht derjenigen mit höherem Molekulargewicht ( wie Proteine, Aminosäuren und Zucker). Osmotische Gleichgewichte in Körperflüssigkeiten sind daher unerlässlich, um den Zellen ein optimales Lebensumfeld zu garantieren.
Nehmen wir eine Zelle wie ein rotes Blutkörperchen und tauchen sie in eine hypotonische Lösung, so quillt diese durch Osmose (durch Wassereintritt) auf, die sogar explodieren kann hypertonische Lösung Die Zelle erfährt aufgrund des Wasserdurchtritts nach außen eine starke Dehydration, die zu Faltenbildung führt. Glücklicherweise sind Zellen im menschlichen Organismus in Bezug auf ihre innere Umgebung in isotonische Lösungen eingetaucht, und es gibt verschiedene Systeme, um diese Flüssigkeiten im osmotischen Gleichgewicht zu halten.
Osmotischer Druck und Lebensmittellagerung
Denken wir einen Moment an eine hausgemachte Marmelade ... Zucker wird in Hülle und Fülle hinzugefügt, um nicht nur den Geschmack zu verbessern, sondern vor allem auch, um die Haltbarkeit zu erhöhen. Dennoch ist Zucker ein wichtiges Element für das Leben vieler Mikroorganismen, die am Abbau des Produkts beteiligt sind. Dieser scheinbare Widerspruch wird durch das Konzept der Osmose selbst zerlegt.