Was ist Amgevita - Adalimumab und wofür wird es angewendet?
Amgevita ist ein Arzneimittel, das auf das Immunsystem wirkt und zur Behandlung der folgenden Erkrankungen angewendet wird:
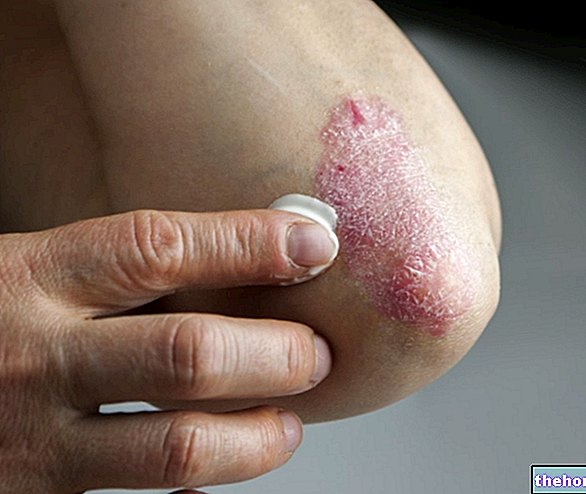
- Plaque-Psoriasis (eine Krankheit, die rote, schuppige Flecken auf der Haut verursacht);
- Psoriasis-Arthritis (eine Krankheit, die rote, schuppige Flecken auf der Haut mit Gelenkentzündungen verursacht);
- rheumatoide Arthritis (eine Krankheit, die eine Entzündung der Gelenke verursacht);
- axiale Spondyloarthritis (Entzündung der Wirbelsäule mit Rückenschmerzen), einschließlich Spondylitis ankylosans, auch ohne Röntgenbefund, aber mit deutlichen Entzündungszeichen;
- Morbus Crohn (eine Krankheit, die eine Darmentzündung verursacht);
- Colitis ulcerosa (eine Krankheit, die Entzündungen und Geschwüre der Darmschleimhaut verursacht);
- polyartikuläre juvenile idiopathische Arthritis und aktive Arthritis in Verbindung mit Enthesitis (beides seltene Krankheiten, die eine Gelenkentzündung verursachen); Hidradenitis suppurativa (Akne inversa), eine chronische Hauterkrankung, die Klumpen, Abszesse (Eiteransammlungen) und Narben auf der Haut verursacht;
- nicht-infektiöse Uveitis (Entzündung der Schicht unter dem Weiß des Augapfels).
Amgevita wird hauptsächlich bei Erwachsenen mit schweren, mittelschweren oder sich verschlechternden Erkrankungen angewendet oder wenn Patienten nicht mit anderen Behandlungen behandelt werden können. Weitere Informationen zur Anwendung von Amgevita unter allen Bedingungen, einschließlich derjenigen, bei denen es bei Kindern angewendet werden kann, finden Sie in der Zusammenfassung der Merkmale des Arzneimittels (im EPAR enthalten).
Amgevita enthält den Wirkstoff Adalimumab und ist ein „Biosimilar“. Dies bedeutet, dass es einem bereits in der Europäischen Union (EU) zugelassenen biologischen Arzneimittel (dem „Referenzarzneimittel") sehr ähnlich ist. Das Referenzarzneimittel für Amgevita ist Humira. Weitere Informationen zu Biosimilars finden Sie in den Fragen. und Antworten, indem Sie hier klicken.
Wie wird Amgevita - Adalimumab angewendet?
Amgevita ist nur auf ärztliche Verschreibung erhältlich; die Behandlung muss von Fachärzten eingeleitet und überwacht werden, die Erfahrung in der Diagnose und Behandlung von Erkrankungen haben, für die sie zugelassen ist. Ärzte, die eine Uveitis-Behandlung verschreiben, sollten auch mit der Anwendung von Amgevita erfahrene Ärzte konsultieren.
Das Arzneimittel ist als Injektionslösung unter die Haut in einer Fertigspritze oder einem Fertigpen erhältlich. Die Dosis hängt von der zu behandelnden Erkrankung ab und wird bei Kindern in der Regel anhand des Körpergewichts und der Körpergröße berechnet. Nach der Anfangsdosis wird Amgevita meistens alle zwei Wochen verabreicht; es kann jedoch in bestimmten Situationen wöchentlich verabreicht werden. Wenn der Arzt dies für angebracht hält, kann die Amgevita-Injektion von den Patienten selbst oder ihren Betreuern nach entsprechender Anweisung erfolgen.Während der Behandlung mit Amgevita können den Patienten andere Arzneimittel wie Methotrexat oder Kortikosteroide (andere entzündungshemmende Medikamente).
Informationen zu den bei den verschiedenen Erkrankungen zu verwendenden Dosen und zur Anwendung von Amgevita finden Sie in der Packungsbeilage.
Wie wirkt Amgevita - Adalimumab?
Der Wirkstoff in Amgevita, Adalimumab, ist ein monoklonaler Antikörper (eine Proteinart), der entwickelt wurde, um einen chemischen Botenstoff im Körper namens Tumornekrosefaktor (TNF) zu erkennen und daran zu binden. Dieser Botenstoff ist für Entzündungen verantwortlich und kommt in hohen Konzentrationen vor bei Patienten mit Erkrankungen, die mit Amgevita behandelt werden können. Durch die Bindung an TNF blockiert Adalimumab dessen Aktivität und reduziert dadurch Entzündungen und andere Symptome der Krankheit.
Welchen Nutzen hat Amgevita - Adalimumab während der Studien gezeigt?
Groß angelegte Laborstudien zum Vergleich von Amgevita und Humira haben gezeigt, dass das in Amgevita enthaltene Adalimumab dem in Humira enthaltenen Adalimumab in Bezug auf chemische Struktur, Reinheit und biologische Aktivität sehr ähnlich ist. P.
Da es sich bei Amgevita um ein Biosimilar handelt, müssen die mit Humira durchgeführten Studien zur Wirksamkeit und Sicherheit nicht alle für Amgevita wiederholt werden.
In einer Hauptstudie mit 526 Patienten mit mittelschwerer bis schwerer rheumatoider Arthritis, die nicht ausreichend auf Methotrexat angesprochen hatten, und in einer anderen Hauptstudie mit 350 Patienten mit mittelschwerer bis schwerer Psoriasis zeigte das Arzneimittel ähnliche Wirkungen wie Humira.
In der Studie zu rheumatoider Arthritis wurde das Ansprechen mit einer Linderung der Symptome von 20 % oder mehr nach 24 Behandlungswochen quantifiziert: 75 % der mit Amgevita behandelten Patienten hatten auf 72 % der mit Humira behandelten Patienten angesprochen Betrachtet man den Grad der Besserung nach 16 Wochen, so lag der Symptomscore bei Amgevita bei 81 % im Vergleich zu 83 % bei der Linderung bei Humira.
Welche Risiken sind mit Amgevita - Adalimumab verbunden?
Sehr häufige Nebenwirkungen von Adalimumab (beobachtet bei mehr als 1 von 10 Patienten) sind Infektionen der Nase und des Rachens, der Nebenhöhlen und der oberen Atemwege, Reaktionen an der Injektionsstelle (Rötung, Juckreiz, Blutungen, Schmerzen oder Schwellungen), Kopfschmerzen und Schmerzen des Bewegungsapparates .
Amgevita und andere Arzneimittel der gleichen Klasse können auch die Fähigkeit des Immunsystems beeinflussen, Infektionen und Krebs zu bekämpfen, und es gab Fälle von schweren Infektionen und Blutkrebs bei Patienten, die Adalimumab einnahmen.
Andere seltene schwerwiegende Nebenwirkungen (beobachtet zwischen 1 von 10.000 und 1 von 1.000 Patienten) sind die Unfähigkeit des Knochenmarks, Blutzellen zu produzieren, Erkrankungen des Nervensystems, Lupus und Lupus-ähnliche Zustände (bei denen das Immunsystem das Gewebe angreift und Entzündungen und Organschäden) und Stevens-Johnson-Syndrom (eine schwere Hauterkrankung).
Amgevita darf nicht bei Patienten mit aktiver Tuberkulose und anderen schweren Infektionen oder bei Patienten mit mittelschwerer bis schwerer Herzinsuffizienz (der Unfähigkeit des Herzens, genügend Blut durch den Körper zu pumpen) angewendet werden. Die vollständige Liste der Einschränkungen finden Sie in der Packungsbeilage.
Warum wurde Amgevita - Adalimumab zugelassen?
Der Ausschuss für Humanarzneimittel (CHMP) der Agentur entschied, dass Amgevita in Übereinstimmung mit den EU-Anforderungen für Biosimilars eine sehr ähnliche Struktur, Reinheit und biologische Aktivität wie Humira aufweist und auf dieselbe Weise im Körper verteilt wird.
Darüber hinaus haben Studien bei rheumatoider Arthritis und Psoriasis gezeigt, dass die Wirkungen des Arzneimittels denen von Humira bei diesen Erkrankungen entsprechen. Alle diese Daten wurden als ausreichend angesehen, um den Schluss zu ziehen, dass sich Amgevita in Bezug auf Wirksamkeit und Sicherheit in den zugelassenen Anwendungsgebieten genauso verhalten wird wie Humira. Daher war der CHMP der Ansicht, dass wie im Fall von Humira der Nutzen die identifizierten Risiken überwiegt, und empfahl die Erteilung der Genehmigung für das Inverkehrbringen von Amgevita.
Welche Maßnahmen werden ergriffen, um die sichere und wirksame Anwendung von Amgevita - Adalimumab zu gewährleisten?
Das Unternehmen, das Amgevita in Verkehr bringt, muss den Ärzten, die das Arzneimittel verschreiben, Informationspakete zur Verfügung stellen. Diese Packungen enthalten Informationen zur Sicherheit des Arzneimittels und eine Warnkarte, die den Patienten ausgehändigt wird.
Die Empfehlungen und Vorsichtsmaßnahmen, die medizinisches Fachpersonal und Patienten für eine sichere und wirksame Anwendung von Amgevita beachten müssen, wurden auch in der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage beschrieben.
Weitere Informationen zu Amgevita - Adalimumab
Die vollständige Version des EPAR von Amgevita finden Sie auf der Website der Agentur: ema.europa.eu/Find Medicine / Human Medicines / European Public Assessment Reports. Für weitere Informationen zur Amgevita-Therapie lesen Sie die Packungsbeilage (im EPAR enthalten) oder wenden Sie sich an Ihren Arzt oder Apotheker.
Die auf dieser Seite veröffentlichten Informationen zu Amgevita - Adalimumab können veraltet oder unvollständig sein. Informationen zur korrekten Verwendung dieser Informationen finden Sie auf der Seite Haftungsausschluss und nützliche Informationen.







-ed-essenziali-(age).jpg)