Wirkstoffe: Fentanyl
Fentanyl Zentiva 25 Mikrogramm/h transdermales Pflaster
Fentanyl Zentiva 50 Mikrogramm/h transdermales Pflaster
Fentanyl Zentiva 75 Mikrogramm/h transdermales Pflaster
Fentanyl Zentiva 100 Mikrogramm/h transdermales Pflaster
Warum wird Fentanyl verwendet - Generikum? Wofür ist das?
Der Name des Arzneimittels ist Fentanyl Zentiva transdermales Pflaster. In dieser Packungsbeilage wird es Fentanyl Zentiva oder einfach nur Pflaster genannt. Das Pflaster hilft, starke und anhaltende Schmerzen zu lindern.
Fentanyl Zentiva transdermales Pflaster enthält ein Arzneimittel namens Fentanyl. Fentanyl gehört zu einer Gruppe starker Schmerzmittel, die Opiate genannt werden.
Das Arzneimittel gelangt langsam vom Pflaster durch die Haut in den Körper.
Kontraindikationen Wenn Fentanyl nicht verwendet werden sollte - Generikum
Verwenden Sie Fentanyl Zentiva transdermales Pflaster nicht, wenn
- wenn Sie allergisch gegen Fentanyl oder einen der in Abschnitt 6 genannten sonstigen Bestandteile dieses Arzneimittels sind;
- der Schmerz, unter dem er leidet, ist von kurzer Dauer; - wenn Ihr zentrales Nervensystem (Gehirn und Rückenmark) stark beeinträchtigt ist, beispielsweise aufgrund eines Hirntraumas;
- wenn Sie Schwierigkeiten beim Atmen haben (langsamere und schwächere Atmung) und sich ungewöhnlich schläfrig fühlen.
Verwenden Sie dieses Arzneimittel nicht, wenn eine der oben genannten Bedingungen auf Sie oder Ihr Kind zutrifft. Wenn Sie sich nicht sicher sind, fragen Sie vor der Anwendung von Fentanyl Zentiva Ihren Arzt oder Apotheker.
Vorsichtsmaßnahmen für die Anwendung Was Sie vor der Einnahme von Fentanyl - Generikum beachten müssen
Was müssen Sie vor der Anwendung von Fentanyl Zentiva transdermales Pflaster beachten?
Fentanyl Zentiva transdermales Pflaster kann bei Kindern ab 2 Jahren angewendet werden, die zuvor Opioid-Schmerzmittel angewendet haben.
Wenn Ihrem Kind das Pflaster verschrieben wurde, ist der nachstehende Begriff „Ihr“ als „Ihr Kind“ zu verstehen.
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Fentanyl Zentiva anwenden. Fentanyl Zentiva ist ein für Kinder lebensbedrohliches Arzneimittel.
Dies gilt auch für unbenutzte transdermale Pflaster. Bitte beachten Sie, dass die Form dieses Arzneimittels für ein Kind attraktiv sein kann und dies in einigen Fällen zum Tod führen kann.
Fentanyl Zentiva kann bei Personen, die nicht routinemäßig verschriebene Opioid-Arzneimittel einnehmen, Nebenwirkungen haben.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Fentanyl - Generikum verändern
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel anwenden, kürzlich andere Arzneimittel angewendet haben oder beabsichtigen andere Arzneimittel einzunehmen.
Informieren Sie Ihren Arzt oder Apotheker insbesondere, wenn Sie Folgendes einnehmen:
- Andere Schmerzmittel wie andere Opioid-Schmerzmittel (Brupenorphin, Nalbuphin oder Pentazocin)
- Medikamente, die Ihnen beim Einschlafen helfen
- Arzneimittel zur Beruhigung (Beruhigungsmittel) und Arzneimittel gegen psychische Störungen
- Medikamente zur Entspannung der Muskulatur
- Einige Arzneimittel zur Behandlung von Depressionen (wie Citalopram, Duloxetin, Escitalopram, Fluoxetin, Fluvoxamin, Paroxetin, Sertralin, Venlafaxin)
- Einige Arzneimittel zur Behandlung von Depressionen (sogenannte MAO-Hemmer). Sie sollten Fentanyl Zentiva 14 Tage lang nicht anwenden, nachdem Sie diese Arzneimittel abgesetzt haben
- Nefazodon, ein Arzneimittel zur Behandlung von Depressionen
- Einige Antihistaminika (insbesondere solche, die Sie schläfrig machen können)
- Einige Antibiotika zur Behandlung von Infektionen, wie Erythromycin, Clarithromycin oder Troleandomycin
- Arzneimittel zur Behandlung von Pilzinfektionen wie Itraconazol, Ketoconazol, Fluconazol oder Voriconazol
- Arzneimittel zur Behandlung von HIV-Infektionen wie Ritonavir oder Nelfinavir
- Arzneimittel zur Behandlung von unregelmäßigem Herzschlag wie Amiodaron, Diltiazem oder Verapamil
- Rifampicin (zur Behandlung von Tuberkulose)
- Einige Arzneimittel zur Behandlung von Epilepsie (wie Carbamazepin, Phenobarbital oder Phenytoin).
Informieren Sie Ihren Arzt, wenn Sie bestimmte Arzneimittel zur Behandlung von Depressionen anwenden, die als Serotonin-Wiederaufnahmehemmer (SSRIs), Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRIs) oder MAO-Hemmer bekannt sind.Ihr Arzt muss über die Anwendung dieser Arzneimittel Bescheid wissen, da die gleichzeitige Anwendung von Fentanyl das Risiko für die Entwicklung eines Serotoninsyndroms, einer potenziell lebensbedrohlichen Erkrankung, erhöhen kann.
Ihr Arzt weiß, welche Arzneimittel während der Anwendung von Fentanyl Zentiva sicher sind. Sie müssen möglicherweise engmaschig überwacht werden, wenn Sie eines der oben aufgeführten Arzneimittel einnehmen oder wenn Sie die Einnahme bestimmter oben aufgeführter Arzneimittel abgesetzt haben, da dies die Dosierung beeinflussen kann von Fentanyl Sie benötigen.
Wenn Sie sich nicht sicher sind, ob einer der oben genannten Punkte auf Sie zutrifft, sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Fentanyl Zentiva anwenden.
Operation oder klinische Untersuchungen
Wenn Sie beabsichtigen, ein Anästhetikum zu verabreichen, teilen Sie Ihrem Arzt oder Zahnarzt mit, dass Sie Fentanyl Zentiva anwenden.
Einnahme von Fentanyl Zentiva transdermales Pflaster zusammen mit Nahrungsmitteln, Getränken und Alkohol
Trinken Sie keinen Alkohol, es sei denn, Sie haben vorher mit Ihrem Arzt gesprochen. Fentanyl Zentiva kann Sie schläfrig machen oder Ihre Atmung verlangsamen. Alkoholkonsum kann diese Auswirkungen verschlimmern.
Warnungen Es ist wichtig zu wissen, dass:
Übertragung des Patches an eine andere Person
Das Pflaster darf nur auf der Haut von Personen angewendet werden, denen es von ihrem Arzt verschrieben wurde. Es gibt Berichte über versehentliches Ankleben eines Pflasters an einem Familienmitglied eines Benutzers aufgrund von engem Kontakt oder gemeinsamem Bett. Das Aufkleben des Pflasters auf eine andere Person (insbesondere ein Kind) kann zu einer Überdosierung führen. Wenn das Pflaster auf der Haut einer anderen Person haftet, entfernen Sie das Pflaster sofort und wenden Sie sich an Ihren Arzt.
- Wie andere starke Schmerzmittel kann Fentanyl Zentiva Schläfrigkeit und eine langsamere oder schwächere Atmung verursachen. Sehr selten können diese Atembeschwerden bei Personen, die noch nie starke morphinhaltige Schmerzmittel (wie Fentanyl Zentiva) oder Morphin selbst angewendet haben, lebensbedrohlich oder tödlich sein. Wenn Sie oder Ihr Partner oder Ihre Bezugsperson feststellen, dass Sie oder Ihr Kind viel langsamer oder schwächer atmen, dann:
- Entfernen Sie das Pflaster
- Kontaktieren Sie Ihren Arzt oder gehen Sie direkt zum nächsten Krankenhaus
- Bewegen und reden Sie so viel wie möglich
- Wenn Sie während der Anwendung von Fentanyl Zentiva Fieber verspüren, sprechen Sie mit Ihrem Arzt, da dies die Passage des Arzneimittels durch die Haut beeinflussen kann.
- Setzen Sie das Pflaster nicht direkter Hitze wie Heizkissen, Wärmflaschen, Heizdecken, Betten mit beheizten Wassermatratzen, Wärme- oder Bräunungslampen, intensiver Sonne, längeren heißen Bädern, Sauna oder Schwimmbad mit heißem Wasser aus des Arzneimittels durch die Haut.
- Fragen Sie vor der Anwendung dieses Arzneimittels mit Ihrem Arzt oder Apotheker, wenn Sie Folgendes haben oder jemals hatten:
- Lungen- oder Atemprobleme
- Probleme mit Herz, Blutdruck oder Blutvolumen, Leber oder Niere
- Hirntumore
- Anhaltende Kopfschmerzen oder Hirnverletzungen
Ihr Arzt muss Sie möglicherweise genauer untersuchen
- Wenn Sie sehr krank, sehr dünn oder älter sind, reagieren Sie möglicherweise empfindlicher auf die Wirkung des Pflasters
- Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Fentanyl Zentiva einnehmen.
- Wie bei vielen anderen starken Schmerzmitteln kann die wiederholte Anwendung der Pflaster zu einer Medikamententoleranz oder einer Entwicklung einer Abhängigkeit von dem Medikament führen.
- Sprechen Sie mit Ihrem Arzt, wenn Sie Alkohol, verschreibungspflichtige Medikamente oder illegale Drogen missbraucht haben oder davon abhängig sind
- Fentanyl Zentiva kann Verstopfung verursachen. Sprechen Sie mit Ihrem Arzt oder Apotheker, der Ihnen sagen wird, wie Sie Verstopfung vorbeugen können.
Wenn Sie sich nicht sicher sind, ob einer der oben genannten Punkte auf Sie zutrifft, sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Fentanyl Zentiva anwenden.
Kinder und Jugendliche
Fentanyl Zentiva darf bei Kindern unter 2 Jahren nicht angewendet werden.
Fentanyl Zentiva darf nicht bei Kindern angewendet werden, die zuvor nicht mit starken Schmerzmitteln wie Morphin behandelt wurden.
Andere Arten von Patches
Es gibt andere Arten von transdermalen Fentanyl-Pflastern, die jedoch nicht genau gleich sind. Wenn das Pflaster anders aussieht als das, was Sie zuvor verwendet haben, sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie es anwenden.
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Es liegen Berichte über Entzugserscheinungen bei Neugeborenen vor, nachdem die Mutter während der Schwangerschaft über einen längeren Zeitraum Fentanyl angewendet hatte. Fentanyl Zentiva sollte während der Geburt nicht angewendet werden, da das Arzneimittel die Atmung des Babys beeinträchtigen kann. Stillen Sie nicht während der Einnahme von Fentanyl Zentiva Sie sollten 3 Tage lang nicht stillen, nachdem Sie das Fentanyl Zentiva Pflaster entfernt haben, da geringe Mengen des Arzneimittels in die Muttermilch übergehen können.
Fragen Sie vor der Einnahme von Arzneimitteln während der Schwangerschaft oder Stillzeit Ihren Arzt oder Apotheker um Rat.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Fentanyl Zentiva kann Sie schläfrig machen. Führen Sie in diesem Fall kein Fahrzeug und bedienen Sie keine Werkzeuge oder Maschinen.
Dosierung und Art der Anwendung Wie man Fentanyl verwendet - Generisches Medikament: Dosierung
Wenden Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker an. Fragen Sie im Zweifelsfall Ihren Arzt oder Apotheker.
Verwendung und Austausch von Patches
- Jedes Pflaster enthält genügend Arzneimittel für mindestens 3 Tage (72 Stunden).
- Sie müssen das Pflaster immer am dritten Tag wechseln, es sei denn, Ihr Arzt sagt Ihnen etwas anderes
- Entfernen Sie immer das alte Pflaster, bevor Sie ein neues anbringen
- Wechseln Sie Ihr Pflaster immer alle 3 Tage (72 Stunden) zur gleichen Tageszeit.
- Wenn Sie mehr als einen Patch verwenden, ändern Sie alle Patches gleichzeitig
- Notieren Sie sich Tag, Datum und Uhrzeit der Anwendung des Pflasters, um sich daran zu erinnern, wann Sie es ändern müssen
- Die folgende Tabelle zeigt Ihnen, an welchem Wochentag Sie das Pflaster wechseln müssen:
Wenden Sie den Patch an Wechseln Sie gleichzeitig den Patch auf Montag Donnerstag Dienstag Freitag Mittwoch Samstag Donnerstag Sonntag Freitag Montag Samstag Dienstag Sonntag Mittwoch
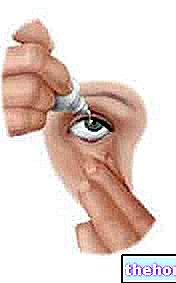
Wo soll der Patch angewendet werden?
Erwachsene
- Bringen Sie das Pflaster auf der flachen Oberfläche des Oberkörpers oder Arms des Kindes an
- Bringen Sie das Pflaster immer am oberen Rücken an, damit Ihr Kind es schwer berühren oder entfernen kann
- Überprüfen Sie sehr oft, ob das Pflaster auf der Haut haftet
- Es ist wichtig, dass Ihr Kind das Pflaster nicht entfernt und in den Mund nimmt, da dies lebensbedrohlich oder sogar tödlich sein könnte
- Es kann einige Zeit dauern, bis das Pflaster vollständig wirksam ist. Daher benötigt Ihr Kind möglicherweise ein zusätzliches Schmerzmittel, bis das Pflaster wirksam ist. Ihr Arzt wird Sie informieren, wenn dies erforderlich ist.
- Kinder sollten bis zu 48 Stunden lang engmaschig überwacht werden nach:
- Die Anwendung des ersten Patches
- Die Anwendung eines hochdosierten Pflasters
Bringen Sie das Pflaster für Sie oder Ihr Kind nicht an:
- Der gleiche Bereich zweimal hintereinander
- Empfindliche Bereiche der Haut, die sich in Bewegung befinden, Schnittwunden, Hautunreinheiten oder andere Hautunreinheiten
- Haut mit vielen Haaren. Wenn Haare vorhanden sind, nicht rasieren (Rasur kann die Haut reizen), sondern die Haare so nah wie möglich an der Haut schneiden.
Es dauert mehrere Tage, bis das Pflaster auf dieselbe Hautstelle aufgetragen wird.
Wenden Sie den Patch an
Phase 1: Hautvorbereitung
- Stellen Sie sicher, dass Ihre Haut vollständig trocken, sauber und kühl ist, bevor Sie das Pflaster darüber auftragen
- Wenn Sie Ihre Haut reinigen müssen, verwenden Sie nur kaltes Wasser
- Verwenden Sie keine Seife oder andere Reinigungsmittel, Cremes, Schäume, Öle oder Talkum, bevor Sie das Pflaster anbringen
- Kleben Sie das Pflaster nicht nach einem heißen Bad oder einer heißen Dusche direkt auf die Haut
Schritt 2: Beutel öffnen
- Jedes Pflaster ist in einem eigenen Beutel versiegelt
- Reißen oder schneiden, um den Beutel zu öffnen
- Schneiden Sie den Rand des Beutels vorsichtig ab oder reißen Sie ihn vollständig ab (bei Verwendung einer Schere so nah wie möglich am Rand des Beutels schneiden, um eine Beschädigung des Pflasters zu vermeiden)
- Fassen Sie beide Seiten an, um den Beutel zu öffnen, und ziehen Sie
- Nehmen Sie das Pflaster und verwenden Sie es sofort
- Bewahren Sie den Beutel leer auf, um das gebrauchte Pflaster später zu entsorgen
- Verwenden Sie jeden Patch nur einmal
- Nehmen Sie das Pflaster nicht aus dem Beutel, bevor Sie es verwenden möchten
- Überprüfen Sie den Patch auf Beschädigungen
- Verwenden Sie das Pflaster nicht, wenn es zerteilt oder geschnitten wurde oder beschädigt aussieht
- Schneiden oder teilen Sie das Pflaster niemals
Schritt 3: Abziehen und drücken
- Stellen Sie sicher, dass das Pflaster von loser Kleidung bedeckt ist und nicht unter einem engen oder elastischen Band feststeckt
- Ziehen Sie vorsichtig eine Hälfte der Plastikfolie von der Mitte des Pflasters ab. Versuchen Sie, die klebrige Seite des Pflasters nicht zu berühren
- Drücken Sie den klebrigen Teil des Pflasters auf die Haut
- Entfernen Sie den anderen Teil des Trägers und drücken Sie das gesamte Pflaster mit der Handfläche auf die Haut
- Halten Sie es mindestens 30 Sekunden lang. Stellen Sie sicher, dass es gut verklebt ist, insbesondere die Ränder.
Schritt 4: Entsorgung des Pflasters
- Falten Sie das Pflaster sofort nach dem Entfernen in der Mitte zurück, sodass die Klebeseite mit sich selbst schließt
- Legen Sie das Pflaster in den Originalbeutel und entsorgen Sie es im Hausmüll
- Da gebrauchte Pflaster einige Arzneimittel enthalten, die für Kinder gefährlich sein können, bewahren Sie gebrauchte Pflaster für Kinder unzugänglich auf.
Schritt 5: Waschen
- Waschen Sie sich anschließend die Hände mit klarem Wasser Erfahren Sie mehr über Fentanyl Zentiva Pflaster Wie schnell das Pflaster wirkt
- Es kann bis zu 1 Tag dauern, bis das erste Pflaster vollständig wirkt
- Ihr Arzt kann Ihnen für den ersten Tag oder länger ein zweites Schmerzmittel verschreiben
- Danach soll das Pflaster Ihnen helfen, die Schmerzen kontinuierlich zu lindern, damit Sie die Einnahme anderer Schmerzmittel abbrechen können.Ihr Arzt kann jedoch von Zeit zu Zeit ein anderes Schmerzmittel verschreiben.
Wenn Sie vergessen, Ihr Pflaster zu wechseln
- Wenn Sie es vergessen, wechseln Sie das Pflaster, sobald Sie sich daran erinnern, und notieren Sie sich den Tag und die Uhrzeit. Wechseln Sie das Pflaster wie gewohnt nach 3 Tagen (72 Stunden) erneut.
- Wenn Sie Ihr Pflaster sehr spät wechseln, sollten Sie mit Ihrem Arzt sprechen, da Sie möglicherweise ein zusätzliches Schmerzmittel benötigen, aber legen Sie kein zusätzliches Pflaster an.
Wenn ein Pflaster abfällt
- Wenn ein Pflaster vor dem Wechseln abfällt, kleben Sie sofort ein neues auf und notieren Sie sich Tag und Uhrzeit.
- Der Oberkörper oder die Arme
- Der obere Rücken Ihres Babys
- Lassen Sie es weitere 3 Tage (72 Stunden) einwirken, bevor Sie es wie gewohnt gegen ein anderes Pflaster austauschen
- Wenn Ihre Pflaster immer wieder abfallen, sprechen Sie mit Ihrem Arzt, dem medizinischen Fachpersonal oder Apotheker.
Wenn das Pflaster an einer anderen Person klebt
- Verwenden Sie das Pflaster nur auf der Haut der Person, der es verschrieben wurde
- Stellen Sie sicher, dass sich das Pflaster nicht löst und an einer anderen Person oder einem Kind haftet, insbesondere wenn Sie ein Bett teilen oder in engem Kontakt stehen
- Wenn ein Pflaster versehentlich an einer anderen Person klebt, entfernen Sie es sofort und rufen Sie Ihren Arzt an.
Wie lange sollte das Pflaster verwendet werden?
Fentanyl Zentiva Pflaster sind für lang anhaltende Schmerzen. Ihr Arzt wird Ihnen sagen, wie lange Sie es anwenden sollen.
Wenn die Schmerzen schlimmer werden
- Wenn sich die Schmerzen während der Anwendung dieser Pflaster verschlimmern, kann Ihr Arzt Ihnen ein Pflaster mit höherer Stärke verschreiben oder Ihnen ein zusätzliches Schmerzmittel (oder beides) verabreichen.
- Wenn eine Erhöhung der Pflasterstärke nicht funktioniert, kann Ihr Arzt entscheiden, die Behandlung abzubrechen.
Wenn Sie die Patches nicht mehr verwenden möchten
- Sprechen Sie mit Ihrem Arzt, bevor Sie die Anwendung dieser Pflaster abbrechen
- Wenn Sie sie seit einiger Zeit verwenden, hat sich Ihr Körper möglicherweise daran gewöhnt. Plötzliches Aufhören kann zu Übelkeit führen
- Wenn Sie die Anwendung der Pflaster abbrechen, beginnen Sie die Anwendung nicht ohne vorherige Rücksprache mit Ihrem Arzt. Möglicherweise benötigen Sie bei der erneuten Anwendung ein Pflaster mit einer anderen Stärke.
Tägliche Aktivitäten während der Anwendung der Pflaster
- Die Patches sind wasserabweisend
- Während Sie das Pflaster tragen, können Sie duschen oder baden, aber nicht auf dem Pflaster reiben
- Wenn Ihr Arzt zustimmt, können Sie während der Anwendung des Pflasters Gymnastik oder Sport treiben
- Sie können schwimmen, während Sie das Pflaster auftragen, aber:
- Verwenden Sie keine Schwimmbäder mit heißem Wasser
- Legen Sie kein elastisches oder enges Band über das Pflaster
- Setzen Sie das Pflaster keinen direkten Wärmequellen wie Heizkissen, Wärmflaschen, Heizdecken, beheizten Wasserbetten, Wärme- oder Bräunungslampen, intensiver Sonne, längeren heißen Bädern oder Saunen aus. Diese können die Aufnahme des Arzneimittels durch die Haut.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
Überdosierung Was ist zu tun, wenn Sie eine Überdosis von Fentanyl - Generika eingenommen haben
Wenn Sie mehrere Pflaster aufgetragen haben oder die Stärke des Pflasters nicht stimmt, entfernen Sie das Pflaster und wenden Sie sich an Ihren Arzt oder suchen Sie das nächste Krankenhaus auf. Anzeichen einer Überdosierung sind Atembeschwerden oder flache Atmung, Müdigkeit, übermäßige Schläfrigkeit, Unfähigkeit, klar zu denken, normal zu gehen oder zu sprechen und sich ohnmächtig, benommen oder verwirrt zu fühlen.
Nebenwirkungen Was sind die Nebenwirkungen von Fentanyl - Generikum?
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Entfernen Sie das Pflaster und wenden Sie sich sofort an Ihren Arzt oder suchen Sie das nächste Krankenhaus auf, wenn Sie eine der unten aufgeführten Wirkungen bemerken oder vermuten.Sie benötigen möglicherweise dringend ärztliche Behandlung.
- Wenn Sie sich ungewöhnlich schläfrig fühlen, atmen Sie langsamer oder schwächer als gewöhnlich. Sehr selten können diese Atembeschwerden lebensbedrohlich oder sogar tödlich sein, insbesondere bei Patienten, die noch nie zuvor starke Opioid-Schmerzmittel (wie Fentanyl oder Morphin) angewendet haben.Wenn Sie oder Ihr Partner oder Ihre Bezugsperson bemerken, dass Sie oder Ihr Baby langsamer oder schwächer atmen, befolgen Sie die obigen Anweisungen und bleiben Sie in Bewegung und sprechen Sie so viel wie möglich.
- Plötzliches Anschwellen von Gesicht oder Rachen, starke Reizung, Rötung oder Blasenbildung der Haut. Dies können Anzeichen einer schweren allergischen Reaktion sein. Dies tritt nur bei einer kleinen Anzahl von Menschen auf.
- Krämpfe, Krampfanfälle. Diese Wirkungen können bis zu 1 von 100 Behandelten betreffen.
- Bewusstlosigkeit oder Bewusstlosigkeit, diese Wirkungen können bis zu 1 von 100 Behandelten betreffen.
Die folgenden Nebenwirkungen wurden berichtet
Sehr häufig (kann mehr als 1 von 10 Behandelten betreffen)
- Übelkeit (Übelkeit) oder Übelkeit (Erbrechen), Verstopfung
- Schwindel, Schläfrigkeit oder Schlaflosigkeit
- Kopfschmerzen
Häufig (kann bis zu 1 von 10 Behandelten betreffen)
- Allergische Reaktionen
- Wenn Sie bemerken, dass Sie einen ungewöhnlichen Herzschlag (auch Herzklopfen genannt) haben, einen schnellen Herzschlag
- Bluthochdruck - Appetitlosigkeit oder trockener Mund
- Sedierung, Nervosität, Angst oder Depression
- Verwirrung, Halluzinationen (Dinge sehen oder hören, die nicht da sind)
- Kribbeln, Zittern, Benommenheit
- Muskelkrämpfe
- Magenschmerzen, Verdauungsstörungen, Schwierigkeiten beim Wasserlassen
- Durchfall
- Kältegefühl, übermäßiges Schwitzen
- Allgemeines Unwohlsein, Müdigkeit, Schwäche
- Schwellung der Hände, Knöchel oder Füße
- Juckende Haut, Hautausschlag oder rote Haut
Gelegentlich (kann bis zu 1 von 100 Behandelten betreffen)
- Grippeähnliche Symptome
- Niedrige Herzfrequenz
- Niedriger Blutdruck
- Verminderte Empfindlichkeit, insbesondere der Haut
- Verschwommene Sicht
- Bläuliche Tönung der Haut
- Sich aufgeregt, desorientiert, aufgeregt oder ungewöhnlich sorglos fühlen
- Gedächtnisverlust, Schwierigkeiten beim Sprechen
- Ekzeme und/oder andere Hauterkrankungen einschließlich Dermatitis im Bereich der Pflasteranwendung
- Sexuelle Dysfunktionen
- Vollständiger Darmverschluss
- Muskelkontraktionen
- Fieber, veränderte Körpertemperatur
- Entzugserscheinungen (wie Übelkeit, Übelkeit, Durchfall, Angst oder Schüttelfrost)
Seltene Nebenwirkungen (kann bis zu 1 von 1000 Behandelten betreffen)
- Verschwommenes Sehen durch Verengung der Pupillen
- Schluckauf
- Teilweise Obstruktion des Dünn- oder Dickdarms
- Unregelmäßige Herzschläge
- Erweiterung der Blutgefäße
Sehr seltene Nebenwirkungen (kann bis zu 1 von 10.000 Behandelten betreffen)
- Schmerzhafte Schwellung - Verlust der Koordination und des Gleichgewichts
- Faules Auge
- Blasenschmerzen, reduzierter Harnabgang im Vergleich zu normal während des Tages
Die folgenden Nebenwirkungen wurden in klinischen Studien bei Kindern (bis 18 Jahre) berichtet:
Sehr häufige Nebenwirkungen (kann mehr als 1 von 10 Behandelten betreffen)
- Kopfschmerzen
- Sich krank fühlen oder krank sein
- Verstopfung, Durchfall
- Juckreiz
Häufige Nebenwirkungen (kann bis zu 1 von 10 Behandelten betreffen)
- Allergische Reaktionen
- Appetitlosigkeit, Bauchschmerzen
- Schlafstörungen, Schläfrigkeit, Müdigkeit, Schwächegefühl
- sich besorgt oder depressiv fühlen, halluzinieren (Dinge sehen oder hören, die nicht da sind) Schwindel
- Zittern, vermindertes Empfinden insbesondere der Haut
- Trockener Mund
- Hautausschlag, übermäßiges Schwitzen, Rötung der Haut
- Muskelkrämpfe
- Schwierigkeiten beim Wasserlassen
- Schwellung der Hände, Knöchel oder Füße
- Hautreaktionen im Bereich der Pflasterapplikation
Gelegentliche Nebenwirkungen (kann bis zu 1 von 100 Behandelten betreffen)
- Verwechslung
- Kribbeln
- Abnahme der Pupillengröße
- Schwindlig fühlen
- Bläuliche Verfärbung der Haut, Ekzeme und/oder andere Hauterkrankungen einschließlich Dermatitis im Bereich der Pflasteranwendung
- Entzugserscheinungen (wie Übelkeit, Unwohlsein, Durchfall, Angst oder Schüttelfrost) grippeähnliche Symptome
Wenn Sie eine dieser Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, das medizinische Fachpersonal oder Ihren Apotheker.
Hautausschlag, Juckreiz oder Schwitzen (kann bis zu 1 von 10 Behandelten betreffen). Möglicherweise bemerken Sie einen leichten Hautausschlag, eine Rötung oder ein Jucken der Haut im Bereich der Pflasteranwendung. Dies ist normalerweise leicht und verschwindet nach Entfernen des Pflasters. Wenn dies nicht der Fall ist oder das Pflaster Ihre Haut stark reizt, informieren Sie bitte Ihren Arzt.
Es gibt Berichte über Entzugserscheinungen bei Neugeborenen nach längerer Anwendung von Fentanyl durch die Mutter während der Schwangerschaft.
Wie bei vielen anderen starken Schmerzmitteln kann die wiederholte Anwendung der Pflaster zu einer Arzneimitteltoleranz oder -sucht führen.
Wenn eine der Nebenwirkungen bei Ihnen auftritt, informieren Sie bitte Ihren Arzt, das medizinische Fachpersonal oder Ihren Apotheker.
Wenn Sie von einem anderen Schmerzmittel auf Fentanyl Zentiva Pflaster umstellen, können Nebenwirkungen wie Unwohlsein, Übelkeit, Durchfall, Angst oder Schüttelfrost auftreten. Informieren Sie Ihren Arzt, wenn Sie eine dieser Wirkungen bemerken.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker, einschließlich aller möglichen Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind. Sie können Nebenwirkungen auch direkt über das nationale Meldesystem unter www.agenziafarmaco.gov.it/it/responsabili melden.Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
Ablauf und Aufbewahrung
Bewahren Sie dieses Arzneimittel auch nach der Anwendung für Kinder unzugänglich auf. Auch nach der Anwendung verbleiben hohe Wirkstoffmengen in den transdermalen Pflastern.
Verwenden Sie dieses Arzneimittel nicht nach dem auf der Packung angegebenen Verfallsdatum. Das Ablaufdatum bezieht sich auf den letzten Tag dieses Monats.
Nicht über 30 °C lagern.
Handhabung des Patches
Gebrauchte Pflaster sollten so gefaltet werden, dass der klebrige Teil des Pflasters an sich selbst haftet und anschließend sicher entsorgt werden muss. Die versehentliche Exposition von gebrauchten und unbenutzten Pflastern kann insbesondere bei Kindern tödliche Folgen haben.Unbenutzte Pflaster sollten an die Apotheke (Krankenhaus) zurückgegeben werden.
Sonstige_Informationen "> Sonstige Informationen
Was Fentanyl Zentiva enthält
- Der Wirkstoff ist Fentanyl
Fentanyl Zentiva 25 Mikrogramm/h transdermales Pflaster
Jedes Pflaster setzt 25 Mikrogramm Fentanyl pro Stunde frei.Jedes 7,5 cm2 Pflaster enthält 4,125 mg Fentanyl.
Fentanyl Zentiva 50 Mikrogramm/h transdermales Pflaster
Jedes Pflaster setzt 50 Mikrogramm Fentanyl pro Stunde frei.Jedes Pflaster von 15 cm2 enthält 8,25 mg Fentanyl.
Fentanyl Zentiva 75 Mikrogramm/h transdermales Pflaster
Jedes Pflaster setzt 75 Mikrogramm Fentanyl pro Stunde frei.Jedes Pflaster von 22,5 cm2 enthält 12,375 mg Fentanyl.
Fentanyl Zentiva 100 Mikrogramm/h transdermales Pflaster
Jedes Pflaster setzt 100 Mikrogramm Fentanyl pro Stunde frei.Jedes Pflaster mit 30 cm2 enthält 16,5 mg Fentanyl.
- Die sonstigen Bestandteile sind: Klebeschicht: Polyacrylat-Klebeschicht. Trägerfolie: Polypropylenfolie, blaue Druckfarbe.
Trennmembran: Polyethylenterephthalat (silikonisiert) Blatt.
Wie Fentanyl Zentiva transdermales Pflaster aussieht und Inhalt der Packung
Fentanyl Zentiva transdermales Pflaster ist ein transparentes transdermales Pflaster mit einer Klebefläche, durch die es auf der Haut haften kann. Die transdermalen Pflaster haben einen blauen Aufdruck, der die Stärke anzeigt.
Fentanyl Zentiva transdermales Pflaster ist in Packungen mit 3, 5, 10 oder 20 transdermalen Pflastern erhältlich.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
HINWEIS
Es ist nicht möglich, alle erforderlichen Stärken mit Fentanyl Zentiva transdermalem Pflaster zu erreichen. Es gibt andere Fentanyl-Pflaster, mit denen Sie diese unterschiedlichen Dosierungen erreichen können.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu erhalten, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS -
FENTANYL ZENTIVA TRANSDERMAL PATCH
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG -
Fentanyl Zentiva 25 mcg / h transdermales Pflaster
Jeden Das Pflaster setzt 25 µg Fentanyl pro Stunde frei.Jedes 7,5 cm² Pflaster enthält 4,125 mg Fentanyl.
Fentanyl Zentiva 50 mcg / h transdermales Pflaster
Jeden Pflaster setzt 50 µg Fentanyl pro Stunde frei.Jedes Pflaster von 15 cm² enthält 8,25 mg Fentanyl.
Fentanyl Zentiva 75 mcg / h transdermales Pflaster
Jeden Das Pflaster setzt 75 µg Fentanyl pro Stunde frei.Jedes Pflaster von 22,5 cm² enthält 12,375 mg Fentanyl.
Fentanyl Zentiva 100 mcg / h transdermales Pflaster
Jeden Pflaster setzt 100 µg Fentanyl pro Stunde frei.Jedes Pflaster von 30 cm² enthält 16,5 mg Fentanyl.
Die vollständige Liste der sonstigen Bestandteile finden Sie in Abschnitt 6.1
03.0 DARREICHUNGSFORM -
Transdermales Pflaster
Fentanyl Zentiva 25 mcg / h transdermales Pflaster
Klarer und farbloser Patch mit blauem Aufdruck auf der Schutzfolie: "fentanyl 25 mcg / h".
Fentanyl Zentiva 50 mcg / h transdermales Pflaster
Klarer und farbloser Patch mit blauem Aufdruck auf der Schutzfolie: "fentanyl 50 mcg / h".
Fentanyl Zentiva 75 mcg / h transdermales Pflaster
Klarer und farbloser Patch mit blauem Aufdruck auf der Schutzfolie: "fentanyl 75 mcg / h".
Fentanyl Zentiva 100 mcg / h transdermales Pflaster
Klarer und farbloser Patch mit blauem Aufdruck auf der Schutzfolie: "fentanyl 100 mcg / h".
04.0 KLINISCHE INFORMATIONEN -
04.1 Anwendungsgebiete -
Fentanyl Zentiva transdermales Pflaster ist angezeigt:
Erwachsene:
• Bei starken chronischen Schmerzen, die nur mit Opioid-Analgetika ausreichend behandelt werden können
Kinder:
- zur Langzeitbehandlung schwerer chronischer Schmerzen bei Kindern ab 2 Jahren unter Opioidtherapie.
04.2 Dosierung und Art der Anwendung -
Zur transdermalen Anwendung
Fentanyl Zentiva transdermales Pflaster sollte auf nicht gereizte, nicht bestrahlte Haut auf einer glatten Oberfläche des Rumpfes oder Oberarms aufgetragen werden. Bei kleinen Kindern ist der obere Rücken die am besten geeignete Stelle, um das Pflaster anzubringen, um die Möglichkeit zu minimieren, dass das Kind es entfernt. Es sollte ein haarloser Bereich ausgewählt werden. Ist dies nicht möglich, müssen die Haare auf der Anwendungsstelle vor der Anwendung getrimmt (nicht rasiert) werden. Wenn der für die Anwendung des Fentanyl Zentiva transdermalen Pflasters gewählte Bereich vor dem Anbringen des Pflasters gereinigt werden muss, sollte er mit Wasser gereinigt werden. Seifen, Öle, Lotionen oder andere Mittel, die die Haut reizen oder ihre Eigenschaften verändern können, dürfen nicht verwendet werden. Die Haut muss vor dem Auftragen des Pflasters vollständig trocken sein. Patches sollten vor der Verwendung überprüft werden. Patches, die geschnitten, gespalten oder anderweitig beschädigt sind, sollten nicht verwendet werden.
Das Fentanyl Zentiva transdermale Pflaster muss aus der Schutzhülle entfernt werden, indem zuerst die Kerbe (befindet sich in der Nähe der Pfeilspitze auf dem Beuteletikett) gefaltet und dann das Verpackungsmaterial vorsichtig abgerissen wird. Wenn die Hülle mit einer Schere geöffnet wird, sollte der Schnitt vorgenommen werden nahe der versiegelten Kante, um den Patch im Inneren nicht zu beschädigen.
Fentanyl Zentiva transdermales Pflaster sollte sofort nach Entnahme aus dem versiegelten Beutel angebracht werden. Vermeiden Sie es, die klebrige Seite des Pflasters zu berühren. Nach dem Entfernen beider Teile der Schutzschicht sollte das transdermale Pflaster mit der Handfläche fest auf die Applikationsstelle gedrückt werden 30 Sekunden lang, um sicherzustellen, dass der Kontakt vollständig ist, insbesondere an den Rändern, dann waschen Sie Ihre Hände mit sauberem Wasser.
Fentanyl Zentiva transdermales Pflaster sollte 72 aufeinanderfolgende Stunden lang aufgetragen bleiben. Nachdem das vorherige transdermale Pflaster entfernt wurde, sollte dann ein neues Pflaster auf einer anderen Hautstelle angebracht werden.Es kann mehrere Tage dauern, bis ein neues Pflaster auf derselben Hautstelle angebrachtwerden kann.
Die Notwendigkeit einer Fortsetzung der Behandlung sollte in regelmäßigen Abständen beurteilt werden.
Auswahl der Anfangsdosis
Die geeignete Anfangsdosis von Fentanyl Zentiva transdermalem Pflaster sollte sich nach der aktuellen Opioidanwendung des Patienten richten.
Es wird empfohlen, Fentanyl Zentiva transdermales Pflaster bei Patienten mit nachgewiesener Opioidtoleranz anzuwenden. Andere Faktoren, die berücksichtigt werden müssen, sind der aktuelle Allgemeinzustand und der medizinische Zustand des Patienten, einschließlich Körpermasse, Alter und Grad der Schwächung sowie der Grad der Opioidtoleranz.
Erwachsene
Opioidtolerante Patienten
Informationen zur Umstellung von Opioid-toleranten Patienten von oralen oder parenteralen Opioiden auf Fentanyl Zentiva transdermales Pflaster finden Sie in der Tabelle Umwandlung der äquianalgetischen Potenz unten gezeigt. Die Dosierung kann dementsprechend bei Bedarf in Schritten von 12,5 oder 25 µg/h nach oben oder unten titriert werden, um die niedrigste angemessene Dosis des Fentanyl Zentiva transdermalen Pflasters basierend auf dem Ansprechen und der Dosis des zusätzlich benötigten Analgetikums zu erreichen.
Opiat-naive Patienten
Bei Opioid-naiven Patienten sollte die normale Anfangsdosis von Fentanyl 25 µg/h nicht überschreiten.
Die klinische Erfahrung mit Fentanyl Zentiva transdermalem Pflaster bei Patienten ist begrenzt naiv zu Opiaten. In Situationen, in denen die transdermale Pflastertherapie mit Fentanyl Zentiva bei Opioid-naiven Patienten als angemessen erachtet wird, wird empfohlen, dass diese Patienten zunächst mit niedrig dosierten Opioiden mit sofortiger Wirkstofffreisetzung (z. B. Morphin, Hydromorphin, Oxycodon, Tramadol und Codein) behandelt werden, um eine äquianalgetische Dosierung von Fentanyl Zentiva transdermales Pflaster mit einer Freisetzungsrate von 25 µg / h. Die Patienten können dann auf die Behandlung mit dem transdermalen Pflaster Fentanyl Zentiva 25 µg/h umstellen. Danach kann die Dosis nach Bedarf in Schritten von 12,5 oder 25 µg/h nach oben oder unten titriert werden, um die niedrigste angemessene Dosis von Fentanyl Zentiva transdermalem Pflaster basierend auf dem Ansprechen und dem Bedarf an zusätzlichen Analgetika zu erreichen (siehe auch Abschnitt 4.4).
Äquianalgetische Leistungsumwandlung
• Berechnen Sie die benötigte Schmerzmitteldosis in den letzten 24 Stunden.
• Rechnen Sie diese Menge anhand von Tabelle 1 in die orale Morphin-Äquivalentdosis um. Alle oralen und intramuskulären (IM) Dosen gelten als äquivalent zu 10 mg Morphin i.m. für die analgetische Wirkung.
• Um die Stärke des transdermalen Pflasters von Fentanyl Zentiva abzuleiten, die der 24-Stunden-Berechnung der äquianalgetischen Morphindosis entspricht, verwenden Sie die Dosisumrechnung in Tabelle 2 oder Tabelle 3 wie folgt:
Tabelle 2 gilt für erwachsene Patienten, für die über mehrere Wochen eine orale Dosis von Morphin oder einem anderen Opioid mit sofortiger Freisetzung definiert wurde und die eine Opioid-Rotation benötigen (Umwandlungsverhältnis von oralem Morphin zu transdermalem Fentanyl ungefähr gleich 150: 1).
Tabelle 3 gilt für erwachsene Patienten mit hoher Opioidtoleranz, die eine langzeitstabile und gut verträgliche Opioidtherapie erhalten und die eine Opioidrotation benötigen (Umwandlungsverhältnis von oralem Morphin zu transdermalem Fentanyl ungefähr gleich 100:1).
Die Tabellen 2 und 3 sollten nicht verwendet werden, um von transdermalem Fentanyl auf eine andere Opioid-Behandlung umzustellen.
Tabelle 1: Umrechnung der äquianalgetischen Potenz
* Basierend auf Einzeldosisstudien, in denen eine i.m. Dosis jeder aufgeführten Substanz mit Morphin verglichen wurde, um die relative Wirksamkeit zu bestimmen. Orale Dosen sind die empfohlenen, wenn von der parenteralen auf die orale Verabreichung umgestellt wird.
** Orale Potenz / IM-Potenz für Morphin basiert auf klinischen Erfahrungen bei Patienten mit chronischen Schmerzen.
Referenzen: adaptiert aus dem Foley KM. Die Behandlung von Krebsschmerzen. NEJM 1985; 313: 84-95 und Updates.
Tabelle 2: Empfohlene Anfangsdosierung von Fentanyl Zentiva transdermalem Pflaster basierend auf der täglichen oralen Morphindosis¹ (für Patienten, die mehrere Wochen lang mit oralem Morphin oder Opioiden mit sofortiger Freisetzung stabilisiert wurden und eine Opioid-Rotation benötigen)
¹ In klinischen Studien wurden diese täglichen oralen Dosisbereiche von Morphin als Grundlage für die Umstellung auf Fentanyl transdermales Pflaster verwendet.
Tisch 3: Empfohlene Anfangsdosis von Fentali Zentiva transdermalem Pflaster basierend auf der täglichen oralen Morphindosis (für Patienten mit stabiler und gut verträglicher Opioidtherapie über einen langen Zeitraum und die eine Opioidrotation benötigen)
Die vorherige analgetische Therapie sollte ab dem Zeitpunkt der ersten Anwendung des Pflasters schrittweise abgesetzt werden, bis die analgetische Wirksamkeit mit Fentanyl Zentiva transdermalem Pflaster erreicht wird. Sowohl bei potenten Opioid-naiven als auch bei opioidtoleranten Patienten ist die anfängliche Beurteilung der „Analgetischen Wirkung von Fentanyl Zentiva transdermalem Pflaster“ sollte 24 Stunden nach der Anwendung des Pflasters nicht durchgeführt werden", da die Fentanyl-Serumkonzentration bis zu diesem Zeitpunkt allmählich ansteigt.
Dosistitration und Erhaltungstherapie
Fentanyl Zentiva transdermales Pflaster sollte alle 72 Stunden ausgetauscht werden. Die Dosis sollte individuell titriert werden, bis ein Gleichgewicht zwischen analgetischer Wirkung und Verträglichkeit erreicht ist. Bei Patienten, bei denen innerhalb von 48-72 Stunden nach der Anwendung eine deutliche Abnahme aufgetreten ist, kann ein Austausch von Fentanyl nach 48 Stunden erforderlich sein. Bei unzureichender Analgesie am Ende der ersten Anwendungsperiode kann die Dosis erhöht werden.Eine Dosisanpassung, falls erforderlich, sollte normalerweise in folgenden Titrationsschritten von 25 µg/h bis 75 µg/h durchgeführt werden: 25 µg/h , 37 µg/h, 50 µg/h, 62,5 µg/h und 75 µg/h; Danach sollten Dosisanpassungen normalerweise in Schritten von 25 µg/h vorgenommen werden, obwohl die zusätzliche analgetische Wirkung erforderlich ist (orales Morphin 90 mg/Tag ≈ Fentanyl Zentiva transdermales Pflaster 25 µg/h) und das Ausmaß der Schmerzen des Patienten. Es kann mehr als ein transdermales Fentanyl Zentiva Pflaster verwendet werden, um die gewünschte Dosis zu erreichen. Patienten können bei vorübergehenden schmerzhaften Exazerbationen regelmäßig zusätzliche Dosen eines kurzwirksamen Schmerzmittels benötigen. Wenn die Dosis von Fentanyl Zentiva transdermalem Pflaster 300 µg / h überschreitet, sollte die Anwendung zusätzlicher oder alternativer Analgesiemethoden in Betracht gezogen werden.
Absetzen der transdermalen Pflastertherapie mit Fentanyl Zentiva
Wenn ein Absetzen der transdermalen Pflastertherapie mit Fentanyl Zentiva erforderlich ist, sollte der Ersatz durch andere Opioid-Medikamente schrittweise erfolgen, beginnend mit einer niedrigen Dosis und langsam ansteigen, da die Konzentration von Fentanyl nach Entfernung von Fentanyl Zentiva allmählich abnimmt und dies 17 Stunden dauert oder mehr, damit die Fentanyl-Serumkonzentration um 50 % sinkt (siehe Abschnitt 5.2) Im Allgemeinen sollte die Opioid-Analgesie schrittweise abgesetzt werden, um das Auftreten von Entzugssymptomen zu verhindern.
Bei einigen Patienten können nach Umstellung oder Dosisanpassung Opioid-Entzugssymptome (siehe Abschnitt 4.8) auftreten.
Tabelle 2 und Tabelle 3 sollten nicht für die Umstellung von Fentanyl Zentiva transdermalen Pflastern auf andere Therapien verwendet werden, um eine Überschätzung der neuen Analgetikadosis zu vermeiden und möglicherweise zu einer Überdosierung zu führen.
Anwendung bei älteren Patienten
Daten aus intravenösen Studien mit Fentanyl deuten darauf hin, dass ältere Patienten eine reduzierte Clearance und eine verlängerte Halbwertszeit haben und möglicherweise empfindlicher auf das Arzneimittel reagieren als jüngere Patienten.Ältere, kachektische oder geschwächte Patienten sollten sorgfältig auf Anzeichen einer Fentanyl-Toxizität überwacht werden und, falls erforderlich, sollte die Dosis reduziert werden (siehe Abschnitt 5.2).
Kinder und Jugendliche
Kinder ab 16 Jahren : Befolgen Sie die für Erwachsene festgelegten Dosierungen.
Kinder zwischen 2 und 16 Jahren :
Fentanyl Zentiva transdermales Pflaster sollte nur an opioidtolerante pädiatrische Patienten (im Alter von 2-16 Jahren) verabreicht werden, die bereits mindestens das Äquivalent von 30 mg Morphin pro Tag oral erhalten Zur Umstellung von pädiatrischen Patienten von der Behandlung mit oralen Opioiden Fentanyl Zentiva transdermales Pflaster siehe Tabelle 4 „Empfohlene Dosis von Fentanyl Zentiva transdermales Pflaster basierend auf der täglichen oralen Morphindosis“.
Tabelle 4: Empfohlene Dosis des transdermalen Fentanyl Zentiva-Pflasters basierend auf der oralen Tagesdosis von Morphin ¹
¹ In klinischen Studien wurden diese täglichen Dosisbereiche von oralem Morphin als Ausgangspunkt für die Umstellung auf das transdermale Fentanyl-Pflaster verwendet.
² Die Umstellung auf Fentanyl Zentiva transdermale Pflasterdosen von mehr als 25 µg/h ist für Erwachsene und pädiatrische Patienten gleich.
Für Kinder, die Morphin-Dosen von mehr als 90 mg oral täglich erhalten haben, liegen nur begrenzte Informationen aus klinischen Studien vor. In pädiatrischen Studien wurde die erforderliche Dosis von Fentanyl transdermalem Pflaster nach folgender Umrechnung berechnet: 30 mg bis 44 mg orales Morphin pro Tag oder seine äquivalente Opioiddosis wurde durch ein 12 Gauge Fentanyl transdermales Pflaster ersetzt bei Kindern, die von oralem Morphin (oder einem Äquivalent) auf Fentanyl Zentiva-Pflaster umgestellt werden müssen. Die Umstellung von Fentanyl Zentiva transdermalem Pflaster auf andere Opioide sollte aufgrund der möglichen Überdosierung nicht angewendet werden.
Die analgetische Wirkung der ersten Dosis des Fentanyl Zentiva Pflasters ist in den ersten 24 Stunden nicht optimal, daher sollte der Patient während der ersten 12 Stunden nach der Umstellung auf das Fentanyl transdermale Pflaster die vorherigen Analgetika in der üblichen Dosis einnehmen In den nächsten 12 Stunden sollten diese Analgetika je nach klinischem Bedarf verabreicht werden.
Da die maximale Fentanyl-Spitze nach 12 oder 24 Stunden Behandlung erreicht wird, wird empfohlen, den Patienten mindestens 48 Stunden nach Beginn der Behandlung mit Fentanyl transdermalem Pflaster oder bis zur Dosistitration auf unerwünschte Ereignisse, einschließlich Hypoventilation, zu überwachen (siehe auch Abschnitt 4.4).
Dosistitration und -erhaltung
Wenn die analgetische Wirkung von Fentanyl Zentiva transdermalem Pflaster unzureichend ist, sollte eine zusätzliche Dosis Morphin oder eines anderen kurzwirksamen Opioids verabreicht werden. Abhängig von der Notwendigkeit, eine zusätzliche analgetische Wirkung zu erzielen, und dem Schmerzzustand des Kindes kann eine Dosiserhöhung beschlossen werden. Die Dosis wird mit jeweils 12 µg / h angepasst.
04.3 Kontraindikationen -
- Überempfindlichkeit gegen den Wirkstoff oder einen der anderen in Abschnitt 6.1 genannten sonstigen Bestandteile.
- Fentanyl Zentiva transdermales Pflaster ist eine Retardformulierung zur Behandlung von chronischen, nicht behandelbaren Schmerzen und ist bei akuten oder postoperativen Schmerzen kontraindiziert, da eine Dosistitration bei kurzzeitiger Anwendung nicht möglich ist und die Möglichkeit einer schweren Atemdepression besteht oder lebensgefährlich.
- Schwere Beeinträchtigung des Zentralnervensystems.
- Schwere Atemdepression
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung -
PATIENTEN, DIE ERNSTE UNERWÜNSCHTE EREIGNISSE MANIFESTIERT HABEN, SOLLTEN MINDESTENS 24 STUNDEN ODER MEHR ÜBERWACHT WERDEN "NACH DEM ENTFERNEN DES FENTANIL ZENTIVA TRANSDERMALEN PATCHES AUFGRUND KLINISCHER SYMPTOME, WEIL DIE SIERIC-KONZENTRATION VON FENTANIL ABNEHMT UND ZWISCHEN ZWISCHEN 13-22 5.2).
Bewahren Sie Fentanyl Zentiva transdermales Pflaster vor und nach der Anwendung stets für Kinder unzugänglich auf.
Fentanyl Zentiva transdermales Pflaster sollte nicht geschnitten werden. Ein gespaltenes, geschnittenes oder in irgendeiner Weise beschädigtes Pflaster sollte nicht verwendet werden.
Die Anwendung von Fentanyl Zentiva bei Opioid-naiven Patienten wurde als initiale Opioidtherapie mit sehr seltenen Fällen schwerer und/oder tödlicher Atemdepression in Verbindung gebracht. Das potenzielle Risiko einer schweren oder potenziell lebensbedrohlichen Hypoventilation besteht auch bei Anwendung der niedrigsten Dosis von Fentanyl Zentiva bei der Erstbehandlung opioidnaiver Patienten Es wird empfohlen, Fentanyl Zentiva bei Patienten anzuwenden, die eine Opioidtoleranz nachgewiesen haben (siehe Abschnitt 4.2).
Wenn Fentanyl Zentiva bei chronischen, nicht behandelbaren Schmerzen angewendet wird, die eine längere Behandlung erfordern, wird dringend empfohlen, dass der Arzt die Behandlungsziele zur Schmerzlinderung und funktionellen Verbesserung in Übereinstimmung mit den lokalen Richtlinien zur Schmerzbehandlung festlegt. Werden diese Ziele nicht erreicht, müssen Arzt und Patient eine Unterbrechung der Behandlung vereinbaren.
Atemwegs beschwerden
Wie bei allen potenten Opioiden kann bei einigen Patienten mit Fentanyl Zentiva transdermalem Pflaster eine schwere Atemdepression auftreten; Patienten sollten beim Einsetzen dieser Wirkung überwacht werden. Eine Atemdepression kann auch nach Entfernen des Pflasters bestehen bleiben. Die Inzidenz einer Atemdepression nimmt mit steigender Fentanyl-Dosis zu (siehe Abschnitt 4.9). ZNS-aktive Arzneimittel können die Atemdepression verstärken (siehe Abschnitt 4.5).
Serotonin-Syndrom
Vorsicht ist geboten, wenn Fentanyl Zentiva zusammen mit Arzneimitteln angewendet wird, die das serotonerge Neurotransmittersystem beeinflussen.
Die Entwicklung eines potenziell lebensbedrohlichen Serotoninsyndroms kann bei gleichzeitiger Anwendung von serotonergen Arzneimitteln wie Serotonin-Wiederaufnahmehemmern (SSRIs) und mit Serotonin- und Noradrenalin-Wiederaufnahmehemmern (SNRIs) und mit Arzneimitteln, die den Serotoninstoffwechsel beeinträchtigen (einschließlich Monoaminoxidase-Hemmern (MAOI)) auftreten. ) Dies kann bei der empfohlenen Dosis auftreten.
Das Serotonin-Syndrom kann Veränderungen des mentalen Zustands (z. B. Agitiertheit, Halluzinationen, Koma), autonome Instabilität (z. B. Tachykardie, instabiler Blutdruck, Hyperthermie), neuromuskuläre Anomalien (z. B. Hyperreflexie, Koordinationsstörungen, Starrheit) und/oder gastrointestinale Symptome (z. B. Übelkeit, Erbrechen) umfassen , Durchfall).
Bei Verdacht auf ein Serotonin-Syndrom sollte ein Absetzen von Fentanyl Zentiva in Erwägung gezogen werden.
Chronische Lungenerkrankung
Fentanyl kann wie andere Opiate bei Patienten mit chronisch obstruktiven Erkrankungen oder anderen Lungenerkrankungen schwerwiegendere Nebenwirkungen verursachen. bei solchen Patienten können Opioide die Atemfrequenz verringern und den Atemwegswiderstand erhöhen.
Drogensucht und Missbrauchspotential
Bei wiederholter Gabe von Opiaten wie Fentanyl können sich Toleranz, körperliche Abhängigkeit und psychische Abhängigkeit entwickeln. Eine iatrogene Abhängigkeit nach Opioidgabe ist selten. Patienten mit einer Drogenabhängigkeit/Alkoholabusus in der Vorgeschichte haben ein höheres Risiko, während einer Opioidbehandlung eine Abhängigkeit und einen Missbrauch zu entwickeln. Patienten mit erhöhtem Risiko für Opioidmissbrauch können mit Opioidformulierungen mit veränderter Wirkstofffreisetzung weiterhin angemessen behandelt werden; diese Patienten müssen jedoch auf verräterische Anzeichen von Missbrauch, Missbrauch oder Abhängigkeit überwacht werden. Ein Missbrauch von Fentanyl kann auf die gleiche Weise auftreten wie bei anderen Opioid-Agonisten Missbrauch oder vorsätzlicher Missbrauch von Fentanyl Zentiva transdermalem Pflaster kann zu Ovedosen und/oder zum Tod führen.
Erhöhter Hirndruck
Fentanyl Zentiva transdermales Pflaster sollte bei Patienten, die besonders empfindlich auf die intrakraniellen Auswirkungen einer CO2-Retention reagieren, wie beispielsweise Patienten mit offensichtlichen Anzeichen eines erhöhten Hirndrucks, Bewusstseinsstörungen oder im Koma, mit Vorsicht angewendet werden.
Fentanyl Zentiva transdermales Pflaster sollte bei Patienten mit Hirntumoren mit Vorsicht angewendet werden.
Herzkrankheit
Opioide können eine Hypotonie verursachen, insbesondere bei Patienten mit akuter Hypovolämie. Eine vorbestehende symptomatische Hypotonie und/oder Hypovolämie sollte vor Beginn der Behandlung mit Fentanyl transdermalen Pflastern korrigiert werden.Fentanyl kann eine Bradykardie auslösen und Fentanyl Zentiva sollte daher bei Patienten mit Bradyarrhythmien mit Vorsicht angewendet werden.
Leberfunktionsstörung
Da Fentanyl in der Leber zu inaktiven Metaboliten metabolisiert wird, kann eine Leberfunktionsstörung seine Elimination verzögern. Wenn Patienten mit eingeschränkter Leberfunktion Fentanyl Zentiva anwenden, sollten sie sorgfältig auf Symptome einer Fentanyl-Toxizität überwacht werden und die Fentanyl-Dosis sollte, falls erforderlich, reduziert werden (siehe Abschnitt 5.2).
Nierenfunktionsstörung
Weniger als 10 % von Fentanyl werden unverändert über die Nieren ausgeschieden, und im Gegensatz zu Morphin sind keine aktiven Metaboliten über die Nieren bekannt. Wenn Patienten mit Nierenfunktionsstörung transdermales Fentanyl verabreicht werden soll, sollten diese engmaschig auf Anzeichen einer Fentanyl-Toxizität überwacht und die Dosis gegebenenfalls reduziert werden (siehe Abschnitt 5.2).
Patienten mit Fieber / Exposition gegenüber externen Wärmequellen
Ein pharmakokinetisches Modell legt nahe, dass die Fentanyl-Serumkonzentration um etwa ein Drittel ansteigen kann, wenn die Körpertemperatur auf 40 °C ansteigt.
Daher sollten Patienten mit Fieber auf Opioid-Nebenwirkungen überwacht und die Dosierung des transdermalen Fentanyl-Pflasters bei Bedarf angepasst werden.
Es besteht ein potenzieller temperaturabhängiger Anstieg der Menge an Fentanyl, die aus dem transdermalen System freigesetzt wird, was zu einer möglichen Überdosierung und zum Tod führen kann.
Eine an gesunden erwachsenen Probanden durchgeführte klinisch-pharmakologische Studie zeigte, dass die Anwendung von Wärme auf das transdermale System von Fentanyl Zentiva die mittleren AUC-Werte von Fentanyl um 120 % und die mittleren Cmax-Werte um 61 % erhöhte.
Alle Patienten sollten angewiesen werden, die Applikationsstelle des Fentanyl Zentiva transdermalen Pflasters keinen direkten externen Wärmequellen wie Heizkissen, Wärmflaschen, Heizdecken, beheizten Wasserbetten, Wärme- oder Bräunungslampen auszusetzen , Sauna oder Schwimmbad mit heißem Wasser, während das Pflaster aufgetragen wird, da eine potenzielle temperaturabhängige Erhöhung der Fentanyl-Freisetzung aus dem Pflaster auftritt.
Wechselwirkungen mit anderen Arzneimitteln
Wechselwirkungen mit CYP3A4-Inhibitoren
Gleichzeitige Anwendung von Fentanyl mit Cytochrom-P450-3A4-Inhibitoren (wie Ritonavir, Ketoconazol, Itraconazol, Fluconazol, Voriconazol, Troleandromycin, Clarithromycin, Erythromycin, Nelfinavir, Nefazodon, Verapamil, Diltiazol, die zu erhöhten Plasmakonzentrationen führen können, die zu erhöhten Plasmakonzentrationen von .Fentanyl führen können) eine Verstärkung oder Verlängerung sowohl der therapeutischen Wirkungen als auch der Nebenwirkungen, die zu einer schweren Atemdepression führen können.In dieser Situation sind besondere Sorgfalt und sorgfältige Beobachtung des Patienten angebracht. Daher wird die gleichzeitige Anwendung des transdermalen Fentanyl-Pflasters mit Cytochrom-P4503A4-Hemmern nicht empfohlen, es sei denn, der Patient wird engmaschig überwacht.Patienten, insbesondere solche, die Fentanyl- und CYP3A4-Hemmer erhalten, sollten auf Anzeichen einer Depression überwacht und gegebenenfalls eine Dosisanpassung vorgenommen werden.
Versehentliche Exposition durch Patch-Transfer
Die versehentliche Übertragung eines Fentanyl-Pflasters auf die Haut eines Nicht-Pflaster-Trägers (insbesondere eines Kindes) in einem Bett oder in engem Körperkontakt mit einem Pflaster-Träger kann bei einem Nicht-Träger zu einer Opioid-Überdosierung führen. Die Patienten sollten darauf hingewiesen werden, dass bei einer versehentlichen Übertragung des Pflasters das übertragene Pflaster sofort von der Haut des Trägers ohne Pflaster entfernt werden sollte (siehe Abschnitt 4.9).
Ältere Patienten
Daten aus intravenösen Studien mit Fentanyl deuten darauf hin, dass ältere Patienten eine reduzierte Clearance und eine verlängerte Halbwertszeit des Arzneimittels haben und möglicherweise empfindlicher auf das Arzneimittel reagieren als junge Patienten.Wenn ältere Patienten Fentanyl Zentiva erhalten, sollten sie sorgfältig auf Anzeichen überwacht werden der Fentanyl-Toxizität und, falls erforderlich, die Dosis reduziert (siehe Abschnitt 5.2).
Magen-Darm-System
Opiate erhöhen den Muskeltonus und vermindern die propulsiven Kontraktionen der glatten Zellen des Gastrointestinaltrakts.Die Folge ist eine Verlängerung der Transitzeit, die für die obstipierende Wirkung von Fentanyl verantwortlich sein kann. Die Patienten sollten über Maßnahmen zur Vorbeugung von Verstopfung aufgeklärt werden und die Anwendung von Abführmitteln als Prophylaxe sollte in Betracht gezogen werden.Bei Patienten mit chronischer Verstopfung ist äußerste Vorsicht geboten.Wenn ein paralytischer Ileus vorliegt oder vermutet wird, sollte die Behandlungmit Fentanyl Zentiva unterbrochen werden.
Pädiatrische Patienten
Fentanyl darf Opioid-naiven pädiatrischen Patienten nicht transdermal verabreicht werden (siehe Abschnitt 4.2). Unabhängig von der verabreichten Dosis von transdermalem Fentanyl besteht die Möglichkeit einer schweren oder lebensbedrohlichen Hypoventilation (siehe Tabelle 2 in Abschnitt 4.2).
Transdermales Fentanyl wurde bei Kindern unter 2 Jahren nicht untersucht, daher sollte es bei diesen Kindern nicht angewendet werden. Fentanyl Zentiva transdermales Pflaster sollte nur Kindern ab 2 Jahren verabreicht werden, die Opioide vertragen (siehe Abschnitt 4.2).
Um eine versehentliche Einnahme durch Kinder zu vermeiden, wählen Sie den Anwendungsbereich des transdermalen Fentanyl Zentiva-Pflasters sorgfältig aus (siehe Abschnitt 4.2) und überwachen Sie sorgfältig die Haftung des Pflasters.
Patch verwerfen
Das verwendete Pflaster kann erhebliche Rückstände des Wirkstoffs enthalten. Daher sollte das Pflaster nach dem Entfernen des gebrauchten Pflasters mit der Klebeschicht nach innen fest in der Mitte gefaltet werden, damit die Klebeschicht nicht außen liegt, und gemäß den Anweisungen in der Verpackung sicher und außerhalb der Reichweite von Kindern entsorgt werden.
Fütterungszeit
Da Fentanyl in die Muttermilch übergeht, sollte das Stillen während der Behandlung mit Fentanyl Zentiva unterbrochen werden (siehe auch Abschnitt 4.6).
Patienten mit Myasthenia gravis
Es können nicht-epileptische (myo) klonische Reaktionen auftreten. Bei der Behandlung von Patienten mit Myasthenia gravis ist Vorsicht geboten.
Gleichzeitige Anwendung von Agonisten/Antagonisten-Kombinationen
Die gleichzeitige Anwendung von Buprenorphin, Nalbuphin oder Pentazocin wird nicht empfohlen (siehe auch Abschnitt 4.5).
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen -
Die gleichzeitige Anwendung anderer Mittel zur Beruhigung des zentralen Nervensystems, einschließlich Opioiden, Sedativa, Anxiolytika, Hypnotika, Allgemeinanästhetika, Phenothiazinen, Tranquilizern, Antipsychotika, Muskel-Skelett-Relaxantien, sedierenden Antihistaminika und alkoholischen Getränken kann zusätzliche dämpfende Wirkungen haben, Hypoventilation und schwere auftreten können Sedierung, Koma oder Tod Die gleichzeitige Anwendung eines der oben genannten Arzneimittel erfordert daher besondere Sorgfalt und Beobachtung.
Fentanyl, ein Arzneimittel mit hoher Clearance, wird hauptsächlich durch CYP3A4 schnell und umfassend metabolisiert. Gleichzeitige Anwendung von Fentanyl transdermalem Pflaster mit Cytochrom P450 3A4 (CYP3A4)-Inhibitoren (z. B. Ritonavir, Ketoconazol, Itraconazol, Fluconazol, Voriconazol, Troleandromycin, Clarithromycin, Erythromycin, Nelemfinavir, erhöhte Plasmakonzentrationen von Fentanyl, die kann eine schwere Atemdepression verursachen.In dieser Situation ist besondere Sorgfalt und Beobachtung des Patienten angezeigt.Die gleichzeitige Anwendung von CYP3A4-Inhibitoren und transdermalem Fentanyl wird nicht empfohlen, es sei denn, der Patient wird engmaschig überwacht (siehe Abschnitt 4.4).
Die gleichzeitige Anwendung mit CYP3A4-Induktoren (z. B. Rifampicin, Carbamazepin, Phenobarbital, Phenytoin) kann zu verringerten Plasmakonzentrationen von Fentanyl und einer verringerten therapeutischen Wirkung führen. Dies kann eine Anpassung der transdermalen Fentanyl-Dosis erforderlich machen. Nach Absetzen der Behandlung mit einem CYP3A4-Induktor nimmt die Wirkung des Induktors allmählich ab und kann zu erhöhten Plasmakonzentrationen von Fentanyl führen, die sowohl therapeutische als auch unerwünschte Wirkungen verstärken oder verlängern und schwere Atemdepression verursachen können.In dieser Situation sorgfältige Überwachung und Dosisanpassung sollte bei Bedarf erfolgen.
Gleichzeitige Anwendung mit Agonisten-/Antagonisten-Kombinationen
Die gleichzeitige Anwendung von Buprenorphin, Nalbuphin oder Pentazocin wird nicht empfohlen.Diese Substanzen haben eine hohe Affinität zu Opioidrezeptoren mit einer relativ geringen intrinsischen Aktivität und antagonisieren daher teilweise die analgetische Wirkung von Fentanyl und können bei Patienten Entzugserscheinungen hervorrufen Abschnitt 4.4).
Monoaminoxidase-Hemmer (MAO-Hemmer)
Die gleichzeitige Anwendung von Fentanyl bei Patienten, die MAO-Hemmer erhalten, wird nicht empfohlen.
Es wurde über schwerwiegende und unerwartete Reaktionen mit MAO-Hemmern berichtet, einschließlich einer Verstärkung von Opioidwirkungen oder einer Verstärkung serotonerger Wirkungen.
Daher sollte Fentanyl in den ersten 14 Tagen nach Beendigung der Behandlung mit MAO-Hemmern nicht angewendet werden.
Serotonerge Medikamente
Die gleichzeitige Anwendung von Fentanyl transdermalem Pflaster mit serotonergen Arzneimitteln wie Serotonin-Wiederaufnahmehemmern (SSRIs) oder Serotonin-Noradrenalin-Wiederaufnahmehemmern (SNRIs) oder Monoaminoxidase-Hemmern (MAOIs) kann das Risiko eines Serotoninsyndroms potenziell erhöhen.
04.6 Schwangerschaft und Stillzeit -
Für die Anwendung von Fentanyl Zentiva bei schwangeren Frauen liegen keine ausreichenden Daten vor. Tierstudien haben eine gewisse Reproduktionstoxizität gezeigt (siehe Abschnitt 5.3). Das potenzielle Risiko für den Menschen ist nicht bekannt, obwohl in anderen Formulierungen Fentanyl als intravenöses Anästhetikum die Plazenta passieren kann in den frühen Stadien der menschlichen Schwangerschaft.
Bei Neugeborenen, deren Mütter während der Schwangerschaft chronisch Fentanyl Zentiva einnahmen, wurde über ein neonatales Abstinenzsyndrom berichtet.
Fentanyl sollte während der Schwangerschaft nicht angewendet werden, es sei denn, dies ist eindeutig erforderlich.
Daher wird die Anwendung von Fentanyl während der Entbindung nicht empfohlen, da es nicht zur Behandlung akuter oder postoperativer Schmerzen verwendet werden sollte (siehe Abschnitte 4.3 und 4.4).
Da Fentanyl außerdem die Plazenta passiert, kann die Anwendung von Fentanyl Zentiva während der Entbindung beim Neugeborenen zu einer Atemdepression führen.
Fentanyl geht in die Muttermilch über und kann beim gestillten Säugling eine Sedierung und Atemdepression verursachen. Das Stillen sollte daher während der Behandlung mit Fentanyl und für mindestens 72 Stunden nach Entfernen des transdermalen Pflasters unterbrochen werden.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen -
Fentanyl Zentiva kann die geistigen und/oder körperlichen Fähigkeiten beeinträchtigen, die erforderlich sind, um potenziell gefährliche Handlungen wie das Führen von Fahrzeugen oder das Bedienen von Maschinen durchzuführen.
04.8 Nebenwirkungen -
Die Sicherheit von Fentanyl wurde an 1854 erwachsenen und pädiatrischen Probanden untersucht, die an 11 klinischen Studien teilnahmen (doppelblindes Fentanyl [Placebo oder Kontrollarzneimittel] und/oder offenes Fentanyl [kein Kontroll- oder oder nicht bösartige Schmerzen.
Diese Patienten erhielten mindestens 1 Dosis Fentanyl und wurden auf Sicherheit untersucht.Basierend auf einem Pool von Sicherheitsdaten aus diesen klinischen Studien waren die am häufigsten berichteten Nebenwirkungen (z. B. ≥ 10 % Inzidenz) (mit % Inzidenz): Übelkeit (35,7 %), Erbrechen (23,2 %), Verstopfung ( 23,1%), Schläfrigkeit (15,0%), Schwindel (13,1%), Kopfschmerzen und Schlaflosigkeit (10,2%).
Die bei der Anwendung von Fentanyl aus diesen klinischen Studien berichteten UAW, einschließlich der oben genannten Nebenwirkungen und der Erfahrungen nach der Markteinführung, sind in Tabelle A unten aufgeführt.
Die gezeigten Häufigkeitskategorien verwenden die folgende Konvention.
Sehr häufig (≥1 / 10),
Häufig (≥1 / 100,
Gelegentlich (≥1 / 1.000 bis
Selten (≥1 / 10.000,
Sehr selten (
Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren klinischen Daten nicht abschätzbar)
Pädiatrische Fächer
Das Nebenwirkungsprofil bei Kindern und Jugendlichen, die mit Fentanyl transdermalen Pflastern behandelt werden, ist ähnlich wie bei Erwachsenen. Bei Kindern und Jugendlichen wurden keine anderen Risiken festgestellt als die, die bei der Anwendung von Opioiden zur Linderung von Schmerzen im Zusammenhang mit schweren Erkrankungen zu erwarten sind, und es scheint kein spezifisches Risiko für die pädiatrische Bevölkerung im Zusammenhang mit der Anwendung des Fentanyl transdermalen Pflasters in zu geben Kinder ab 2 Jahren, bei bestimmungsgemäßer Verwendung. Sehr häufige Nebenwirkungen, die in klinischen Studien mit Kindern und Jugendlichen berichtet wurden, waren Fieber, Erbrechen und Übelkeit.
Die Sicherheit von Fentanyl transdermalem Pflaster wurde bei 289 pädiatrischen Patienten untersucht (
Basierend auf den gepoolten klinischen Daten aus diesen 3 klinischen Studien mit pädiatrischen Probanden waren die häufigsten (d. h. ≥ 10 % Inzidenz) unerwünschten Arzneimittelwirkungen (UAW) (% Inzidenz): 16,3%), Verstopfung (13,5%), Durchfall (12,8%) und Juckreiz (12,8%). Tabelle B zeigt alle UAW, die in den genannten klinischen Studien mit Fentanyl transdermalem Pflaster bei pädiatrischen Patienten berichtet wurden.
Den UAW in Tabelle B für die pädiatrische Population wurden Häufigkeitskategorien nach der gleichen Konvention wie in Tabelle A zugewiesen.
Wie bei anderen Opioid-Analgetika können sich bei wiederholter Anwendung des transdermalen Fentanyl-Pflasters Toleranz, körperliche Abhängigkeit und psychische Abhängigkeit entwickeln (siehe Abschnitt 4.4).
Opioid-Entzugserscheinungen (wie Übelkeit, Erbrechen, Durchfall, Angstzustände, Schüttelfrost) sind bei einigen Patienten nach Umstellung von ihrem vorherigen Opioid-Analgetikum auf Fentanyl transdermales Pflaster oder bei abruptem Therapieabbruch möglich (siehe Abschnitt 4.2).
Es liegen Berichte über Neugeborene mit Entzugssyndrom vor, wenn Mütter während der Schwangerschaft Fentanyl transdermales Pflaster angewendet haben (siehe Abschnitt 4.6).
Meldung von vermuteten Nebenwirkungen.
Die Meldung von vermuteten Nebenwirkungen, die nach der Zulassung des Arzneimittels auftreten, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht. Angehörige von Gesundheitsberufen werden gebeten, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem zu melden. "Adresse www. agenziafarmaco.gov.it/it/responsabili.
04.9 Überdosierung -
Symptome
Die Manifestationen einer Überdosierung von Fentanyl sind eine Erweiterung seiner pharmakologischen Wirkungen, wobei die schwerwiegendste Wirkung eine Atemdepression ist.
Behandlung
Zur Behandlung einer Atemdepression sollten sofortige Gegenmaßnahmen ergriffen werden, einschließlich der Entfernung des Pflasters und der körperlichen oder verbalen Stimulation des Patienten. Diesen Wirkungen kann die Verabreichung eines spezifischen Opiatantagonisten wie Naloxon folgen.
Eine durch eine Überdosierung verursachte Atemdepression kann über die Wirkung des Opioid-Antagonisten hinaus andauern.
Das Intervall zwischen den Dosen des intravenösen Antagonisten muss wegen der möglichen Renarkotisierung nach Entfernen des Pflasters sorgfältig abgewogen werden; es kann notwendig sein, Naloxon in wiederholten Dosen oder als Dauerinfusion zu verabreichen.
Das Aufheben der narkotischen Wirkung kann zu einer Verschlimmerung der Schmerzen und zur Freisetzung von Katecholaminen führen.
Wenn die klinische Situation dies rechtfertigt, muss eine Durchgängigkeit der Atemwege hergestellt und aufrechterhalten werden, ggf. über den oropharyngealen Weg oder mit einer Endotrachealkanüle, und es muss Sauerstoff verabreicht und gegebenenfalls die Atmung unterstützt oder kontrolliert werden Körpertemperatur und eine angemessene Flüssigkeitszufuhr aufrechterhalten werden.
Sollte eine schwere oder anhaltende Hypotonie auftreten, sollte die Möglichkeit einer Hypovolämie in Betracht gezogen und der Zustand mit ausreichend parenteraler Flüssigkeit behandelt werden.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN -
05.1 "Pharmakodynamische Eigenschaften -
Pharmakotherapeutische Gruppe: Opiate; Phenylpiperidin-Derivate
ATC-Code: N02AB03
Fentanyl ist ein Opioid-Analgetikum mit hoher Affinität zu m-Opiat-Rezeptoren.
Pädiatrische Patienten
Die Sicherheit von transdermalem Fentanyl wurde in drei offenen Studien mit 289 pädiatrischen Patienten mit chronischen Schmerzen im Alter von 2 bis 18 Jahren, davon 66 Kinder im Alter von 2 bis 6 Jahren, untersucht. In diesen Studien wurde oral verabreichtes Morphin in Dosen von 30 mg bis 44 mg pro Tag durch ein Pflaster mit einer Freisetzungsrate von 12 µg/h ersetzt.
Anfangsdosen von 25 µg/h oder höher wurden bei 181 Patienten angewendet, die zuvor eine tägliche Opioidtherapie von mindestens 45 mg oraler Morphindosis erhielten.
05.2 "Pharmakokinetische Eigenschaften -
Erwachsene
Fentanyl Zentiva transdermales Pflaster bietet eine kontinuierliche systemische Freisetzung von Fentanyl über einen Verabreichungszeitraum von mehr als 72 Stunden. Fentanyl wird relativ konstant freigesetzt. Der Konzentrationsgradient zwischen der Matrix und der niedrigsten Konzentration in der Haut bestimmt die Freisetzung des Wirkstoffs.
Nach der ersten Anwendung von Fentanyl Zentiva transdermalem Pflaster steigen die Serumkonzentrationen von Fentanyl allmählich an, gleichen sich in der Regel zwischen 12 und 24 Stunden ein und bleiben für die restlichen 72 Stunden der Anwendung relativ konstant. Die erreichten Fentanyl-Serumkonzentrationen sind proportional zur Größe des Fentanyl-Pflasters. Mit der zweiten 72-stündigen Anwendung wird eine Steady-State-Serumkonzentration erreicht, die bei nachfolgenden Anwendungen eines gleich großen Pflasters erhalten bleibt.
Ein pharmakokinetisches Modell hat ergeben, dass die Fentanyl-Serumkonzentrationen um 14 % (Bereich 0-26 %) ansteigen können, wenn ein neues Pflaster nach 24 Stunden statt nach der empfohlenen 72-stündigen Anwendung aufgetragen wird.
Verteilung
Fentanyl ist zu etwa 84 % an Plasmaproteine gebunden.
Biotransformation
Fentanyl hat eine hohe Clearance und wird hauptsächlich in der Leber durch CYP3A4 schnell und umfassend metabolisiert. Der Hauptmetabolit, Norfentanyl, ist nicht aktiv. Die Haut scheint nicht transdermal verabreichtes Fentanyl zu metabolisieren. Dies wurde in Keratinozytenzellen festgestellt klinische Studien, in denen 92 % der vom System freigesetzten Dosis unverändertes Fentanyl war, das im systemischen Kreislauf gefunden wurde.
Beseitigung
Nach Entfernung von Fentanyl Zentiva transdermalem Pflaster, die Serumkonzentrationen von Fentanyl nehmen allmählich ab und nehmen nach einer 24-stündigen Anwendung in etwa 17 Stunden (Bereich 13-22) um etwa 50 % ab. Nach einer 72-stündigen Anwendung betrug die mittlere Halbwertszeit 20-27 Std. Eine kontinuierliche transdermale Resorption von Fentanyl führt zu einem langsameren Verschwinden des Arzneimittels aus dem Serum als nach intravenöser Infusion, wo die "scheinbare Halbwertszeit etwa 7" beträgt Stunden (Bereich 3-12 Stunden). Fentanyl wird hauptsächlich in der Leber metabolisiert. Innerhalb von 72 Stunden nach intravenöser Gabe von Fentanyl werden ungefähr 75 % der Fentanyl-Dosis mit dem Urin ausgeschieden, meistens in Form von Metaboliten, mit weniger als 10 % in Form des unveränderten Wirkstoffs. Ungefähr 9 % der Dosis werden im Stuhl gefunden, hauptsächlich als Metaboliten. Die Mittelwerte des ungebundenen Anteils von Fentanyl im Plasma werden auf 13 bis 21 % geschätzt.
Besondere Bevölkerungsgruppen
Senioren
Daten aus intravenösen Studien mit Fentanyl deuten darauf hin, dass ältere Patienten eine verringerte Clearance und eine verlängerte Halbwertszeit aufweisen und möglicherweise empfindlicher auf das Arzneimittel reagieren als jüngere Patienten unterscheiden sich nicht signifikant von denen gesunder junger Probanden, obwohl die Spitzenkonzentrationen im Serum tendenziell niedriger waren und die mittleren Halbwertswerte auf etwa 34 Stunden verlängert wurden. Ältere Patienten sollten sorgfältig auf Anzeichen einer Fentanyl-Toxizität beobachtet und die Dosis gegebenenfalls reduziert werden (siehe Abschnitt 4.2).
Pädiatrische Patienten
Die körpergewichtskorrigierte Clearance (l/h/kg) bei pädiatrischen Patienten scheint bei Kindern zwischen 2 und 5 Jahren um 82 % und bei Kindern zwischen 6 und 10 Jahren um 25 % höher zu sein -16 Jahre alt, die wahrscheinlich die gleiche Clearance wie Erwachsene haben Dieses Ergebnis wurde unter Berücksichtigung der empfohlenen Dosis ermittelt, die für pädiatrische Patienten bestimmt wurde.
Leberfunktionsstörung
In einer Studie mit Patienten mit Leberzirrhose wurde die Pharmakokinetik einer einmaligen Anwendung von 50 Mikrogramm/h Fentanyl transdermalem Pflaster untersucht. Obwohl sich tmax und t1 / 2 nicht änderten, erhöhten sich die mittleren Plasma-AUC-Werte bei diesen Patienten um etwa 35 % bzw. 73 %. Patienten mit eingeschränkter Leberfunktion sollten sorgfältig auf Toxizitätssymptome und gegebenenfalls eine reduzierte Fentanyl-Pflasterdosis überwacht werden (siehe Abschnitt 4.4).
Nierenfunktionsstörung
Daten aus Studien mit intravenös verabreichtem Fentanyl bei Nierentransplantationspatienten deuten darauf hin, dass die Fentanyl-Clearance bei dieser Patientenpopulation verringert sein kann.Wenn Patienten mit eingeschränkter Nierenfunktion Fentanyl transdermales Pflaster erhalten, sollten sie sorgfältig auf Anzeichen einer Fentanyl-Toxizität beobachtet und die Dosis gegebenenfalls reduziert werden (siehe Abschnitt 4.4).
05.3 Präklinische Daten zur Sicherheit -
In-vitro-Studien haben wie andere Opioid-Analgetika mutagene Wirkungen in kultivierten Säugerzellen nur bei zytotoxischen und metabolisch aktivierten Konzentrationen gezeigt. Fentanyl zeigt keine Hinweise auf Mutagenität, wenn es in In-vivo-Studien an Nagetieren und bakteriellen Methoden untersucht wird.
In einer zweijährigen Kanzerogenitätsstudie an Ratten war Fentanyl bei einer subkutanen Dosis von bis zu 33 µg/kg/Tag bei Männern bzw. 100 µg/kg/Tag bei Frauen nicht mit einem Anstieg der Tumorinzidenz verbunden (AUC0-24 h) war in diesen Studien die maximal tolerierte Plasmakonzentration bei Ratten.
Fentail wurde auf Auswirkungen auf die fetale Entwicklung bei Ratten und Kaninchen untersucht. Einige Untersuchungen an weiblichen Ratten zeigten eine verminderte Fertilität sowie embryonale Mortalität und vorübergehende Entwicklungsverzögerungen.
Diese Ergebnisse standen im Zusammenhang mit der maternalen Toxizität und nicht mit einer direkten Wirkung des Arzneimittels auf die Embryonalentwicklung. Diese Veränderungen wurden bei Plasmakonzentrationen im Steady-State beobachtet, die (Css, Ratte/Css, Mensch = 1,1) der in der Klinik nach Anwendung eines 100 µg/h-Pflasters beobachteten äquivalenten waren. Es wurden keine Effekte beobachtet Beim Menschen wurde eine Plasmakonzentration des 6,6-fachen der Steady-State-Plasmakonzentration von Fentanyl erreicht.Das tägliche Expositionsverhältnis (AUC4-24, Kaninchen/Mensch AUC 0-24 = 1,1) entsprach denen, die in der Klinik nach Anwendung von 100 . beobachtet wurden mcg / h des Patches. Es gibt keine Hinweise auf teratogene Wirkungen.
06.0 PHARMAZEUTISCHE INFORMATIONEN -
06.1 Hilfsstoffe -
Klebeschicht:
Polyacryl-Klebeschicht
Verstärkungsfolie:
Polypropylenfolie, blaue Druckfarbe
Trennmembran:
Polyethylenterephthalatplatte (silikonisiert)
06.2 Inkompatibilität "-
Nicht relevant
06.3 Gültigkeitsdauer "-
36 Monate
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung -
Nicht über 30 °C lagern.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks -
Jedes transdermale Pflaster ist einzeln in einem Beutel verpackt. Die laminierte Platte besteht aus den folgenden Schichten (von außen nach innen): beschichtetes Papier, Platte aus Polyethylen niedriger Dichte, Aluminiumfolie, Surlyn (Copolymer aus thermoplastischer Ethylen-Methacrylsäure).
Fentanyl Zentiva 25 mcg / h transdermales Pflaster
Fentanyl Zentiva 50 mcg / h transdermales Pflaster
Fentanyl Zentiva 75 mcg / h transdermales Pflaster
Fentanyl Zentiva 100 mcg / h transdermales Pflaster
Packung mit 3, 5, 10, 20 transdermalen Pflastern
Packung mit 7 transdermalen Pflastern
Packung mit 14 transdermalen Pflastern
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
06.6 Gebrauchs- und Handhabungshinweise -
Anweisungen zur Anwendung des Pflasters finden Sie in Abschnitt 4.2. Für andere Applikationsstellen liegen keine Daten zur Sicherheit und Pharmakokinetik vor.
Nach dem Entfernen sollte das gebrauchte Pflaster mit der Klebeseite nach innen in der Mitte gefaltet werden, damit die Klebeschicht nicht freiliegt, in den Originalbeutel gelegt und sicher und für Kinder unzugänglich entsorgt werden.
Waschen Sie Ihre Hände erst nach dem Anbringen oder Entfernen des Pflasters mit Wasser.
07.0 INHABER DER "MARKETING GENEHMIGUNG" -
Zentiva Italia S.r.l.
Viale Bodio 37 / b
20158 Mailand
08.0 NUMMER DER VERMARKTUNGSBERECHTIGUNG -
Fentanyl Zentiva 25 mcg / h transdermales Pflaster
3 transdermale AIC-Pflaster k. 037609017 / M
5 transdermale AIC-Pflaster k. 037609029 / M
10 transdermale AIC-Pflaster k. 037609031 / M
20 transdermale AIC-Pflaster n. 037609043 / M
Fentanyl Zentiva 50 mcg / h transdermales Pflaster
3 transdermale AIC-Pflaster k. 037609056 / M
5 transdermale AIC-Pflaster k. 037609068 / M
10 transdermale AIC-Pflaster k. 037609070 / M
20 transdermale AIC-Pflaster n. 037609082 / M
Fentanyl Zentiva 75 mcg / h transdermales Pflaster
3 transdermale AIC-Pflaster k. 037609094 / M
5 transdermale AIC-Pflaster k. 037609106 / M
10 transdermale AIC-Pflaster k. 037609118 / M
20 transdermale AIC-Pflaster n. 037609120 / M
Fentanyl Zentiva 100 mcg / h transdermales Pflaster
3 transdermale AIC-Pflaster k. 037609132 / M
5 transdermale AIC-Pflaster k. 037609144 / M
10 transdermale AIC-Pflaster k. 037609157 / M
20 transdermale AIC-Pflaster n. 037609169 / M
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG -
Datum der Erstzulassung: 07.04.2007
Datum der letzten Verlängerung: 17.05.2011
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs -
Dezember 2013
11.0 BEI FUNKDRUCK VOLLSTÄNDIGE DATEN ZUR INTERNEN STRAHLENDOSIMETRIE -
12.0 FÜR FUNKDROGEN, WEITERE DETAILLIERTE ANWEISUNGEN ZUR BEISPIELHAFTEN ZUBEREITUNG UND QUALITÄTSKONTROLLE -