Wirkstoffe: Olmesartanmedoxomil, Hydrochlorothiazid
OLPREZIDE 20 mg / 12,5 mg Filmtabletten
OLPREZIDE 20 mg / 25 mg Filmtabletten
Olprezide Packungsbeilagen sind für Packungsgrößen erhältlich: - OLPREZIDE 20 mg / 12,5 mg Filmtabletten, OLPREZIDE 20 mg / 25 mg Filmtabletten
- OLPREZIDE 40 mg / 12,5 mg Filmtabletten, OLPREZIDE 40 mg / 25 mg Filmtabletten
Warum wird Olprezid verwendet? Wofür ist das?
OLPREZIDE enthält zwei Substanzen namens Olmesartanmedoxomil und Hydrochlorothiazid. Beide werden verwendet, um hohen Blutdruck (Hypertonie) zu kontrollieren.
- Olmesartanmedoxomil gehört zu einer Gruppe von Arzneimitteln, die als „Angiotensin-II-Rezeptor-Antagonisten“ bezeichnet werden. Es senkt den Blutdruck, indem es die Blutgefäße freisetzt.
- Hydrochlorothiazid gehört zu einer Gruppe von Substanzen, die als „Thiazid-Diuretika“ bezeichnet werden.
Sie erhalten OLPREZIDE, wenn OLPRESS (Olmesartanmedoxomil) allein Ihren Blutdruck nicht ausreichend kontrolliert. Bei gemeinsamer Anwendung helfen die beiden Wirkstoffe in Olprezide dabei, den Blutdruck stärker zu senken als bei alleiniger Anwendung. Wenn Sie bereits Arzneimittel zur Behandlung von Bluthochdruck einnehmen, kann Ihr Arzt Ihnen OLPREZIDE verschreiben, um eine weitere Senkung des Blutdrucks zu erreichen. Ihr Bluthochdruck kann mit Arzneimitteln wie OLPREZIDE Tabletten kontrolliert werden. Ihr Arzt hat Ihnen wahrscheinlich auch empfohlen, einige Änderungen an Ihrem Bluthochdruck vorzunehmen Ihr Lebensstil zur Senkung Ihres Blutdrucks (z. B. Gewichtsabnahme, Raucherentwöhnung, Reduzierung des Alkoholkonsums und Reduzierung der Salzaufnahme mit der Nahrung) Ihr Arzt hat Ihnen möglicherweise auch geraten, regelmäßig Sport zu treiben, wie zum Beispiel Gehen oder Schwimmen dass Sie diese Ratschläge Ihres Arztes befolgen.
Kontraindikationen Wenn Olprezid nicht angewendet werden sollte
OLPREZIDE® darf nicht eingenommen werden
- wenn Sie allergisch gegen Olmesartanmedoxomil oder Hydrochlorothiazid oder einen der sonstigen Bestandteile dieses Arzneimittels (aufgeführt in Abschnitt 6) oder gegen Hydrochlorothiazid (Sulfonamide) ähnliche Substanzen sind.
- wenn Sie im dritten Monat schwanger sind (es wird empfohlen, OLPREZIDE auch in den ersten Schwangerschaftsmonaten nicht einzunehmen – siehe Abschnitt „Schwangerschaft und Stillzeit“)
- wenn Sie schwere Nierenprobleme haben
- wenn Sie Diabetes oder eine eingeschränkte Nierenfunktion haben und mit einem blutdrucksenkenden Arzneimittel behandelt werden, das Aliskiren enthält.
- wenn Sie niedrige Kalium- oder Natriumspiegel oder hohe Calcium- oder Harnsäurespiegel (mit Symptomen von Gicht oder Nierensteinen) in Ihrem Blut haben, die sich nach der Behandlung nicht bessern
- wenn Sie schwere Leberprobleme oder eine Gelbfärbung der Haut und der Augen (Gelbsucht) oder Probleme mit dem Gallenfluss aus der Gallenblase (Gallenobstruktion, zum Beispiel Steine) haben.
Wenn Sie glauben, an einer der oben genannten Erkrankungen zu leiden, oder wenn Sie sich nicht sicher sind, nehmen Sie das Arzneimittel nicht ein. Wenden Sie sich an Ihren Arzt und befolgen Sie seinen Rat.
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Olprezide beachten?
Bitte sprechen Sie mit Ihrem Arzt, bevor Sie OLPREZIDE anwenden.
Konsultieren Sie vor der Einnahme dieses Arzneimittels Ihren Arzt, wenn Sie eines der folgenden Arzneimittel zur Behandlung von Bluthochdruck einnehmen:
- einen „ACE-Hemmer“ (z. B. Enalapril, Lisinopril, Ramipril), insbesondere wenn Sie Diabetes-bedingte Nierenprobleme haben
- Aliskiren
Ihr Arzt wird möglicherweise in regelmäßigen Abständen Ihre Nierenfunktion, Ihren Blutdruck und die Menge an Elektrolyten (wie Kalium) in Ihrem Blut überprüfen.
Siehe auch Informationen unter der Überschrift „Olprezid darf nicht eingenommen werden“
Konsultieren Sie vor der Einnahme dieses Arzneimittels Ihren Arzt, wenn Sie eines der folgenden gesundheitlichen Probleme haben:
- Leichte oder mittelschwere Nierenprobleme oder wenn Sie kürzlich eine Nierentransplantation hatten.
- Erkrankungen der Leber.
- Herzinsuffizienz oder Probleme mit Ihren Herzklappen oder Ihrem Herzmuskel.
- Erbrechen oder Durchfall, der schwer ist oder mehrere Tage anhält.
- Behandlung mit hochdosierten Diuretika oder wenn Sie eine salzarme Diät einhalten.
- Probleme mit den Nebennieren (zum Beispiel primärer Aldosteronismus).
- Diabetes.
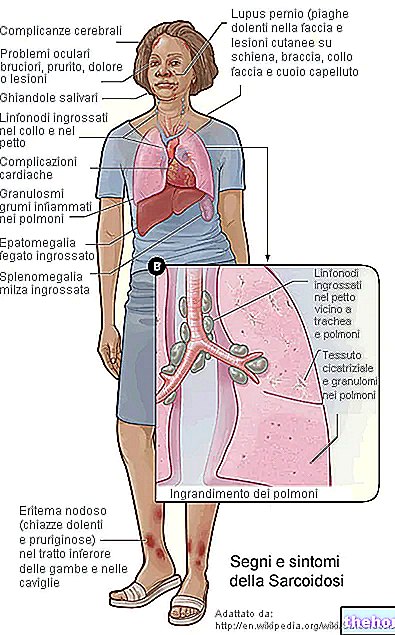
- Lupus erythematodes (eine Autoimmunerkrankung).
- Allergien oder Asthma.
Ihr Arzt möchte Sie möglicherweise häufiger sehen und einige Tests anordnen, wenn Sie eine der vorherigen Erkrankungen haben.
Informieren Sie Ihren Arzt, wenn bei Ihnen schwerer und anhaltender Durchfall mit erheblichem Gewichtsverlust auftritt. Ihr Arzt wird Ihre Symptome beurteilen und entscheiden, ob diese blutdrucksenkende Behandlung fortgesetzt werden soll.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Olprezide® verändern?
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie eines der folgenden Arzneimittel anwenden, kürzlich angewendet haben oder beabsichtigen, eines der folgenden Arzneimittel anzuwenden.
Informieren Sie Ihren Arzt oder Apotheker insbesondere über die folgenden Arzneimittel:
- Andere blutdrucksenkende Arzneimittel (Antihypertensiva) können die Wirkung von Olprezide verstärken. Ihr Arzt muss möglicherweise Ihre Dosis anpassen und/oder andere Vorsichtsmaßnahmen treffen. Wenn Sie einen ACE-Hemmer oder Aliskiren einnehmen (siehe auch Informationen unter Olprezid "und" Warnhinweise und Vorsichtsmaßnahmen "
- Arzneimittel, die bei gleichzeitiger Anwendung mit OLPREZIDE Veränderungen des Kaliumspiegels im Blut verursachen können. Diese beinhalten:
- Kaliumpräparate (wie kaliumhaltige Salzersatzstoffe)
- Diuretika
- Heparin (zur Blutverdünnung)
- Abführmittel
- Steroide
- adrenocorticotropes Hormon (ACTH)
- Carbenoxolon (ein Arzneimittel zur Behandlung von Mund- und Magengeschwüren)
- Penicillin-G-Natrium (auch Benzylpenicillin-Natrium genannt, ein Antibiotikum)
- einige Schmerzmittel wie Aspirin oder Salicylate
- Lithium (ein Arzneimittel zur Behandlung von Stimmungsschwankungen und einigen Arten von Depressionen), das zusammen mit Olprezide angewendet wird, kann die Toxizität von Lithium erhöhen.Wenn Sie Lithium einnehmen müssen, wird Ihr Arzt Ihren Lithium-Blutspiegel messen.
- Nichtsteroidale Antirheumatika (NSAIDs, Arzneimittel zur Linderung von Schmerzen, Schwellungen und anderen Entzündungssymptomen, einschließlich „Arthritis“), die zusammen mit OLPREZIDE angewendet werden, können das Risiko eines Nierenversagens erhöhen. Die Wirksamkeit von OLPREZIDE kann durch NSAR verringert werden.
- Schlaftabletten, Beruhigungsmittel und Antidepressiva, die zusammen mit Olprezide angewendet werden, können einen „plötzlichen Blutdruckabfall beim Aufstehen“ verursachen.
- Einige Arzneimittel wie Baclofen und Tubocurarin zur Entspannung der Muskeln
- Amifostin und einige andere Arzneimittel zur Behandlung von Krebs, wie Cyclophosphamid oder Methotrexat
- Colestyramin und Colestipol, Arzneimittel zur Senkung des Blutfettspiegels
- Colesevelamhydrochlorid, ein Arzneimittel, das den Cholesterinspiegel im Blut senkt, was die Wirkung von Olprezide abschwächen kann.Ihr Arzt wird Ihnen möglicherweise empfehlen, Olprezide mindestens 4 Stunden vor Colesevelamhydrochlorid einzunehmen
- Anticholinergika wie Atropin und Biperiden
- Arzneimittel wie Thioridazin, Chlorpromazin, Levomepromazin, Trifluoperazin, Ciamemazin, Sulpirid, Amisulprid, Pimozid, Sultoprid, Tiaprid, Droperidol oder Haloperidol zur Behandlung einiger psychiatrischer Erkrankungen
- Bestimmte Arzneimittel wie Chinidin, Hydrochinidin, Disopyramid, Amiodaron, Sotalol oder Digitalis zur Behandlung von Herzerkrankungen
- Arzneimittel wie Mizolastin, Pentamidin, Terfenadin, Dofetilid, Ibutilid oder Erythromycin injiziert, die den Herzrhythmus verändern können
- Orale Antidiabetika wie Metformin oder Insulin zur Senkung des Blutzuckerspiegels
- Betablocker und Diazoxid, Arzneimittel zur Behandlung von Bluthochdruck bzw. niedrigem Blutzucker, da OLPREZIDE ihre hyperglykämische Wirkung verstärken kann
- Methyldopa, ein Arzneimittel zur Behandlung von Bluthochdruck
- Arzneimittel wie Noradrenalin, die verwendet werden, um den Blutdruck zu erhöhen und die Herzfrequenz zu verlangsamen
- Difemanil, zur Behandlung einer langsamen Herzfrequenz oder zur Verringerung des Schwitzens
- Arzneimittel wie Probenecid, Sulfinpyrazon und Allopurinol zur Behandlung von Gicht
- Calcium-Ergänzungen
- Amantadin, ein antivirales Arzneimittel
- Ciclosporin, ein Arzneimittel zur Verhinderung der Abstoßung transplantierter Organe
- Bestimmte Antibiotika namens Tetracycline oder Sparfloxacin
- Amphotericin, ein Arzneimittel zur Behandlung von Pilzerkrankungen
- Einige Antazida, die zur Behandlung von Magensäure verwendet werden, wie Aluminium- und Magnesiumhydroxid, da sie die Wirksamkeit von OLPREZIDE geringfügig verringern können.
- Cisaprid, verwendet, um die Bewegung der Nahrung im Magen und Darm zu erhöhen
- Halofanthin, verwendet für Malaria
Einnahme von OLPREZIDE zusammen mit Nahrungsmitteln und Getränken
OLPREZIDE kann auf vollen oder nüchternen Magen eingenommen werden.
Achten Sie darauf, dass Sie während der Einnahme von Olprezide Alkohol trinken, da manche Personen sich schwach oder schwindelig fühlen können. Wenn dies bei Ihnen der Fall ist, trinken Sie keinen anderen Alkohol, einschließlich Wein, Bier oder aromatisierte alkoholische Getränke.
Warnungen Es ist wichtig zu wissen, dass:
Olprezid kann einen erhöhten Fett- und Harnsäurespiegel im Blut verursachen (wodurch Gicht - schmerzhafte Schwellung der Gelenke verursacht wird.) Ihr Arzt wird wahrscheinlich regelmäßige Blutuntersuchungen durchführen lassen, um diese Erkrankungen zu beurteilen.
Der Spiegel bestimmter Substanzen, sogenannter Elektrolyte, im Blut kann sich ändern. Ihr Arzt wird wahrscheinlich regelmäßige Bluttests durchführen lassen, um diese Bedingungen zu beurteilen. Anzeichen von Elektrolytveränderungen sind: Durst, Mundtrockenheit, Muskelschmerzen oder -krämpfe, Muskelermüdung, niedriger Blutdruck (Hypotonie), Schwächegefühl, Trägheit, Müdigkeit, Schläfrigkeit oder mangelnde Ruhe, Übelkeit, Erbrechen, verminderter Harndrang, schnelles Pulsschlag. Informieren Sie Ihren Arzt, wenn diese Symptome auftreten.
Wie bei jedem blutdrucksenkenden Arzneimittel kann eine übermäßige Blutdrucksenkung bei Patienten mit Durchblutungsstörungen des Herzens oder des Gehirns zu einem Herzinfarkt oder Schlaganfall führen. Ihr Arzt wird dann Ihren Blutdruck sorgfältig überprüfen.
Wenn bei Ihnen Nebenschilddrüsenfunktionstests durchgeführt werden müssen, müssen Sie die Einnahme von Olprezide absetzen, bevor Sie diese Tests durchführen.
Wenn Sie Sport treiben, kann dieses Arzneimittel die Ergebnisse eines Anti-Doping-Tests verändern und positiv werden.
Sie sollten Ihren Arzt informieren, wenn Sie glauben, schwanger zu sein oder schwanger zu werden. OLPREZIDE wird in der frühen Schwangerschaft nicht empfohlen und darf nach dem dritten Schwangerschaftsmonat nicht mehr eingenommen werden, da es bei Anwendung in diesem Zeitraum dem Baby ernsthaft schaden kann (siehe Abschnitt „Schwangerschaft und Stillzeit“).
Kinder und Jugendliche
Olprezid wird für Kinder und Jugendliche unter 18 Jahren nicht empfohlen.
Patienten schwarzer Abstammung
Wie bei anderen ähnlichen Arzneimitteln kann die blutdrucksenkende Wirkung von OLPREZIDE bei Patienten mit schwarzer Hautfarbe etwas abgeschwächt sein.
Schwangerschaft und Stillzeit
Schwangerschaft
Sie sollten Ihren Arzt informieren, wenn Sie vermuten, schwanger zu sein oder die Möglichkeit besteht, schwanger zu werden. In der Regel wird Ihr Arzt Ihnen raten, die Einnahme von OLPREZIDE vor einer Schwangerschaft bzw. sobald Sie wissen, dass Sie schwanger sind, abzusetzen und wird Ihnen raten, anstelle von OLPREZIDE ein anderes Arzneimittel einzunehmen. OLPREZIDE wird während der Schwangerschaft nicht empfohlen und darf nicht eingenommen werden nach dem dritten Schwangerschaftsmonat, da es dem Baby ernsthaft schaden kann, wenn es nach dem dritten Schwangerschaftsmonat eingenommen wird.
Fütterungszeit
Informieren Sie Ihren Arzt, wenn Sie stillen oder mit dem Stillen beginnen möchten.OLPREZIDE wird während der Stillzeit nicht empfohlen und Ihr Arzt kann eine andere Behandlung für Sie wählen, wenn Sie stillen möchten.
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Einnahme dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Während einer Behandlung mit Bluthochdruck können Sie sich schläfrig oder schwindelig fühlen. Führen Sie in diesem Fall kein Fahrzeug und bedienen Sie keine Maschinen, bis die Symptome abgeklungen sind. Fragen Sie Ihren Arzt um Rat.
OLPREZIDE enthält Lactose
Dieses Arzneimittel enthält Lactose (eine Zuckerart). Bitte nehmen Sie dieses Arzneimittel erst nach Rücksprache mit Ihrem Arzt ein, wenn Ihnen bekannt ist, dass Sie unter einer Zuckerunverträglichkeit leiden.
Dosis, Methode und Zeitpunkt der Anwendung Wie ist Olprezide anzuwenden: Dosierung
Nehmen Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt ein. Wenn Sie sich nicht sicher sind, wenden Sie sich an Ihren Arzt oder Apotheker.
Die empfohlene Dosis beträgt eine Tablette Olprezide 20 mg/12,5 mg pro Tag. Wenn Ihr Blutdruck jedoch nicht kontrolliert wird, kann Ihr Arzt entscheiden, Ihr Rezept auf eine Tablette Olprezide 20 mg / 25 mg pro Tag zu ändern.
Schlucken Sie die Tabletten mit etwas Wasser. Nehmen Sie Ihre Tagesdosis möglichst jeden Tag zur gleichen Zeit ein, zum Beispiel zum Frühstück. Es ist wichtig, dass Sie OLPREZIDE so lange einnehmen, bis Ihr Arzt Ihnen sagt, dass Sie die Einnahme beenden sollen.
Wenn Sie die Einnahme von OLPREZIDE® vergessen haben
Wenn Sie die Einnahme einer Dosis vergessen haben, nehmen Sie am nächsten Tag einfach Ihre normale Dosis ein. Nehmen Sie nicht die doppelte Dosis ein, wenn Sie die vorherige Einnahme vergessen haben.
Wenn Sie die Einnahme von OLPREZIDE® abbrechen
Es ist wichtig, dass Sie OLPREZIDE weiterhin einnehmen, es sei denn, Ihr Arzt sagt Ihnen, dass Sie die Einnahme beenden sollen.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
Überdosierung Was ist zu tun, wenn Sie zu viel Olprezide eingenommen haben?
Wenn Sie eine größere Menge von OLPREZIDE eingenommen haben, als Sie sollten
Wenn Sie mehr Tabletten eingenommen haben, als Sie sollten, oder wenn ein Kind versehentlich Tabletten verschluckt hat, gehen Sie sofort zu Ihrem Arzt oder der nächstgelegenen Notaufnahme und nehmen Sie die Arzneimittelpackung mit.
Nebenwirkungen Was sind die Nebenwirkungen von Olprezide
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Die folgenden zwei Nebenwirkungen können jedoch schwerwiegend sein:
- In seltenen Fällen können allergische Reaktionen, die den ganzen Körper betreffen können, mit Schwellungen von Gesicht, Mund und/oder Kehlkopf (Lage der Stimmbänder), verbunden mit Juckreiz und Hautausschlag auftreten.
- Olprezid kann bei anfälligen Personen oder als Folge einer allergischen Reaktion zu einer übermäßigen Senkung des Blutdrucks führen. Schwindel oder Ohnmacht sind nicht sehr häufig. Wenn dies geschieht, beenden Sie die Einnahme von Olprezid, wenden Sie sich sofort an Ihren Arzt und legen Sie sich hin.
OLPREZIDE ist eine Kombination aus zwei Wirkstoffen und in den folgenden Informationen werden zuerst die anderen bisher bei der OLPREZIDE-Kombination berichteten Nebenwirkungen (zusätzlich zu den bereits oben genannten) und dann die für die einzelnen Wirkstoffe bekannten Nebenwirkungen erwähnt.
Andere bisher bekannte mögliche Nebenwirkungen von OLPREZIDE:
Wenn diese Nebenwirkungen auftreten, sind sie oft mild und die Behandlung mit Olprezid sollte nicht abgebrochen werden.
Häufige Nebenwirkungen (kann bis zu 1 von 10 Behandelten betreffen):
Schwindel, Schwäche, Kopfschmerzen, Müdigkeit, Brustschmerzen, geschwollene Knöchel, Füße, Beine, Hände oder Arme.
Gelegentliche Nebenwirkungen (kann bis zu 1 von 100 Behandelten betreffen):
Wahrnehmung von Herzschlag (Palpitationen), Hautausschlag, Ekzeme, Schwindel, Husten, Verdauungsstörungen, Bauchschmerzen, Übelkeit, Erbrechen, Durchfall, Muskelschmerzen und Muskelkrämpfe, Gelenkschmerzen, Schmerzen in Armen und Beinen, Rückenschmerzen, Erektionsschwierigkeiten bei Männern, Blut im Urin.
Gelegentlich wurden auch einige Veränderungen bei Labortests beobachtet, darunter: erhöhte Blutfettwerte, erhöhte Blutharnstoff- oder Harnsäurespiegel, erhöhtes Kreatinin, erhöhte oder erniedrigte Kaliumspiegel im Blut, Anstieg des Calciumspiegels im Blut, Anstieg des Blutzuckerspiegels, Erhöhung der Leberfunktion Indizes. Ihr Arzt wird dies anhand Ihrer Blutuntersuchungen erfahren und Ihnen sagen, ob Sie etwas unternehmen müssen.
Seltene Nebenwirkungen (kann bis zu 1 von 1000 Behandelten betreffen):
Unwohlsein, Bewusstseinsstörungen, Hautblasen (Quaddeln), akutes Nierenversagen.
In seltenen Fällen wurden auch einige Veränderungen bei Labortests beobachtet, darunter: erhöhter Harnstoffstickstoff im Blut, erniedrigte Hämoglobin- und Hämatokritwerte Ihr Arzt wird dies anhand Ihrer Blutuntersuchungen erfahren und Ihnen mitteilen, ob etwas getan werden sollte.
Zusätzliche Nebenwirkungen, die bei Anwendung von Olmesartanmedoxomil oder Hydrochlorothiazid allein, jedoch nicht mit OLPREZIDE oder häufiger berichtet wurden:
Olmesartanmedoxomil:
Häufige Nebenwirkungen (kann bis zu 1 von 10 Behandelten betreffen):
Bronchitis, Husten, nasale Hypersekretion, trockener Hals, Bauchschmerzen, Verdauungsstörungen, Durchfall, Übelkeit, Gastroenteritis, Gelenk- oder Knochenschmerzen, Rückenschmerzen, Blut im Urin, Harnwegsinfektionen, grippeähnliche Symptome, Schmerzen.
Einige Laboranomalien wurden ebenfalls häufig beobachtet, einschließlich: erhöhte Blutfettwerte, erhöhte Blutharnstoff- oder Harnsäurewerte, erhöhte Leber- und Muskelfunktionsindizes.
Gelegentliche Nebenwirkungen (kann bis zu 1 von 100 Behandelten betreffen):
Schnelle allergische Reaktionen, die den ganzen Körper betreffen können und die Atembeschwerden oder einen schnellen Blutdruckabfall verursachen können, der zu Ohnmacht (anaphylaktische Reaktionen), Gesichtsschwellung, Angina pectoris (Schmerzen oder unangenehmes Gefühl in der Brust, bekannt als Angina pectoris) führen kann, Unwohlsein, allergische Hautreaktion, Juckreiz, Hautausschlag (Hautausschlag), Hautblasen (Quaddeln).
Gelegentlich wurden auch einige Veränderungen bei Labortests beobachtet, darunter: Verminderung der Anzahl bestimmter Blutzellen, die als Blutplättchen bezeichnet werden (Thrombozytopenie).
Seltene Nebenwirkungen (kann bis zu 1 von 1000 Behandelten betreffen):
Nierenfunktionsstörung, Schwäche.
In seltenen Fällen wurden auch einige Veränderungen bei Labortests beobachtet, einschließlich der folgenden: erhöhter Kaliumspiegel im Blut.
Hydrochlorothiazid:
Sehr häufige Nebenwirkungen (kann mehr als 1 von 10 Behandelten betreffen):
Veränderungen bei Labortests, die einschließen: erhöhte Fett- und Harnsäurespiegel im Blut.
Häufige Nebenwirkungen (kann bis zu 1 von 10 Behandelten betreffen):
Verwirrtheit, Bauchschmerzen, Magenbeschwerden, Blähungen, Durchfall, Übelkeit, Erbrechen, Verstopfung, Ausscheidung von Glukose mit dem Urin.
Es wurden auch einige Veränderungen bei Labortests beobachtet, darunter: Anstieg der Kreatinin-, Harnstoff-, Kalzium- und Glukosespiegel im Blut, Abnahme der Chlorid-, Kalium-, Magnesium- und Natriumspiegel im Blut. Erhöhte Serumamylase (Hyperamylasämie).
Gelegentliche Nebenwirkungen (kann bis zu 1 von 100 Behandelten betreffen):
Appetitlosigkeit oder -verlust, schwere Atembeschwerden, anaphylaktische Reaktionen der Haut (Überempfindlichkeitsreaktionen), Verschlechterung einer vorbestehenden Kurzsichtigkeit, Erythem, Hautreaktionen auf Licht, Juckreiz, violette Flecken oder Flecken auf der Haut aufgrund einer kleinen Blutung (Purpura), Haut Blasen (Quaddeln).
Seltene Nebenwirkungen (kann bis zu 1 von 1000 Behandelten betreffen):
Geschwollene und schmerzhafte Speicheldrüsen, verminderte Anzahl weißer Blutkörperchen, verminderte Thrombozytenzahl, Anämie, Knochenmarkschäden, Ruhelosigkeit, Depressionen, Schlafstörungen, Desinteresse (Apathie), Kribbeln und Taubheit, Krampfanfälle, Anblick gelber Gegenstände, verschwommenes Sehen , trockenes Auge, unregelmäßiger Herzschlag, Entzündung der Blutgefäße, Blutgerinnsel (Thrombose oder Embolie), Lungenentzündung, Flüssigkeitsansammlung in der Lunge, Entzündung der Bauchspeicheldrüse, Gelbsucht, Infektion der Gallenblase, Symptome von Lupus erythematodes wie Hautausschlag, Gelenkschmerzen und kalte Hände und Finger, allergische Hautreaktionen, Abschälen und Blasenbildung der Haut, nicht-infektiöse Nierenentzündung (interstitielle Nephritis), Fieber, Muskelschwäche (was manchmal zu motorischen Einschränkungen führt).
Sehr seltene Nebenwirkungen (kann bis zu 1 von 10.000 Behandelten betreffen):
Elektrolytveränderungen, die zu einer „abnormalen Verringerung des Chloridgehalts im Blut (hypochlorämische Alkalose) führen. Darmverschluss (paralytischer Ileus).
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker, einschließlich aller möglichen Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind. Sie können Nebenwirkungen auch direkt über das nationale Meldesystem unter www.agenziafarmaco.gov.it//responsible melden.Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
Ablauf und Aufbewahrung
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Verwenden Sie dieses Arzneimittel nicht nach dem auf der Packung und der Blisterpackung nach „EXP“ angegebenen Verfallsdatum. Das Ablaufdatum bezieht sich auf den letzten Tag des Monats.
Entsorgen Sie Arzneimittel nicht im Abwasser oder Haushaltsabfall.Fragen Sie Ihren Apotheker, wie Arzneimittel zu entsorgen sind, die Sie nicht mehr verwenden. Dies trägt zum Schutz der Umwelt bei.
Frist "> Weitere Informationen
Was OLPREZIDE enthält
- Die Wirkstoffe sind:
- OLPREZIDE 20 mg / 12,5 mg: Jede Filmtablette enthält 20 mg Olmesartanmedoxomil und 12,5 mg Hydrochlorothiazid.
- OLPREZIDE 20 mg / 25 mg: Jede Filmtablette enthält 20 mg Olmesartanmedoxomil und 25 mg Hydrochlorothiazid.
- Die sonstigen Bestandteile sind: Mikrokristalline Cellulose, Lactose-Monohydrat, niedrig substituierte Hyprolose, Hyprolose, Magnesiumstearat, Titandioxid (E171), Talkum, Hypromellose, Eisen(III)-oxid (E172).
Beschreibung wie OLPREZIDE aussieht und Inhalt der Packung
OLPREZIDE 20 mg / 12,5 mg rötlich-gelbe, runde, 8,5 mm Filmtabletten mit einseitiger Prägung C22
OLPREZIDE 20 mg / 25 mg rosafarbene, runde, 8,5 mm Filmtabletten mit der Prägung C24 auf einer Seite
OLPREZIDE ist in Packungen mit 14, 28, 30, 56, 84, 90, 98 und 10x28 Filmtabletten sowie in Packungen mit 10, 50 und 500 Filmtabletten mit perforierten Blisterpackungen zur Abgabe von Einzeldosen erhältlich.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu erhalten, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS -
OLPREZID-TABLETTEN MIT FILM . BESCHICHTET
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG -
Olprezid 20 mg / 12,5 mg Filmtabletten:
jede Filmtablette enthält 20 mg Olmesartanmedoxomil und 12,5 mg Hydrochlorothiazid
Olprezid 20 mg / 25 mg Filmtabletten:
jede Filmtablette enthält 20 mg Olmesartanmedoxomil und 25 mg Hydrochlorothiazid
Hilfsstoffe:
Olprezide 20 mg / 12,5 mg Filmtabletten: Jede Filmtablette enthält 110,7 mg Lactose-Monohydrat
Olprezide 20 mg / 25 mg Filmtabletten: Jede Filmtablette enthält 98,2 mg Lactose-Monohydrat
Die vollständige Liste der sonstigen Bestandteile finden Sie in Abschnitt 6.1
03.0 DARREICHUNGSFORM -
Filmtablette.
Olprezide 20 mg / 12,5 mg Filmtabletten: rötlich-gelbe, runde Filmtabletten mit der Prägung C22 auf einer Seite.
Olprezide 20 mg / 25 mg Filmtabletten: Rosafarbene, runde Filmtabletten mit der Prägung C24 auf einer Seite.
04.0 KLINISCHE INFORMATIONEN -
04.1 Anwendungsgebiete -
Behandlung der essentiellen arteriellen Hypertonie.
Olprezid, Fixkombination, ist angezeigt bei erwachsenen Patienten, deren Blutdruck durch Olmesartanmedoxomil allein nicht ausreichend kontrolliert wird.
04.2 Dosierung und Art der Anwendung -
Erwachsene
Olprezid ist bei Patienten angezeigt, deren Blutdruck durch eine Monotherapie mit 20 mg Olmesartanmedoxomil nicht ausreichend kontrolliert wird, und sollte nicht als Initialtherapie angewendet werden. Olprezid wird einmal täglich entweder auf nüchternen oder vollen Magen verabreicht.
Wenn klinisch angemessen, kann eine direkte Umstellung von 20 mg Olmesartanmedoxomil-Monotherapie auf die Fixkombination in Betracht gezogen werden, da die blutdrucksenkende Wirkung von Olmesartanmedoxomil etwa 8 Wochen nach Therapiebeginn maximal ist (siehe Abschnitt 5.1). Komponenten.
Die Kombination von 20 mg Olmesartanmedoxomil und 12,5 mg Hydrochlorothiazid kann bei Patienten angewendet werden, deren Blutdruck durch eine optimale Monotherapie mit 20 mg Olmesartanmedoxomil nicht ausreichend kontrolliert wird.
Die Kombination von 20 mg Olmesartanmedoxomil und 25 mg Hydrochlorothiazid kann bei Patienten angewendet werden, deren Blutdruck durch die Kombination von 20 mg Olmesartanmedoxomil und 12,5 mg Hydrochlorothiazid nicht ausreichend kontrolliert wird.
Senioren (65 plus Jahre)
Bei älteren Patienten wird die gleiche Dosierung wie die bei Erwachsenen angewendete Kombination empfohlen.
Veränderte Nierenfunktion
Bei der Anwendung von Olprezide bei Patienten mit leichter bis mittelschwerer Nierenfunktionsstörung (Kreatinin-Clearance zwischen 30 und 60 ml/min) wird empfohlen, die Nierenfunktion regelmäßig zu überwachen (siehe Abschnitt 4.4). Olprezid ist bei Patienten mit schwerer Nierenfunktionsstörung (Kreatinin-Clearance unter 30 ml/min) kontraindiziert (siehe Abschnitt 4.3).
Veränderte Leberfunktion
Olprezid sollte bei Patienten mit leichter bis mittelschwerer Leberfunktionsstörung mit Vorsicht angewendet werden (siehe Abschnitte 4.4, 5.2). Bei Patienten mit mittelschwerer Leberfunktionsstörung beträgt die empfohlene Anfangsdosis von Olmesartanmedoxomil 10 mg einmal täglich und die Höchstdosis sollte 20 mg einmal täglich nicht überschreiten. Bei Patienten mit eingeschränkter Leberfunktion, die Diuretika und/oder andere blutdrucksenkende Arzneimittel einnehmen, wird eine engmaschige Überwachung des Blutdrucks und der Nierenfunktion empfohlen. Es liegen keine Erfahrungen mit der Anwendung von Olmesartanmedoxomil bei Patienten mit schwerer Leberfunktionsstörung vor Olprezid sollte nicht bei Patienten mit schwerer Leberfunktionsstörung (siehe Abschnitte 4.3, 5.2), Cholestase und Gallenwegsobstruktion (siehe Abschnitt 4.3) angewendet werden.
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Olprezide bei Kindern und Jugendlichen unter 18 Jahren sind nicht erwiesen.Es liegen keine Daten vor.
Art der Verabreichung:
Die Tablette sollte mit ausreichend Flüssigkeit (zB einem Glas Wasser) geschluckt, nicht gekaut und jeden Tag zur gleichen Zeit eingenommen werden.
04.3 Kontraindikationen -
Überempfindlichkeit gegen die Wirkstoffe, einen der sonstigen Bestandteile (siehe Abschnitt 6.1) oder andere von Sulfonamid abgeleitete Substanzen (da Hydrochlorothiazid ein von Sulfonamid abgeleitetes Arzneimittel ist).
Schwere Nierenfunktionsstörung (Kreatinin-Clearance weniger als 30 ml / min).
Refraktäre Hypokaliämie, Hyperkalzämie, Hyponatriämie und symptomatische Hyperurikämie. Schwere Leberfunktionsstörung, Cholestase und obstruktive Gallenwegserkrankung. Zweites und drittes Schwangerschaftstrimester (siehe Abschnitte 4.4 und 4.6).
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung -
Intravaskulärer Volumenverlust:
Bei Patienten mit Hypovolämie und/oder Natriummangel durch hohe Diuretikadosen, reduzierte Natriumaufnahme mit der Nahrung, Durchfall oder Erbrechen kann insbesondere nach der ersten Dosis eine symptomatische Hypotonie auftreten. Diese Zustände müssen vor Beginn der Behandlung mit Olprezide korrigiert werden.
Andere Zustände im Zusammenhang mit der Stimulation des Renin-Angiotensin-Aldosteron-Systems: Bei Patienten, deren Gefäßtonus und Nierenfunktion hauptsächlich von der Aktivität des Renin-Angiotensin-Aldosteron-Systems abhängig sind (z. B. Patienten mit schwerer kongestiver Herzinsuffizienz oder betroffener Nierenerkrankung, einschließlich Nierenarterienstenose) wurde die Behandlung mit Arzneimitteln, die auf dieses System abzielen, mit akuter Hypotonie, Azotämie, Oligurie oder in seltenen Fällen akutem Nierenversagen in Verbindung gebracht.
Renovaskuläre Hypertonie:
Bei Patienten mit beidseitiger Stenose der Nierenarterie oder Stenose der afferenten Arterie zu einer einzigen funktionsfähigen Niere, die mit Arzneimitteln behandelt werden, die das Renin-Angiotensin-Aldosteron-System beeinflussen, besteht ein erhöhtes Risiko für Hypotonie und schweres Nierenversagen.
Veränderte Nierenfunktion und Nierentransplantation:
Olprezid darf nicht bei Patienten mit schwerer Nierenfunktionsstörung (Kreatinin-Clearance unter 30 ml/min) angewendet werden (siehe Abschnitt 4.3). Bei Patienten mit leichter bis mittelschwerer Nierenfunktionsstörung (Kreatinin-Clearance ≥ 30 ml/min und Serumkalium, Kreatinin und Harnsäure) sind keine Dosisanpassungen erforderlich. Thiaziddiuretika. Wenn eine fortschreitende Nierenfunktionsstörung erkennbar ist, ist eine sorgfältige Neubewertung der Therapie unter Berücksichtigung Absetzen des Diuretikums Es liegen keine Erfahrungen mit der Anwendung von Olprezide bei Patienten vor, die sich vor kurzem einer Nierentransplantation unterzogen haben.
Eingeschränkte Leberfunktion:
Derzeit liegen keine Erfahrungen mit Olmesartanmedoxomil bei Patienten mit schwerer Leberfunktionsstörung vor. Darüber hinaus können leichte Veränderungen des Wasser-Elektrolyt-Gleichgewichts während der Thiazidtherapie bei Patienten mit eingeschränkter Leberfunktion oder fortschreitender Lebererkrankung ein Leberkoma induzieren. Daher ist bei Patienten mit leichter bis mittelschwerer Leberfunktionsstörung Vorsicht geboten (siehe Abschnitt 4.2). Die Anwendung von Olprezide ist bei Patienten mit schwerer Leberfunktionsstörung, Cholestase oder Gallenwegsobstruktion kontraindiziert (siehe Abschnitte 4.3, 5.2).
Aorten- und Mitralklappenstenose, obstruktive hypertrophe Kardiopathie:
Wie bei anderen Vasodilatatoren ist bei Patienten mit Aorten- oder Mitralklappenstenose oder obstruktiver hypertropher Kardiomyopathie besondere Vorsicht geboten.
Primärer Aldosteronismus:
Patienten mit primärem Aldosteronismus sprechen im Allgemeinen nicht auf blutdrucksenkende Arzneimittel an, die durch eine Hemmung des Renin-Angiotensin-Systems wirken, daher wird die Anwendung von Olprezid bei diesen Patienten nicht empfohlen.
Stoffwechsel- und endokrine Wirkungen
Eine Thiazidtherapie kann die Glukosetoleranz beeinträchtigen. Bei Diabetikern können Dosisanpassungen von Insulin oder orale Hypoglykämien erforderlich sein (siehe Abschnitt 4.5) Während einer Thiazidtherapie kann sich ein latenter Diabetes mellitus manifestieren.
Erhöhte Cholesterin- und Triglyceridspiegel stellen eine bekannte Nebenwirkung im Zusammenhang mit einer Thiazid-Diuretika-Therapie dar. Bei einigen Patienten, die eine Thiazid-Therapie erhalten, kann es zu Hyperurikämie oder Gicht kommen.
Elektrolytstörungen
Wie bei allen Patienten unter Diuretikatherapie sollten in angemessenen Abständen regelmäßige Serumelektrolytmessungen durchgeführt werden.
Thiazide, einschließlich Hydrochlorothiazid, können ein Flüssigkeits- oder Elektrolytungleichgewicht (einschließlich Hypokaliämie, Hyponatriämie und hypochlorämische Alkalose) verursachen. Warnzeichen für ein Flüssigkeits- oder Elektrolyt-Ungleichgewicht sind Mundtrockenheit, Durst, Schwäche, Lethargie, Schläfrigkeit, Ruhelosigkeit, Muskelschmerzen oder -krämpfe, Muskelermüdung, Hypotonie, Oligurie, Tachykardie und gastrointestinale Störungen wie Übelkeit oder Erbrechen (siehe Abschnitt 4.8).
Das Risiko einer Hypokaliämie ist bei Patienten mit Leberzirrhose, bei Patienten mit schneller Diurese, bei Patienten, die eine unzureichende orale Aufnahme von Elektrolyten erhalten und bei Patienten, die gleichzeitig mit Kortikosteroiden oder ACTH behandelt werden, größer (siehe Abschnitt 4.5). Umgekehrt kann aufgrund des Angiotensin-II (AT-1)-Rezeptor-Antagonismus von Olmesartanmedoxomil, das in Olprezid enthalten ist, eine Hyperkaliämie auftreten, insbesondere bei Vorliegen einer eingeschränkten Nierenfunktion und/oder Herzinsuffizienz und Diabetes mellitus. Bei Risikopatienten wird eine angemessene Überwachung des Serumkaliums empfohlen. Kaliumsparende Diuretika, Kaliumergänzungsmittel oder kaliumhaltige Salzersatzstoffe und andere Arzneimittel, die eine Erhöhung des Serumkaliums bewirken können (wie Heparin), sollten während der Einnahme von Olprezide mit Vorsicht angewendet werden (siehe Abschnitt 4.5).
Es gibt keine Hinweise darauf, dass Olmesartanmedoxomil eine Diuretika-induzierte Hyponatriämie reduziert oder verhindert.Chloridmangel ist in der Regel mild und erfordert in der Regel keine Behandlung.
Thiazide können die Calciumausscheidung im Urin reduzieren und einen leichten und intermittierenden Anstieg des Serumcalciums verursachen, wenn keine bekannten Störungen des Calciumstoffwechsels vorliegen. Hypercalcämie kann eine Manifestation eines okkulten Hyperparathyreoidismus sein. Thiazide müssen vor einer Analyse der Nebenschilddrüsenfunktion abgesetzt werden.
Thiazide erhöhen nachweislich die Ausscheidung von Magnesium im Urin mit möglicher Hypomagnesiämie.
Bei ödematösen Patienten kann eine Verdünnungshyponatriämie auftreten, wenn sie hohen atmosphärischen Temperaturen ausgesetzt ist.
Lithium:
Wie bei anderen Arzneimitteln, die Angiotensin-II-Rezeptor-Antagonisten und Thiazide in Kombination enthalten, wird die gleichzeitige Anwendung von Lithium und Olprezid nicht empfohlen (siehe Abschnitt 4.5).
Ethnische Unterschiede:
Wie bei allen anderen Angiotensin-II-Antagonisten ist die blutdrucksenkende Wirkung von Olmesartanmedoxomil bei Patienten mit schwarzer Hautfarbe etwas geringer, möglicherweise aufgrund der höheren Prävalenz niedriger Reninspiegel in der Bevölkerung mit schwarzer Hautfarbe.
Dopingtest:
Das in diesem Arzneimittel enthaltene Hydrochlorothiazid kann positive Dopingtests verursachen.
Schwangerschaft:
Eine Behandlung mit Angiotensin-II-Antagonisten sollte während der Schwangerschaft nicht begonnen werden. Bei Patientinnen, die eine Schwangerschaft planen, sollte eine alternative blutdrucksenkende Behandlung mit einem etablierten Sicherheitsprofil für die Schwangerschaft angewendet werden, es sei denn, eine Fortsetzung der Behandlung mit Angiotensin-II-Antagonisten wird als notwendig erachtet mit Angiotensin-II-Antagonisten sollte sofort abgesetzt und gegebenenfalls eine alternative Therapie eingeleitet werden (siehe Abschnitte 4.3 und 4.6).
Sonstiges:
Bei Vorliegen einer generalisierten Arteriosklerose und bei Patienten mit ischämischer Herzkrankheit oder ischämischer zerebrovaskulärer Erkrankung besteht immer das Risiko, dass die übermäßige Blutdrucksenkung zu einem Herzinfarkt oder Schlaganfall führen kann.
Überempfindlichkeitsreaktionen gegen Hydrochlorothiazid können bei Patienten mit oder ohne Allergie oder Asthma bronchiale in der Vorgeschichte auftreten, sind jedoch bei solchen anamnestischen Befunden häufiger.
Bei der Anwendung von Thiaziddiuretika wurde über eine Verschlimmerung oder Aktivierung von systemischem Lupus erythematodes berichtet.
Dieses Arzneimittel enthält Lactose. Patienten mit der seltenen hereditären Galactose-Intoleranz, Lapp-Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten dieses Arzneimittel nicht einnehmen.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen -
Mögliche Wechselwirkungen mit Olmesartanmedoxomil und Hydrochlorothiazid
Gleichzeitige Anwendung nicht empfohlen
Lithium:
Bei gleichzeitiger Gabe von Lithium mit Angiotensin-Converting-Enzym-Hemmern und selten mit Angiotensin-II-Antagonisten wurde über einen reversiblen Anstieg der Lithiumkonzentration im Serum und der Toxizität berichtet Die Toxizität kann erhöht sein, daher wird die Anwendung von Olprezid und Lithium in Kombination nicht empfohlen (siehe Abschnitt 4.4). Wenn eine gleichzeitige Anwendung als notwendig erachtet wird, wird eine sorgfältige Überwachung des Serumlithiumspiegels empfohlen.
Bei gleichzeitiger Anwendung ist Vorsicht geboten
Baclofen
Eine Verstärkung der blutdrucksenkenden Wirkung kann auftreten.
Nichtsteroidale Antirheumatika (NSAR)
NSAR, zB Acetylsalicylsäure (> 3 g/Tag), COX2-Hemmer und nicht-selektive NSAR, können die blutdrucksenkende Wirkung von Thiaziddiuretika und Angiotensin-II-Antagonisten reduzieren.
Bei einigen Patienten mit eingeschränkter Nierenfunktion (z. B. dehydrierte oder ältere Patienten mit eingeschränkter Nierenfunktion) kann die gleichzeitige Anwendung von Angiotensin-II-Antagonisten und Cyclooxygenase-Hemmern zu einer weiteren Verschlechterung der Nierenfunktion, einschließlich eines möglichen akuten Nierenversagens, führen Kombination sollte mit Vorsicht angewendet werden, insbesondere bei älteren Patienten.Die Patienten sollten ausreichend hydratisiert werden und eine Überwachung der Nierenfunktion sollte nach Beginn der Begleitbehandlung und in regelmäßigen Abständen während dieser in Betracht gezogen werden.
Die gleichzeitige Anwendung muss bewertet werden
Amifostina
Eine Verstärkung der blutdrucksenkenden Wirkung kann auftreten.
Andere blutdrucksenkende Arzneimittel:
Die blutdrucksenkende Wirkung von Olprezid kann durch die gleichzeitige Anwendung anderer blutdrucksenkender Arzneimittel verstärkt werden.
Alkohol, Barbiturate, Betäubungsmittel oder Antidepressiva
Eine Potenzierung der orthostatischen Hypotonie kann auftreten.
Mögliche Wechselwirkungen mit Olmesartanmedoxomil:
Gleichzeitige Anwendung nicht empfohlen
Arzneimittel, die den Kaliumspiegel beeinflussen:
Basierend auf den Erfahrungen mit anderen Arzneimitteln, die das Renin-Angiotensin-System beeinflussen, ist die gleichzeitige Anwendung von kaliumsparenden Diuretika, Kaliumpräparaten, kaliumhaltigen Salzersatzmitteln oder anderen Arzneimitteln, die einen erhöhten Serumkaliumspiegel verursachen können (z. B. Heparin, ACE-Hemmer) können zu einem Anstieg des Serumkaliumspiegels führen (siehe Abschnitt 4.4) Wenn Arzneimittel, die den Kaliumspiegel beeinflussen können, in Kombination mit Olprezide verschrieben werden, Überwachung des Kaliumspiegels im Plasma.
Weitere Informationen
Eine mäßige Verringerung der Bioverfügbarkeit von Olmesartan wurde nach der Behandlung mit Antazida (Aluminiummagnesiumhydroxid) beobachtet.
Olmesartanmedoxomil hat keinen signifikanten Einfluss auf die Pharmakokinetik oder Pharmakodynamik von Warfarin oder die Pharmakokinetik von Digoxin.
Die gleichzeitige Anwendung von Olmesartanmedoxomil und Pravastatin hatte bei gesunden Probanden keine klinisch relevanten Auswirkungen auf die Pharmakokinetik der beiden Substanzen.
Olmesartan hat in vitro keine klinisch relevante Hemmwirkung auf die humanen Cytochrom-P450-Enzyme 1A1 / 2, 2A6, 2C8 / 9, 2C19, 2D6, 2E1 und 3A4, während die Induktionswirkungen auf Cytochrom P450 der Ratte minimal sind oder gar nicht vorhanden sind. Klinisch relevante Wechselwirkungen zwischen Olmesartan und Arzneimitteln, die durch die oben genannten Cytochrom-P450-Enzyme metabolisiert werden, sind nicht zu erwarten.
Mögliche Wechselwirkungen mit Hydrochlorothiazid: Gleichzeitige Anwendung nicht empfohlen Arzneimittel, die den Kaliumspiegel beeinflussen:
Die kaliumabbauende Wirkung von Hydrochlorothiazid (siehe Abschnitt 4.4) kann durch die gleichzeitige Anwendung anderer Arzneimittel im Zusammenhang mit Kaliumverlust und Hypokaliämie (z Säurederivate) Daher wird eine solche gleichzeitige Anwendung nicht empfohlen.
Bei gleichzeitiger Anwendung ist Vorsicht geboten
Calciumsalze
Thiaziddiuretika können den Serumkalziumspiegel erhöhen, indem sie ihre Ausscheidung verringern. Wenn Kalziumpräparate verschrieben werden sollen, sollten die Serumkalziumspiegel überwacht und die Kalziumdosis entsprechend angepasst werden.
Colestyramin- und Colestipolharze
Die Aufnahme von Hydrochlorothiazid wird in Gegenwart von Anionenaustauscherharzen beeinträchtigt.
Digitalis-Glykoside
Thiazid-induzierte Hypokaliämie oder Hypomagnesiämie können Digitalis-induzierte Herzrhythmusstörungen begünstigen.
Arzneimittel, die von Veränderungen des Kaliumspiegels betroffen sind
Eine regelmäßige Überwachung des Serumkaliums und des EKGs wird empfohlen, wenn Olprezide gleichzeitig mit Arzneimitteln angewendet wird, die von Kaliumanomalien betroffen sind (z. B. Digitalisglykoside und Antiarrhythmika) oder mit den folgenden Arzneimitteln (einschließlich einiger Antiarrhythmika), die Torsade de pointes (ventrikuläre Tachykardie), da Hypokaliämie ein prädisponierender Faktor für Torsades de Pointes (ventrikuläre Tachykardie) ist:
Antiarrhythmika der Klasse Ia (z. B. Chinidin, Hydrochinidin, Disopyramid)
Klasse-III-Antiarrhythmika (z. B. Amiodaron, Sotalol, Dofetilid, Ibutilid)
einige Antipsychotika (z. B. Thioridazin, Chlorpromazin, Levomepromazin, Trifluoperazin, Ciamemazin, Sulpirid, Sultoprid, Amisulprid, Thiaprid, Pimozid, Haloperidol, Droperidol)
andere (z. B. Bepridyl, Cisaprid, Dihemanyl, iv Erythromycin, Halofantrin, Mizolastin, Pentamidin, Sparfloxacin, Terfenadin, iv Vincamin).
Nichtdepolarisierende Muskelrelaxanzien (z. B. Tubocurarin)
Die Wirkung von nicht depolarisierenden Muskelrelaxanzien kann durch Hydrochlorothiazid verstärkt werden.
Anticholinergika (zB Atropin, Biperiden)
Erhöhte Bioverfügbarkeit von Thiaziddiuretika aufgrund einer verringerten gastrointestinalen Motilität und einer verringerten Magenentleerungszeit.
Olmesartan hat in vitro keine klinisch relevante Hemmwirkung auf die humanen Cytochrom-P450-Enzyme 1A1 / 2, 2A6, 2C8 / 9, 2C19, 2D6, 2E1 und 3A4, während die Induktionswirkungen auf Cytochrom P450 der Ratte minimal sind oder gar nicht vorhanden sind. Klinisch relevante Wechselwirkungen zwischen Olmesartan und Arzneimitteln, die durch die oben genannten Cytochrom-P450-Enzyme metabolisiert werden, sind nicht zu erwarten.
Mögliche Wechselwirkungen mit Hydrochlorothiazid: Gleichzeitige Anwendung nicht empfohlen Arzneimittel, die den Kaliumspiegel beeinflussen:
Die kaliumabbauende Wirkung von Hydrochlorothiazid (siehe Abschnitt 4.4) kann durch die gleichzeitige Anwendung anderer Arzneimittel im Zusammenhang mit Kaliumverlust und Hypokaliämie (z Säurederivate) Daher wird eine solche gleichzeitige Anwendung nicht empfohlen.
Bei gleichzeitiger Anwendung ist Vorsicht geboten
Calciumsalze
Thiaziddiuretika können den Serumkalziumspiegel erhöhen, indem sie ihre Ausscheidung verringern. Wenn Kalziumpräparate verschrieben werden sollen, sollten die Serumkalziumspiegel überwacht und die Kalziumdosis entsprechend angepasst werden.
Colestyramin- und Colestipolharze
Die Aufnahme von Hydrochlorothiazid wird in Gegenwart von Anionenaustauscherharzen beeinträchtigt.
Digitalis-Glykoside
Thiazid-induzierte Hypokaliämie oder Hypomagnesiämie können Digitalis-induzierte Herzrhythmusstörungen begünstigen.
Arzneimittel, die von Veränderungen des Kaliumspiegels betroffen sind
Eine regelmäßige Überwachung des Serumkaliums und des EKGs wird empfohlen, wenn Olprezide gleichzeitig mit Arzneimitteln angewendet wird, die von Kaliumanomalien betroffen sind (z. B. Digitalisglykoside und Antiarrhythmika) oder mit den folgenden Arzneimitteln (einschließlich einiger Antiarrhythmika), die Torsade de pointes (ventrikuläre Tachykardie), da Hypokaliämie ein prädisponierender Faktor für Torsades de Pointes (ventrikuläre Tachykardie) ist:
Antiarrhythmika der Klasse Ia (z. B. Chinidin, Hydrochinidin, Disopyramid)
Antiarrhythmika der Klasse III (z. B. Amiodaron, Sotalol, Dofetilid, Ibutilid)
einige Antipsychotika (z. B. Thioridazin, Chlorpromazin, Levomepromazin, Trifluoperazin, Ciamemazin, Sulpirid, Sultoprid, Amisulprid, Thiaprid, Pimozid, Haloperidol, Droperidol)
andere (z. B. Bepridyl, Cisaprid, Dihemanyl, iv Erythromycin, Halofantrin, Mizolastin, Pentamidin, Sparfloxacin, Terfenadin, iv Vincamin).
Nichtdepolarisierende Muskelrelaxanzien (z. B. Tubocurarin)
Die Wirkung von nicht depolarisierenden Muskelrelaxanzien kann durch Hydrochlorothiazid verstärkt werden.
Anticholinergika (zB Atropin, Biperiden)
Erhöhte Bioverfügbarkeit von Thiaziddiuretika aufgrund einer verringerten gastrointestinalen Motilität und einer verringerten Magenentleerungszeit.
Antidiabetika (orale Arzneimittel und Insulin)
Die Behandlung mit einem Thiazid-Diuretikum kann die Glukosetoleranz beeinträchtigen. Dosisanpassungen von Antidiabetika können erforderlich sein (siehe Abschnitt 4.4).
Metformin
Metformin sollte aufgrund des Risikos einer Laktatazidose aufgrund eines möglichen funktionellen Nierenversagens in Verbindung mit Hydrochlorothiazid mit Vorsicht angewendet werden.
Betablocker und Diazoxid
Die hyperglykämische Wirkung von Betablockern und Diazoxid kann durch Thiazide verstärkt werden.
Pressoramine (Noradrenalin)
Die Wirkung von Pressoraminen kann verringert werden.
Arzneimittel zur Behandlung von Gicht (Probenecid, Sulfinpyrazon und Allopurinol)
Eine Dosisanpassung von Urikosurika kann erforderlich sein, da Hydrochlorothiazid den Serumharnsäurespiegel erhöhen kann Eine Dosiserhöhung von Probenecid oder Sulfinpyrazon kann erforderlich sein Die gleichzeitige Anwendung eines Thiaziddiuretikums kann die Inzidenz von Überempfindlichkeitsreaktionen gegenüber Allopurinol erhöhen.
Amantadina
Thiazide können das Risiko von Nebenwirkungen von Amantadin erhöhen.
Zytotoxische Arzneimittel (z. B. Cyclophosphamid, Methotrexat)
Thiazide können die renale Ausscheidung von Zytostatika reduzieren und ihre myelosuppressive Wirkung verstärken.
Salicylate
Bei Anwendung hoher Salicylat-Dosen kann Hydrochlorothiazid die toxische Wirkung von Salicylat auf das Zentralnervensystem verstärken.
Methyldopa
Es gab vereinzelte Berichte über hämolytische Anämie nach gleichzeitiger Anwendung von Hydrochlorothiazid und Methyldopa.
Cyclosporin
Die gleichzeitige Behandlung mit Ciclosporin kann das Risiko einer Hyperurikämie und gichtähnlicher Komplikationen erhöhen.
Tetracycline
Die gleichzeitige Anwendung von Tetracyclinen und Thiaziden erhöht das Risiko eines Tetracyclin-induzierten Anstiegs der Harnstoffspiegel. Diese Wechselwirkung tritt bei Doxycyclin wahrscheinlich nicht auf.
04.6 Schwangerschaft und Stillzeit -
Schwangerschaft (siehe Abschnitt 4.3):
Aufgrund der Wirkungen der Wirkstoffe dieser Kombination in der Schwangerschaft wird die Anwendung von Olprezide während des ersten Schwangerschaftstrimesters nicht empfohlen (siehe Abschnitt 4.4) Die Anwendung von Olprezide ist während des zweiten und dritten Schwangerschaftstrimesters kontraindiziert (siehe Abschnitt ). 4.4) siehe Abschnitte 4.3 und 4.4).
Olmesartan Medoxomil
Die Anwendung von Angiotensin-II-Antagonisten wird während des ersten Schwangerschaftstrimesters nicht empfohlen (siehe Abschnitt 4.4). Die Anwendung von Angiotensin-II-Antagonisten ist während des zweiten und dritten Schwangerschaftstrimesters kontraindiziert (siehe Abschnitte 4.3 und 4.4).
Epidemiologische Hinweise auf das Teratogenitätsrisiko nach Exposition mit ACE-Hemmern während des ersten Schwangerschaftstrimesters sind nicht schlüssig; eine geringfügige Erhöhung des Risikos kann jedoch nicht ausgeschlossen werden. Obwohl keine kontrollierten epidemiologischen Risikodaten für Angiotensin-II-Antagonisten verfügbar sind, kann ein ähnliches Risiko auch für diese Arzneimittelklasse bestehen.Bei Patientinnen, die eine Schwangerschaft planen, sollte eine alternative blutdrucksenkende Behandlung mit einem nachgewiesenen Sicherheitsprofil für die Anwendung in der Schwangerschaft angewendet werden, es sei denn, eine fortgesetzte Therapie mit Angiotensin-II-Antagonisten wird als notwendig erachtet. Wenn eine Schwangerschaft diagnostiziert wird, sollte die Behandlung mit Angiotensin-II-Antagonisten sofort abgebrochen und gegebenenfalls eine alternative Therapie eingeleitet werden.
Es ist bekannt, dass die Exposition gegenüber Angiotensin-II-Antagonisten während des zweiten und dritten Trimesters fötale Toxizität (verminderte Nierenfunktion, Oligohydramnion, verzögerte Verknöcherung des Schädels) und neonatale Toxizität (Nierenversagen, Hypotonie, Hyperkaliämie) induziert (siehe auch Abschnitt 5.3).
Bei Exposition mit Angiotensin-II-Antagonisten ab dem zweiten Schwangerschaftstrimester wird eine Ultraschalluntersuchung der Nierenfunktion und des Schädels empfohlen.
Neugeborene, deren Mütter Angiotensin-II-Antagonisten eingenommen haben, sollten engmaschig auf Hypotonie überwacht werden (siehe Abschnitte 4.3 und 4.4).
Hydrochlorothiazid
Die Erfahrungen mit der Anwendung von Hydrochlorothiazid während der Schwangerschaft, insbesondere im ersten Trimester, sind begrenzt. Tierversuche sind unzureichend.
Hydrochlorothiazid ist plazentagängig.Aufgrund des pharmakologischen Wirkmechanismus von Hydrochlorothiazid kann seine Anwendung während des zweiten und dritten Schwangerschaftstrimesters die fetoplazentare Durchblutung beeinträchtigen und fetale und neonatale Wirkungen wie Gelbsucht, Elektrolytstörungen und Thrombozytopenie verursachen.
Hydrochlorothiazid sollte bei Schwangerschaftsödemen, Schwangerschaftshypertonie oder Präeklampsie wegen des Risikos eines Plasmavolumenmangels und einer plazentaren Hypoperfusion ohne günstige Auswirkungen auf den Krankheitsverlauf nicht angewendet werden.
Hydrochlorothiazid sollte bei schwangeren Frauen nicht bei essentieller Hypertonie angewendet werden, außer in den seltenen Situationen, in denen keine andere Behandlung angewendet werden kann.
Fütterungszeit
Olmesartan Medoxomil
Da keine Daten zur Anwendung von Olprezide während der Stillzeit vorliegen, wird die Anwendung von Olprezide nicht empfohlen und alternative Therapien mit einem nachgewiesenen Sicherheitsprofil für die Stillzeit sollten bevorzugt werden, insbesondere bei Neugeborenen oder Frühgeborenen.
Hydrochlorothiazid
Hydrochlorothiazid geht in geringen Mengen in die Muttermilch über. Hohe Thiaziddosen, die zu einer intensiven Diurese führen, können die Milchproduktion hemmen. Die Anwendung von Olpreziden während der Stillzeit wird nicht empfohlen. Sie müssen so niedrig wie möglich gehalten werden.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen -
Olprezid kann einen leichten oder mäßigen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen haben Bei Patienten unter blutdrucksenkender Therapie können gelegentlich Schwindel oder Müdigkeitserscheinungen auftreten, die die Reaktionsfähigkeit beeinträchtigen können.
04.8 Nebenwirkungen -
Die am häufigsten berichteten Nebenwirkungen während der Behandlung mit Olprezide sind Kopfschmerzen (2,9 %), Schwindel (1,9 %) und Müdigkeit (1,0 %).
Hydrochlorothiazid kann einen Flüssigkeitsmangel verursachen oder verschlimmern, der zu einem Elektrolytungleichgewicht führen kann (siehe Abschnitt 4.4).
In klinischen Studien mit 1155 Patienten, die die Olmesartanmedoxomil/Hydrochlorothiazid-Kombination in Dosen von 20/12,5 mg oder 20/25 mg erhielten, und 466 Patienten, die Placebo über einen Zeitraum von bis zu 21 Monaten erhielten, wurde die Gesamthäufigkeit der Nebenwirkungen der Kombination Olmesartanmedoxomil/ Hydrochlorothiazid waren ähnlich wie Placebo Abbruch der Behandlung aufgrund von Nebenwirkungen war auch für Olmesartanmedoxomil/Hydrochlorothiazid 20/12,5 mg 20/25 mg (2 %) und für Placebo (3 %) ähnlich / Hydrochlorothiazid-Gruppe insgesamt im Vergleich zu Placebo schien nicht altersabhängig zu sein (
Darüber hinaus wurde die Verträglichkeit von hochdosiertem Olprezid in klinischen Studien mit 3709 Patienten untersucht, die Olmesartanmedoxomil in Kombination mit Hydrochlorothiazid in Dosierungen von 40 mg/12,5 mg und 40 mg/25 mg erhielten.
Nebenwirkungen, die mit Olprezide in klinischen Studien, Verträglichkeitsstudien nach der Zulassung und Spontanberichten beobachtet wurden, sind in der folgenden Tabelle aufgeführt, ebenso wie die Nebenwirkungen, die durch die Einzelkomponenten Olmesartanmedoxomil und Hydrochlorothiazid basierend auf dem Verträglichkeitsprofil dieser Substanzen hervorgerufen werden.
Die folgende Terminologie wurde verwendet, um die Häufigkeit von Nebenwirkungen zu klassifizieren: sehr häufig (≥ 1/10); häufig (≥ 1/100 Jahre)
In zeitlicher Verbindung mit der Einnahme von Angiotensin-II-Rezeptorblockern wurden einzelne Fälle von Rhabdomyolyse berichtet.
04.9 Überdosierung -
Es liegen keine spezifischen Informationen zu den Wirkungen oder der Behandlung einer Olprezid-Überdosierung vor. Der Patient sollte sorgfältig überwacht werden und die Behandlung sollte symptomatisch und unterstützend sein. Die Behandlung hängt von der Zeit seit der Einnahme und der Schwere der Symptome ab.Zu den empfohlenen Maßnahmen gehören Erbrechen und/oder Magenspülung. Aktivkohle kann bei der Behandlung einer Überdosierung hilfreich sein. Serumelektrolyte und Kreatinin sollten häufig kontrolliert werden. Wenn eine Hypotonie auftritt, sollte der Patient in Rückenlage mit rascher Wiederherstellung des Plasmavolumens und der Salze gelagert werden.
Die am wahrscheinlichsten zu erwartenden Manifestationen einer Olmesartanmedoxomil-Überdosierung sind Hypotonie und Tachykardie; Bradykardie kann ebenfalls auftreten. Eine Überdosierung von Hydrochlorothiazid ist mit Elektrolytmangel (Hypokaliämie, Hypochlorämie) und Dehydration aufgrund übermäßiger Diurese verbunden. Die häufigsten Anzeichen und Symptome einer Überdosierung sind Übelkeit und Bei gleichzeitiger Anwendung von Digitalisglykosiden oder bestimmten Antiarrhythmika kann eine Hypokaliämie zu schweren Muskelkrämpfen und/oder Herzrhythmusstörungen führen.
Es liegen keine Daten zur Dialysierbarkeit von Olmesartan oder Hydrochlorothiazid vor.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN -
05.1 "Pharmakodynamische Eigenschaften -
Pharmakotherapeutische Gruppe:
Diuretika-assoziierte Angiotensin-II-Antagonisten, ATC-Code: C09DA08.
Wirkmechanismus / Pharmakodynamische Wirkungen
Olprezid ist eine Kombination aus einem Angiotensin-II-Rezeptor-Antagonisten, Olmesartanmedoxomil, und einem Thiazid-Diuretikum, Hydrochlorothiazid. Die Kombination dieser Substanzen hat eine additive blutdrucksenkende Wirkung und senkt den Blutdruck stärker als jede der beiden Komponenten allein.
Die einmal tägliche Verabreichung von Olprezide gewährleistet eine wirksame und schrittweise Senkung des Blutdrucks in den 24 Stunden zwischen zwei Verabreichungen.
Olmesartan Medoxomil ist ein oral wirksamer selektiver Angiotensin-II-Rezeptor-Antagonist (Typ AT1). Angiotensin II ist das wichtigste vasoaktive Hormon des Reninangiotensin-Aldosteron-Systems und spielt eine bedeutende Rolle in der Pathophysiologie des Bluthochdrucks. Die Wirkungen von Angiotensin II umfassen Vasokonstriktion, Stimulation der Aldosteronsynthese und -freisetzung , Herzstimulation und renale Natriumreabsorption Olmesartan blockiert die vasokonstriktorischen und aldosteronsekretorischen Wirkungen von Angiotensin II, indem es seine Bindung an den AT1-Rezeptor in Geweben, einschließlich glatter Gefäßmuskulatur und Nebenniere, blockiert. Die Wirkung von Olmesartan ist unabhängig von der Herkunft oder dem Weg der Synthese von Angiotensin II. Der selektive Antagonismus von Olmesartan gegen den Angiotensin-II-Rezeptor (AT1) führt zu einem Anstieg der Plasma-Reninspiegel und der Konzentrationen von Angiotensin I und II und einer gewissen Abnahme der Plasmakonzentrationen Aldosteron-Tics.
Bei Hypertonie bewirkt Olmesartanmedoxomil eine langfristige dosisabhängige Senkung des Blutdrucks.
Die einmal tägliche Gabe von Olmesartanmedoxomil gewährleistet eine effektive und konstante Blutdrucksenkung im 24-Stunden-Intervall zwischen einer Dosis und der nächsten Bei gleicher Gesamtdosis führte die einmal tägliche Gabe zu ähnlichen Blutdrucksenkungen wie die Gabe . des Arzneimittels zweimal täglich.
Bei fortgesetzter Behandlung wird die maximale Blutdrucksenkung innerhalb von 8 Wochen nach Therapiebeginn erreicht, obwohl ein wesentlicher Anteil der blutdrucksenkenden Wirkung bereits nach 2 Behandlungswochen beobachtet wird.
Die Auswirkungen von Olmesartan auf Mortalität und Morbidität sind derzeit nicht bekannt. L "Hydrochlorothiazid ist ein Thiazid-Diuretikum. Der Mechanismus der blutdrucksenkenden Wirkung von Thiaziddiuretika ist nicht vollständig geklärt Thiazide wirken auf die Elektrolytrückresorptionsmechanismen des Nierentubulus und erhöhen direkt die Ausscheidung von Natrium und Chlor in ungefähr äquivalenten Mengen. Die harntreibende Wirkung von Hydrochlorothiazid reduziert das Plasmavolumen, erhöht die Plasmareninaktivität und erhöht die Aldosteronsekretion, was zu einem erhöhten Verlust von Bicarbonat und Kalium im Urin und einer Abnahme des Serumkaliums führt.Die Renin-Aldosteron-Bindung wird durch Angiotensin II vermittelt und daher neigt die gleichzeitige Gabe eines Angiotensin-II-Rezeptor-Antagonisten dazu, dem mit Thiaziddiuretika verbundenen Kaliumverlust entgegenzuwirken. Bei Hydrochlorothiazid tritt die Diurese nach etwa zwei Stunden ein und der Höhepunkt der Wirkung etwa vier Stunden nach der Verabreichung, während die Wirkung etwa 612 Stunden anhält.
Epidemiologische Studien haben gezeigt, dass eine Langzeitbehandlung mit Hydrochlorothiazid allein das Risiko kardiovaskulärer Mortalität und Morbidität reduziert.
Klinische Wirksamkeit und Sicherheit
Die Kombination von Olmesartanmedoxomil und Hydrochlorothiazid führt zu einer additiven Blutdrucksenkung, die im Allgemeinen mit steigender Dosis jedes Bestandteils zunimmt.In den Gesamtdaten der placebokontrollierten Studien führte die Anwendung der Kombination Olmesartanmedoxomil / Hydrochlorothiazid 20 / 12,5 mg und 20/25 mg zu eine mittlere Senkung (abzüglich der Senkung aufgrund von Placebo) des systolischen/diastolischen Blutdrucks auf den niedrigsten Wert von 12/7 mmHg bzw. 16/9 mmHg. Alter und Geschlecht hatten keinen klinisch relevanten Einfluss auf das Ansprechen auf die Behandlung mit der Kombination Olmesartanmedoxomil / Hydrochlorothiazid.
Die Gabe von 12,5 mg und 25 mg Hydrochlorothiazid bei Patienten, die bei einer Therapie mit 20 mg Olmesartanmedoxomil allein nicht ausreichend eingestellt waren, führte zu einer „weiteren Senkung des diastolischen/systolischen 24-Stunden-Blutdrucks, gemessen durch ambulante Blutdrucküberwachung. 7/5 mmHg und 12/7 mmHg im Vergleich zu den Ausgangswerten nach Monotherapie mit Olmesartanmedoxomil Die mittlere weitere Senkung des systolischen / diastolischen Blutdrucks auf den niedrigsten Wert vom Ausgangswert, konventionell gemessen, betrug 11/10 mmHg bzw. 16/ 11 mmHg.
Die Wirksamkeit der Kombination Olmesartanmedoxomil/Hydrochlorothiazid wurde im Verlauf von Langzeitbehandlungen (ein Jahr) aufrechterhalten. Das Absetzen von Olmesartanmedoxomil mit oder ohne gleichzeitige Gabe von Hydrochlorothiazid führte nicht zu einer Rebound-Hypertonie. Die Auswirkungen der Fixkombination Olmesartanmedoxomil / Hydrochlorothiazid auf die kardiovaskuläre Morbidität und Mortalität sind derzeit nicht bekannt.
05.2 "Pharmakokinetische Eigenschaften -
Aufnahme und Verteilung
Olmesartanmedoxomil:
Olmesartanmedoxomil ist ein Prodrug, das während der Resorption aus dem Magen-Darm-Trakt durch Esterasen in der Darmschleimhaut und im Pfortaderkreislauf schnell in das pharmakologisch aktive Stoffwechselprodukt Olmesartan umgewandelt wird. Es gibt keine Spuren von intaktem Olmesartanmedoxomil oder der intakten Medoxomil-Seitenkette im Plasma oder in den Ausscheidungen. Die mittlere absolute Bioverfügbarkeit von Olmesartan in der Tablettenformulierung betrug 25,6 %.
Die mittlere Spitzenkonzentration (Cmax) von Olmesartan wird im Durchschnitt innerhalb von etwa 2 Stunden nach oraler Gabe von Olmesartanmedoxomil erreicht; Die Plasmakonzentrationen von Olmesartan steigen ungefähr linear an, wenn die orale Einzeldosis auf ungefähr 80 mg ansteigt.
Die Nahrungsaufnahme hat minimale Auswirkungen auf die Bioverfügbarkeit von Olmesartan und daher kann Olmesartanmedoxomil nüchtern oder nüchtern verabreicht werden.
Es wurden keine klinisch relevanten Unterschiede in der Pharmakokinetik von Olmesartan in Abhängigkeit vom Geschlecht des Patienten beobachtet.
Olmesartan wird stark an Plasmaproteine (99,7%) gebunden, aber das Potenzial für klinisch signifikante Proteinbindungsverdrängungswechselwirkungen zwischen Olmesartan und anderen hoch gebundenen Wirkstoffen, die gleichzeitig verabreicht werden, ist gering (wie durch das Fehlen einer Wechselwirkung bestätigt. Klinisch signifikant zwischen Olmesartan Medoxomil und Warfarin). Die Bindung von Olmesartan an Blutzellen ist vernachlässigbar. Das mittlere Verteilungsvolumen nach intravenöser Verabreichung ist gering (16-29 l).
Hydrochlorothiazid:
Nach oraler Gabe von kombiniertem Olmesartanmedoxomil und Hydrochlorothiazid lag die mediane Zeit bis zur maximalen Plasmakonzentration von Hydrochlorothiazid zwischen 1,5 und 2 Stunden nach Einnahme. Hydrochlorothiazid ist zu 68 % an Plasmaproteine gebunden und sein scheinbares Verteilungsvolumen beträgt 0,831,14 l / kg.
Stoffwechsel und Ausscheidung
Olmesartanmedoxomil:
Die Gesamtplasmaclearance von Olmesartan betrug 1,3 L/h (CV 19%), relativ niedrig im Vergleich zum Leberfluss (ca. 90 L/h). Nach oraler Gabe einer Einzeldosis von 14C-markiertem Olmesartanmedoxomil wurden 1016 % der verabreichten Radioaktivität mit dem Urin ausgeschieden (größtenteils innerhalb von 24 Stunden nach Einnahme), während die restliche Radioaktivität mit den Fäzes ausgeschieden wurde. Basierend auf einer systemischen Bioverfügbarkeit von 25,6% kann geschätzt werden, dass resorbiertes Olmesartan renal (ca. 40%) und hepatobiliär (ca. 60%) ausgeschieden wird.Die gesamte wiedergefundene Radioaktivität wurde als Olmesartan identifiziert Da Olmesartan in großen Mengen über die Gallenwege ausgeschieden wird, ist die Anwendung bei Patienten mit Gallenwegsobstruktion kontraindiziert (siehe Abschnitt 4.3).
Die terminale Eliminationshalbwertszeit von Olmesartan variiert zwischen 10 und 15 Stunden nach wiederholter oraler Verabreichung. Steady State wurde nach den ersten Verabreichungen erreicht und nach 14 Tagen wiederholter Verabreichung wurde keine weitere Akkumulation festgestellt. Die renale Clearance betrug ungefähr 0,50,7 l/ h und war dosisunabhängig.
Hydrochlorothiazid:
Hydrochlorothiazid wird beim Menschen nicht metabolisiert und wird fast vollständig als unveränderter Wirkstoff mit dem Urin ausgeschieden. Ungefähr 60 % der oralen Dosis werden innerhalb von 48 Stunden als unveränderter Wirkstoff ausgeschieden. Die renale Clearance beträgt etwa 250-300 ml / min.
Die terminale Eliminationshalbwertszeit von Hydrochlorothiazid beträgt 1015 Stunden.
Olprezid
Die systemische Verfügbarkeit von Hydrochlorothiazid wird bei gleichzeitiger Anwendung mit Olmesartanmedoxomil um ca. 20 % reduziert, diese geringfügige Reduzierung ist jedoch ohne klinische Relevanz. Die Kinetik von Olmesartan wird durch die gleichzeitige Anwendung von Hydrochlorothiazid nicht beeinflusst.
Pharmakokinetik in speziellen Patientengruppen
Ältere (65 Jahre oder älter):
Bei hypertensiven Patienten war die AUC von Olmesartan im Steady-State bei älteren Patienten (65 bis 75 Jahre) um ca. 35 % und bei sehr älteren Patienten (75 Jahre) um ca. 44 % im Vergleich zu älteren Patienten erhöht (siehe Abschnitt 4.2). ). Begrenzte Daten deuten jedoch darauf hin, dass die systemische Clearance von Hydrochlorothiazid bei älteren, gesunden oder hypertensiven Patienten im Vergleich zu jungen gesunden Probanden verringert ist..
Veränderte Nierenfunktion:
Bei Patienten mit eingeschränkter Nierenfunktion war die Steady-State-AUC von Olmesartan bei Patienten mit leichter, mittelschwerer und schwerer Nierenfunktionsstörung um 62 %, 82 % bzw. 179 % im Vergleich zu gesunden Kontrollpersonen erhöht (siehe Abschnitte 4.2, 4.4). Bei Patienten mit eingeschränkter Nierenfunktion ist die Halbwertszeit von Hydrochlorothiazid verlängert.
Eingeschränkte Leberfunktion:
Nach einmaliger oraler Gabe waren die AUC-Werte von Olmesartan bei Patienten mit leichter und mittelschwerer Leberfunktionsstörung um 6 % bzw. 65 % höher als bei Personen mit normaler Leberfunktion mit leichter Leberfunktionsstörung und 0,41 % bei Patienten mit mittelschwerer Leberfunktionsstörung Nach wiederholter Einnahme bei Patienten mit mittelschwerer Leberfunktionsstörung war die mittlere AUC von Olmesartan immer noch etwa 65 % höher als bei gesunden Kontrollpersonen. Die mittleren Cmax-Werte von Olmesartan waren bei Patienten mit eingeschränkter Leberfunktion und gesunden Probanden ähnlich. Olmesartanmedoxomil wurde bei Patienten mit schwerer Leberfunktionsstörung nicht untersucht (siehe Abschnitte 4.2, 4.4).Eine Leberfunktionsstörung hat keinen signifikanten Einfluss auf die Pharmakokinetik von Hydrochlorothiazid.
05.3 Präklinische Daten zur Sicherheit -
Die potenzielle Toxizität der Kombination Olmesartanmedoxomil/Hydrochlorothiazid wurde in oralen Toxizitätsstudien mit wiederholter Gabe von bis zu sechs Monaten Dauer an Ratten und Hunden untersucht.
Wie sowohl bei Einzelkomponenten als auch bei anderen Arzneimitteln dieser Klasse ist das toxikologische Hauptzielorgan der Kombination die Niere. Die Kombination von Olmesartanmedoxomil/Hydrochlorothiazid induzierte Veränderungen der Nierenfunktion (Erhöhung des Serum-Harnstoff-Stickstoffs und des Serum-Kreatinins). Hohe Dosierungen verursachten eine tubuläre Degeneration und Regeneration in den Nieren von Ratten und Hunden, möglicherweise durch Veränderungen der renalen Hämodynamik (verminderte Nierendurchblutung aufgrund von Hypotonie mit tubulärer Hypoxie und tubulärer Zelldegeneration) Darüber hinaus führte die Kombination Olmesartanmedoxomil / Hydrochlorothiazid zu einer Verringerung der Erythrozytenparameter (Erythrozytenzahl, Hämoglobin, Hämatokrit) und Gewichtsreduktion des Herzens bei Ratten. Diese Wirkungen wurden auch bei den anderen AT1-Rezeptor-Antagonisten und bei ACE-Hemmern beobachtet; sie scheinen durch eine pharmakologische Wirkung von Olmesartanmedoxomil in hohen Dosen induziert worden zu sein und scheinen beim Menschen in den empfohlenen therapeutischen Dosen nicht relevant zu sein.
Genotoxizitätsstudien mit Olmesartanmedoxomil und Hydrochlorothiazid in Kombination oder allein ergaben keine Anzeichen einer klinisch relevanten genotoxischen Aktivität.
Das krebserzeugende Potenzial der Kombination von Olmesartanmedoxomil und Hydrochlorothiazid wurde nicht untersucht, da es unter klinischen Anwendungsbedingungen keine Hinweise auf relevante krebserzeugende Wirkungen der beiden Einzelkomponenten gibt.
Es gibt keine Hinweise auf Teratogenität bei Mäusen oder Ratten, die mit der Kombination Olmesartanmedoxomil/Hydrochlorothiazid behandelt wurden. Wie für diese Arzneimittelklasse zu erwarten, wurde bei Ratten eine fetale Toxizität beobachtet, die durch ein geringes fetales Gewicht von Müttern, die während der Schwangerschaft mit Olmesartan, Medoxomil und Hydrochlorothiazid behandelt wurden, nachgewiesen wurde (siehe Abschnitte 4.3, 4.6).
06.0 PHARMAZEUTISCHE INFORMATIONEN -
06.1 Hilfsstoffe -
Kern des Tablets Mikrokristalline Cellulose Lactose-Monohydrat
Hyprolose mit geringer Substitution
Hyprolose
Magnesiumstearat
Glasur Hypromellose Talkum
Titandioxid (E 171)
Eisen(III)-oxid gelb (E 172) Eisen(III)-oxid rot (E 172)
06.2 Inkompatibilität "-
Nicht relevant.
06.3 Gültigkeitsdauer "-
5 Jahre.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung -
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks -
Laminiertes Polyamid / Aluminium / Polyvinylchlorid / Aluminiumblister.
Packungen enthalten 14, 28, 30, 56, 84, 90, 98 oder 10x28 Filmtabletten. Einzeldosis-Blisterpackungen enthalten 10, 50 oder 500 Filmtabletten.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
06.6 Gebrauchs- und Handhabungshinweise -
Keine besonderen Anweisungen.
07.0 INHABER DER "MARKETING GENEHMIGUNG" -
Menarini International Operations Luxembourg S.A.
1, Avenue de la Gare, L1611 Luxemburg unter Lizenz der Daiichi Sankyo Europe GmbH
Händler zu verkaufen: Malesci Istituto Farmacobiologico S.p.A. Badezimmer in Ripoli
08.0 NUMMER DER VERMARKTUNGSBERECHTIGUNG -
OLPREZIDE 20 mg / 12,5 mg Filmtabletten:
14 Tabletten 037109016;
28 Tabletten 037109028;
30 Tabletten 037109030;
56 Tabletten 037109042;
84 Tabletten 037109055;
90 Tabletten 037109067;
98 Tabletten 037109079;
10X28 Tabletten 037109081;
10 Tabletten 037109093;
50 Tabletten 037109105;
500 Tabletten 037109117.
OLPREZIDE 20 mg / 25 mg Filmtabletten:
14 Tabletten 037109129;
28 Tabletten 037109131;
30 Tabletten 037109143;
56 Tabletten 037109156;
84 Tabletten 037109168;
90 Tabletten 037109170;
98 Tabletten 037109182;
10X28 Tabletten 037109194;
10 Tabletten 037109206;
50 Tabletten 037109218;
500 Tabletten 037109220.
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG -
Datum der Erstzulassung: Februar 2007
Datum der letzten Verlängerung: 07. Juni 2011
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs -
Juli 2012