Wirkstoffe: Levodopa, Carbidopa
SINEMET 200 mg + 50 mg Tabletten mit veränderter Wirkstofffreisetzung
SINEMET 100 mg + 25 mg Tabletten mit veränderter Wirkstofffreisetzung
Sinemet Packungsbeilagen sind erhältlich für Packungsgrößen: - SINEMET 250 mg + 25 mg Tabletten, SINEMET 100 mg + 25 mg Tabletten
- SINEMET 200 mg + 50 mg Tabletten mit veränderter Wirkstofffreisetzung, SINEMET 100 mg + 25 mg Tabletten mit veränderter Wirkstofffreisetzung
Warum wird Sinemet verwendet? Wofür ist das?
Sinemet Tabletten mit veränderter Wirkstofffreisetzung enthalten die Wirkstoffe Levodopa und Carbidopa und werden zur Behandlung der Parkinson-Krankheit und insbesondere zur Reduzierung von Komplikationen im fortgeschrittenen Stadium der Erkrankung, wie Muskelversteifung ("Off"-Phasen), bei Patienten mit bereits mit Kombinationen von Levodopa/Decarboxylase-Hemmern (z. B. Carbidopa) oder mit Levodopa allein behandelt werden, bei denen Schwankungen der motorischen Symptome aufgetreten sind. Die Schwankungen der motorischen Symptome zeigen sich im Tagesverlauf durch die Verbesserung der motorischen Symptome im Zusammenhang mit der Behandlung (Phase "on") und das Wiederauftreten der Symptome, wenn die Wirkung der Therapie endet (Phase "off" ").
Es liegen nur begrenzte Daten zur Anwendung von Sinemet Tabletten mit veränderter Wirkstofffreisetzung bei Patienten vor, die zuvor nicht mit Levodopa-reinen Arzneimitteln behandelt wurden.
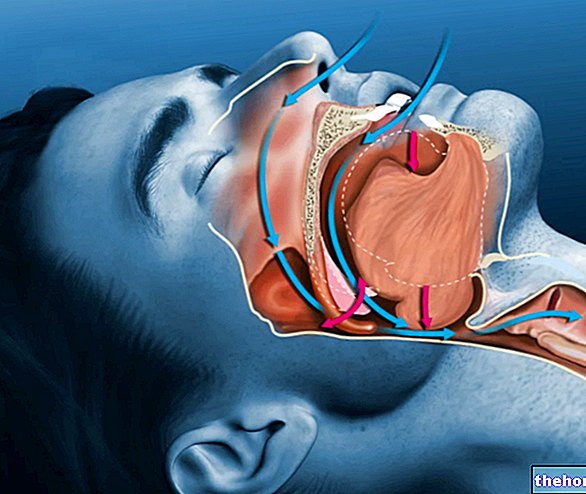
Was ist die Parkinson-Krankheit?
Es ist eine Pathologie des Nervensystems, die Zittern, Steifheit, Verlangsamung der Bewegung und Schwierigkeiten beim Gehen verursacht; es wird durch niedrige Dopaminspiegel verursacht, eine Substanz, die normalerweise vom Gehirn produziert wird und eine wesentliche Rolle bei der Kontrolle der Muskelbewegungen spielt.
Kontraindikationen Wenn Sinemet nicht verwendet werden sollte
Sinemet® darf nicht eingenommen werden
- wenn Sie allergisch gegen die Wirkstoffe Levodopa und Carbidopa oder einen der sonstigen Bestandteile dieses Arzneimittels sind (aufgeführt in Abschnitt 6);
- wenn Sie keine Arzneimittel anwenden können, die das Zentralnervensystem beeinflussen (Sympathomimetika);
- wenn Sie an erhöhtem Augeninnendruck (Engwinkelglaukom) leiden;
- wenn Sie kürzlich an Herzproblemen (akute Phase des Myokardinfarkts) gelitten haben;
- wenn Sie Arzneimittel zur Behandlung der Parkinson-Krankheit einnehmen, die Monoaminoxidase-Typ-A-(MAOA)-Hemmer genannt werden, mit Ausnahme niedriger Dosen von selektiven Monoaminoxidase-Typ-B-Hemmern (siehe Abschnitte „Warnhinweise und Vorsichtsmaßnahmen“ und „Einnahme von Sinemet zusammen mit anderen Arzneimitteln“). Beenden Sie die Einnahme von MAO-A-Hemmern mindestens zwei Wochen vor Beginn der Behandlung mit Sinemet;
- wenn Sie nicht diagnostizierte verdächtige Hautläsionen haben;
- wenn Sie Hautkrebs (Melanom) haben oder hatten;
- wenn Sie unter 18 Jahre alt sind;
- wenn Sie schwanger sind oder stillen (siehe Abschnitt „Schwangerschaft und Stillzeit“).
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Sinemet® beachten?
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Sinemet einnehmen. Wenn Sie während der Einnahme von Sinemet ungewöhnliche Anzeichen oder Symptome bemerken, wenden Sie sich sofort an Ihren Arzt oder Apotheker.
Informieren Sie Ihren Arzt, bevor Sie dieses Arzneimittel anwenden:
- wenn Sie derzeit Arzneimittel nur mit Levodopa einnehmen. In diesem Fall müssen Sie mindestens 8 Stunden warten, bevor Sie mit der Einnahme von Sinemet Tabletten mit veränderter Wirkstofffreisetzung beginnen (mindestens 12 Stunden, wenn Sie Levodopa mit verzögerter Wirkstofffreisetzung einnehmen);
- wenn Sie derzeit die empfohlene Dosis eines selektiven Monoaminoxidase-Typ-B-Hemmers zur Behandlung der Parkinson-Krankheit einnehmen (z. B. Selegilinhydrochlorid) (siehe Abschnitt 2 „Einnahme von Sinemet mit anderen Arzneimitteln“). Da Selegilin die Wirkung von Levodopa verstärkt, können Nebenwirkungen von Levodopa verstärkt werden, insbesondere wenn Sie eine hochdosierte Levodopa-Therapie erhalten. Er wird vom Arzt überwacht. Die Zugabe von Selegilin zur Levodopa-Therapie kann zu unwillkürlichen Bewegungen und/oder Agitiertheit führen Diese Nebenwirkungen verschwinden nach einer Verringerung der Levodopa-Dosis;
- wenn Sie morgens unter Veränderungen der Muskelbewegung leiden (morgendliche Dyskinesie). Die therapeutische Wirkung von Sinemet-Tabletten mit veränderter Wirkstofffreisetzung kann in diesem Fall im Vergleich zur Formulierung von Sinemet-Tabletten verlangsamt sein. Die Inzidenz von Dyskinesien bei Patienten mit schweren Formen der motorischen Fluktuation ist während der Behandlung mit Sinemet-Tabletten mit veränderter Wirkstofffreisetzung etwas höher zu Sinemet-Tabletten (16,5% vs. 12,2%). Da die Funktion von Carbidopa darin besteht, sicherzustellen, dass eine höhere Levodopa-Konzentration das Gehirn erreicht, sodass mehr Dopamin gebildet wird, können Sie Dyskinesie entwickeln, wenn Sie Arzneimittel, die nur Levodopa enthalten, zusammen mit Sinemet einnehmen. In solchen Fällen kann eine Dosisreduktion erforderlich sein;
- wenn Sie in der Vergangenheit nach einer Behandlung mit Levodopa allein oder in Kombination mit Decarboxylasehemmern (z. B. Carbidopa) an schweren unwillkürlichen Bewegungen oder psychotischen Episoden gelitten haben. Wie Levodopa kann Sinemet unwillkürliche Bewegungen und psychische Störungen verursachen, daher wird Ihr Arzt Sie während der Anfangsphase der Behandlung mit Sinemet überwachen. Es wird angenommen, dass diese Reaktionen auf einen Anstieg von Dopamin im Gehirn (eine vom Körper produzierte Substanz, die die Funktion eines Botenstoffs in den Zellen des Nervensystems ausübt) nach der Verabreichung von Levodopa zurückzuführen ist; folglich kann die Anwendung von Sinemet ein Rückfall. In diesen Fällen kann eine Dosisreduktion erforderlich sein;
- Sie werden engmaschig auf die mögliche Entwicklung von Depressionen und begleitenden suizidalen Tendenzen überwacht, insbesondere wenn Sie in der Vergangenheit psychotische Episoden hatten oder hatten;
- wenn Sie an einer schweren Herz-Kreislauf-Erkrankung leiden;
- wenn Sie eine schwere Lungenerkrankung oder Asthma bronchiale haben;
- wenn Sie an Nieren- oder Leberproblemen leiden oder wenn Sie Probleme mit dem endokrinen System haben (ein System, das eine Reihe von Drüsen umfasst, die Hormone in den Blutkreislauf freisetzen);
- wenn Sie in der Vergangenheit an einer Verletzung der Magen- oder Darmwand gelitten haben (peptisches Ulkus);
- wenn Sie in der Vergangenheit an Krämpfen gelitten haben;
- wenn Sie vor kurzem einen Herzinfarkt (Myokardinfarkt) hatten und immer noch Herzrhythmusstörungen (atriale, nodale oder ventrikuläre Arrhythmien) haben. In diesem Fall muss Ihr Arzt Ihre Herzfunktion während der anfänglichen Dosisanpassungsphase sehr sorgfältig überwachen;
- wenn Sie Augenerkrankungen haben, die durch Veränderungen des Augeninnendrucks verursacht werden (chronisches Offenwinkelglaukom). Sie können Sinemet trotzdem einnehmen, sofern der Augeninnendruck gut ausgeglichen ist und der Arzt während der Therapie die Schwankungen desselben sorgfältig überwacht;
- wenn Sie die Einnahme von Arzneimitteln zur Behandlung der Parkinson-Krankheit abrupt abbrechen; dies kann ähnliche Symptome wie das maligne neuroleptische Syndrom verursachen, die sich in Muskelsteifheit und erhöhter Körpertemperatur, mentalen Veränderungen und erhöhtem Serum-Kreatinkinase (ein im Blut vorhandenes Enzym) äußern engmaschig, wenn Ihre Carbidopa-Levodopa-Dosis abrupt reduziert oder beendet wird, insbesondere wenn Sie Antipsychotika einnehmen;
- wenn Sie an einer Erbkrankheit leiden, die durch plötzliche unwillkürliche und unkoordinierte Bewegungen gekennzeichnet ist (Huntington-Chorea). In diesem Fall wird Sinemet nicht empfohlen.
Die Behandlung mit Levodopa-Carbidopa, den in Sinemet enthaltenen Wirkstoffen, wurde mit Schläfrigkeit und Episoden plötzlicher Schlafanfälle in Verbindung gebracht. Es wurde sehr selten über plötzliche Schlafanfälle während der täglichen Aktivität berichtet, in einigen Fällen ohne Bewusstsein und ohne Warnzeichen.Wenn Sie Schläfrigkeit und/oder eine Episode von plötzlichem Einschlafen verspüren, führen Sie kein Fahrzeug und bedienen Sie keine Maschinen. Ziehen Sie eine Dosisreduktion in Betracht oder Abbruch der Therapie.
Während der Therapiezeit sind regelmäßige Blutuntersuchungen sowie Leber-, Nieren- und Herz-Kreislauf-Funktionstests ratsam.
Patienten und medizinischem Fachpersonal wird empfohlen, bei der Anwendung von Sinemet für jede Indikation eine häufige und regelmäßige Überwachung zur Vorbeugung von Hautkrebs (Melanom) durchzuführen. Einige Studien haben gezeigt, dass Parkinson-Patienten ein höheres Melanomrisiko haben (2- bis etwa 6-mal höher) als die Allgemeinbevölkerung. Es ist nicht klar, ob das beobachtete erhöhte Risiko auf die Parkinson-Krankheit oder andere Faktoren zurückzuführen ist, wie die Einnahme von Medikamenten zur Behandlung der Krankheit selbst. Aus diesen Gründen wird empfohlen, regelmäßige Hautuntersuchungen durch qualifiziertes Personal (z . ).
Informieren Sie Ihren Arzt, wenn Sie oder jemand in Ihrer Familie/Ihrem Betreuer bemerken, dass Sie einen für Sie ungewöhnlichen Drang oder Wunsch entwickeln, sich auf eine Weise zu verhalten, die für Sie ungewöhnlich ist, und Sie dem Drang oder der Versuchung nicht widerstehen können, bestimmte Aktivitäten auszuführen, die sich selbst oder anderen schaden könnten werden Impulskontrollstörungen genannt und können Spielsucht, übermäßiges Essen oder Geldausgeben, ein abnormales, übertriebenes sexuelles Verlangen oder eine Zunahme sexueller Gedanken oder Gefühle umfassen. Der Arzt kann es für erforderlich halten, die Behandlung zu überprüfen, zu ändern oder abzubrechen.
Während der Behandlung mit Sinemet können sich die Ergebnisse einiger Labortests ändern:
- Anstieg bestimmter Substanzen im Blut (Lebertransaminasen, LDH, Bilirubin, alkalische Phosphatase, Stickstoff, Kreatinin und Harnsäure);
- positiver Coombs-Test (ein Test zum Nachweis bestimmter Arten von Antikörpern im Blut);
- falsch positiv für Ketonkörper im Urin, wenn ein Streifentest zur Bestimmung der Ketonurie verwendet wird. Diese Reaktion wird durch das Sieden der Urinprobe nicht verändert;
- falsch negativ bei der Untersuchung der Glykosurie mit den Glucose-Oxidase-Methoden.
Wenn Sie während der Einnahme von SINEMET ungewöhnliche Anzeichen oder Symptome bemerken, wenden Sie sich sofort an Ihren Arzt oder Apotheker.
Kinder und Jugendliche
Die Anwendung von Sinemet bei Kindern und Jugendlichen unter 18 Jahren wird aufgrund fehlender Daten zur Sicherheit und Wirksamkeit bei Säuglingen und Kindern nicht empfohlen.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Sinemet® beeinflussen?
Einnahme von Sinemet® zusammen mit anderen Arzneimitteln
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen, kürzlich andere Arzneimittel eingenommen haben oder beabsichtigen andere Arzneimittel einzunehmen.
Sie sollten besonders vorsichtig sein, wenn Sie Sinemet zusammen mit den folgenden Arzneimitteln einnehmen:
- blutdrucksenkende Arzneimittel zur Behandlung von Bluthochdruck: Die gleichzeitige Anwendung mit Sinemet kann nach einem plötzlichen Übergang vom Sitzen oder Liegen zum Stehen zu einem Blutdruckabfall führen (symptomatische posturale Hypotonie). Bevor Sie mit der Behandlung mit Sinemet beginnen, wenden Sie sich an Ihren Arzt, um eine mögliche Dosisanpassung;
- Arzneimittel zur Behandlung von Depressionen: Nebenwirkungen, einschließlich Bluthochdruck und unwillkürliche Muskelbewegungen (Dyskinesie), wurden bei gleichzeitiger Behandlung mit Sinemet und einigen Arzneimitteln zur Behandlung von Depressionen (trizyklische Antidepressiva) selten beobachtet; Wenn Sie Monoaminoxidase-Hemmer einnehmen, lesen Sie den Abschnitt „Sinemet darf nicht eingenommen werden“;
- Arzneimittel, die auf das Zentralnervensystem wirken (Anticholinergika): Diese Arzneimittel können die Resorption von Sinemet und damit das Ansprechen auf die Therapie beeinträchtigen;
- Eisenhaltige Arzneimittel (zB Eisensulfat oder Eisengluconat): bewirken eine Verringerung der Resorption und Wirksamkeit von Carbidopa und/oder Levodopa (den Wirkstoffen von Sinemet);
- Dopamin-Rezeptor-Antagonisten Arzneimittel wie Phenothiazine, Butyrophenone und Risperidon zur Behandlung von Psychosen und Isoniazid zur Behandlung von Tuberkulose: Die therapeutische Wirkung von Levodopa kann durch diese Arzneimittel verringert werden;
- Arzneimittel wie Phenytoin zur Behandlung von Epilepsie und Papaverin zur Muskelentspannung: Die therapeutische Wirkung von Levodopa kann durch diese Arzneimittel aufgehoben werden. Wenn Sie gleichzeitig mit Sinemet Antipsychotika, Phenytoin oder Papaverin einnehmen, wird Ihr Arzt Sie in Bezug auf „Verlust des therapeutischen Ansprechens“ engmaschig überwachen.
- Arzneimittel, die Wirkstoffe enthalten, die die Dopaminspeicher im Körper reduzieren, wie Reserpin, zur Behandlung von Bluthochdruck und Tetrabenazin, zur Behandlung von Krämpfen und unkontrollierbaren Muskelbewegungen, oder zusammen mit anderen Arzneimitteln, von denen bekannt ist, dass sie die Monoaminspeicher leeren, wie Adrenalin und Noradrenalin: Die Anwendung von Sinemet wird mit diesen Arzneimitteln nicht empfohlen;
- Arzneimittel, die Selegilin enthalten, zur Behandlung der Parkinson-Krankheit, Depression und seniler Demenz: Eine gleichzeitige Behandlung mit Selegilin und Carbidopa-Levodopa kann zu einem schweren Blutdruckabfall führen, der nicht auf Carbidopalevodopa allein zurückzuführen ist (siehe Abschnitt 2 „Warnhinweise und Vorsichtsmaßnahmen“ );
- Antazida zur Linderung von Sodbrennen (Hauptsymptom der gastroösophagealen Refluxkrankheit): Die Auswirkungen einer gleichzeitigen Anwendung dieser Arzneimittel und Sinemet auf die Resorption und Wirksamkeit von Levodopa sind nicht bekannt.
Einnahme von Sinemet zusammen mit Nahrungsmitteln und Getränken
Die Aufnahme von Sinemet kann bei einigen Patienten, die hohe Proteinmengen mit der Nahrung aufnehmen, eingeschränkt sein. Fragen Sie Ihren Arzt, wenn Ihre Nahrung hohe Proteinmengen enthält.
Warnungen Es ist wichtig zu wissen, dass:
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat. Es liegen keine ausreichenden Daten zur Anwendung von Sinemet während der Schwangerschaft vor. Da Sinemet in Tierstudien schädlich war (Skelett- und viszerale Fehlbildungen bei Kaninchen) und nicht bekannt ist, ob Carbidopa und Levodopa in die Muttermilch übergehen, dürfen Sie Sinemet nicht anwenden, wenn Sie schwanger sind oder Stillen.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Die Behandlung mit Sinemet kann Schläfrigkeit (übermäßige Taubheit) und plötzliche Schlafanfälle verursachen. Aus diesem Grund muss er das Führen eines Fahrzeugs und jede Tätigkeit unterlassen, bei der eine eingeschränkte Aufmerksamkeit sich selbst oder andere dem Risiko schwerer Verletzungen oder des Todes aussetzen könnte (z. B. das Bedienen von Maschinen), bis diese wiederkehrenden Episoden und die Schläfrigkeit nicht abgeklungen sind.
Dosierung und Art der Anwendung Wie ist Sinemet anzuwenden: Dosierung
Nehmen Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker ein. Fragen Sie im Zweifelsfall Ihren Arzt oder Apotheker.
Schlucken Sie die Sinemet-Tablette im Ganzen, kauen Sie sie nicht, zerdrücken Sie sie nicht, um die Eigenschaften der Tablette mit veränderter Wirkstofffreisetzung nicht zu beeinträchtigen. Informieren Sie Ihren Arzt während der anfänglichen Dosisanpassungsphase, wenn bei Ihnen Übelkeit oder abnormale unwillkürliche Bewegungen (einschließlich Dyskinesie, Chorea und Dystonie) auftreten oder sich verschlimmern. Während der Behandlung mit Sinemet können Sie weiterhin Arzneimittel zur Behandlung der Parkinson-Krankheit einnehmen, mit Ausnahme von Levodopa allein, obwohl die Dosis möglicherweise angepasst werden muss. Sie können Sinemet zusammen mit pyridoxinhaltigen Vitaminpräparaten (zB Vitamin B6) einnehmen, da Carbidopa die antagonistische Wirkung von Pyridoxin auf Levodopa verhindert.
Anfangsdosierung
Wenn Sie derzeit nur mit Levodopa behandelt werden
Sinemet 100 mg + 25 mg mit veränderter Wirkstofffreisetzung ist in erster Linie für die Anwendung bei Patienten mit früher Erkrankung, die zuvor nicht mit Levodopa behandelt wurden, oder zur Erleichterung der Dosisanpassung bei Patienten, die Sinemet 200 mg + 50 mg mit veränderter Wirkstofffreisetzung einnehmen, indiziert.
Gegebenenfalls kann eine Levodopa-Therapie auch mit Sinemet 200 mg + 50 mg mit veränderter Wirkstofffreisetzung eingeleitet werden. Die Anfangsdosis sollte 600 mg Levodopa pro Tag nicht überschreiten und sollte nicht in Abständen von weniger als 6 Stunden eingenommen werden.
Sinemet 200 mg + 50 mg mit veränderter Wirkstofffreisetzung: Die empfohlene Dosis beträgt zwei- oder dreimal täglich eine Tablette.
Sinemet 100 mg + 25 mg mit veränderter Wirkstofffreisetzung: Die empfohlene Dosis beträgt zweimal täglich eine Tablette. Wenn Ihr Arzt dies für erforderlich hält, kann die Dosis von einer auf vier Tabletten zweimal täglich erhöht werden.
Wenn Sie derzeit mit der herkömmlichen Kombination Levodopa/Decarboxylase-Hemmer behandelt werden
Sie müssen eine Dosis Sinemet 200 mg + 50 mg mit veränderter Wirkstofffreisetzung einnehmen, um etwa 10 % mehr Levodopa als zuvor eingenommen zu erhalten. Diese Dosis kann je nach klinischem Ansprechen um bis zu 30 % mehr Levodopa pro Tag erhöht werden. Halten Sie während der wachen Stunden zwischen den Dosen von Sinemet 200 mg + 50 mg mit veränderter Wirkstofffreisetzung einen Abstand von 4-8 Stunden ein.
Nachfolgend finden Sie eine Tabelle, die Ihnen bei der Umstellung von herkömmlichen Levodopa/Carbidopa-Kombinationen auf Sinemet 200 mg + 50 mg mit veränderter Wirkstofffreisetzung hilft.
* Dosierungsintervalle, die nicht in der Tabelle aufgeführt sind, siehe Abschnitt 4.2 – Anfangsdosis – Patienten unter konventioneller Levodopa/Decarboxylase-Inhibitor-Kombination.
SINEMET 100 mg + 25 mg mit veränderter Wirkstofffreisetzung ist erhältlich, um die Titration von 100 mg zu erleichtern und das oben angegebene Dosierungsschema einzuhalten.
Wenn Sie derzeit eine alleinige Levodopa-Therapie erhalten
Sie müssen die Behandlung mit Levodopa mindestens 8 Stunden vor Beginn der Behandlung mit Sinemet 200 mg + 50 mg mit veränderter Wirkstofffreisetzung beenden. Die empfohlene Anfangsdosis für Patienten mit leichter bis mittelschwerer Parkinson-Krankheit beträgt zweimal täglich eine Sinemet 200 mg + 50 mg Tablette mit veränderter Wirkstofffreisetzung.
Bestimmung der optimalen Dosis
Sobald die Therapie begonnen wurde, können die Dosis und die Zeitintervalle für die Verabreichung basierend auf dem therapeutischen Ansprechen geändert werden. Die meisten Patienten wurden mit 2-8 Sinemet 200 mg + 50 mg Tabletten mit veränderter Wirkstofffreisetzung pro Tag in Abständen von 4-12 Stunden über den Tag hinweg angemessen behandelt. Therapien mit höherer Dosis (bis zu 12 Tabletten) in kürzeren Abständen (weniger als 4 Stunden) wurden evaluiert, werden jedoch nicht allgemein empfohlen. Wenn die Dosis von Sinemet 200 mg + 50 mg mit veränderter Wirkstofffreisetzung in Abständen von weniger als 4 Stunden verabreicht oder in ungleiche Dosen aufgeteilt wird, wird empfohlen, die niedrigere Dosis am Ende des Tages einzunehmen. Im Vergleich zum normalerweise erhaltenen Ansprechen kann die pharmakologische Wirkung bei einigen Patienten nach Einnahme der ersten Tagesdosis von Sinemet Tabletten mit veränderter Wirkstofffreisetzung sogar mit einer Verzögerung von einer Stunde auftreten.
Dosisanpassungen sollten in Abständen von mindestens drei Tagen vorgenommen werden.
Erhaltungstherapie
Aufgrund der Natur der Parkinson-Krankheit wird Ihr Arzt Sie regelmäßig untersuchen und gegebenenfalls die Dosis anpassen.
Begleitbehandlung mit anderen Antiparkinson-Arzneimitteln
Die gleichzeitige Behandlung mit Sinemet mit Anticholinergika, Dopaminagonisten und Amantadin kann eine Dosisanpassung erforderlich machen.
Überdosierung Was ist zu tun, wenn Sie zu viel Sinemet® eingenommen haben?
Wenn Sie eine größere Menge von Sinemet eingenommen haben, als Sie sollten
Im Falle einer versehentlichen Einnahme / Einnahme einer Überdosierung von Sinemet benachrichtigen Sie sofort Ihren Arzt oder Apotheker oder wenden Sie sich an das nächste Krankenhaus.
Behandlungsmethode bei Überdosierung von Sinemet
Die Behandlung im Falle einer Überdosierung von Sinemet ist dieselbe wie bei einer Levodopa-Überdosierung; Pyridoxin hat jedoch keine Wirkung beim "Aufheben" der Wirkung von Sinemet.
Es sollte eine elektrokardiographische Untersuchung durchgeführt und der Patient sorgfältig auf die mögliche Entwicklung von Herzrhythmusstörungen (Arrhythmien) überwacht und gegebenenfalls eine geeignete „antiarrhythmische Therapie“ durchgeführt werden haben möglicherweise andere Arzneimittel zusammen mit Sinemet eingenommen. Bisher liegen keine Erfahrungen zur Wirksamkeit der Dialyse bei Überdosierung vor.
Wenn Sie die Einnahme von Sinemet vergessen haben
Nehmen Sie nicht die doppelte Dosis ein, wenn Sie die vergessene Tablette vergessen haben.
Wenn Sie die Einnahme einer Tablette vergessen haben, nehmen Sie diese ein, sobald Sie sich daran erinnern. Wenn es fast Zeit für die nächste Tablette ist, nehmen Sie die vergessene Tablette nicht ein, sondern fahren Sie mit dem üblichen Dosierungsschema fort.
Wenn Sie die Einnahme von Sinemet® abbrechen
Wenn Ihre Sinemet-Dosis abrupt reduziert oder beendet wird, wird Ihr Arzt Sie regelmäßig überwachen, insbesondere wenn Sie Antipsychotika einnehmen.
Wenn Sie sich einer Operation unterziehen müssen, die eine Vollnarkose erfordert, beenden Sie die Einnahme von Sinemet, bis Sie wieder eine orale Therapie einnehmen können.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
Nebenwirkungen Was sind die Nebenwirkungen von Sinemet
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
In Studien an Patienten mit mäßigen oder starken Schwankungen der motorischen Symptome verursachte Sinemet keine Nebenwirkungen der Formulierung mit veränderter Wirkstofffreisetzung.
Die am häufigsten berichtete Nebenwirkung war Dyskinesie, die sich in abnormalen unwillkürlichen Bewegungen äußerte.
Andere Nebenwirkungen, die in klinischen Studien oder während der tatsächlichen Vermarktung von Sinemet berichtet wurden, sind:
- zufällige und kontinuierliche Bewegungen (Choreiformen), abnormale Muskelkontraktionen (Dystonie) und andere unwillkürliche Bewegungen (Dyskinesie);
- Übelkeit (Übelkeit);
- Veränderungen der Muskelkontraktion (Muskelkrämpfe) und erzwungenes und unwillkürliches Schließen der Augenlider (Blepharospasmus). Das Vorhandensein dieser Symptome deutet auf eine Dosisreduktion hin.
Andere Nebenwirkungen, die in klinischen Studien oder während der tatsächlichen Vermarktung von Sinemet berichtet wurden, sind:
- Brechreiz;
- Halluzinationen, Verwirrung, Schwindel;
- zufällige, kontinuierliche und unwillkürliche Bewegungen (Chorea);
- trockener Mund;
- Störungen der Traumaktivität (Traumveränderung);
- abnorme Muskelkontraktionen (Dystonie);
- Schläfrigkeit (übermäßige Taubheit), einschließlich sehr selten übermäßiger Tagesschläfrigkeit und Episoden von plötzlichem Einschlafen, Schlaflosigkeit;
- Depression;
- verminderte Muskelkraft (Asthenie);
- Er würgte;
- Anorexie.
- Brustschmerzen;
- Bewusstlosigkeit (Synkope);
- Herzklopfen, haltungsbedingter Druckabfall (orthostatische Hypotonie);
- Verstopfung, Durchfall, Verdauungsstörungen (Dyspepsie), Magen-Darm-Schmerzen, dunkler Speichel;
- allergische Erscheinungen wie Entzündungsreaktionen und Hautschwellungen (Angioödem), Nesselsucht, Juckreiz;
- Gewichtsverlust;
- malignes neuroleptisches Syndrom, das sich durch Muskelsteifheit, erhöhte Körpertemperatur und psychische Störungen manifestiert (siehe Abschnitt „Warnhinweise und Vorsichtsmaßnahmen“);
- Unruhe, Angst, verminderte geistige Schärfe;
- Veränderungen der Empfindung in den Gliedmaßen oder anderen Körperteilen (Parästhesie);
- Orientierungslosigkeit;
- Müdigkeit;
- Kopfschmerzen;
- Störungen durch Ursachen außerhalb des Nervensystems (extrapyramidale Störungen) und der Bewegung, Leichtigkeit beim Fallen, Gangwechsel;
- Muskelkrämpfe;
- plötzliche Veränderungen der Symptome der Parkinson-Krankheit ("An-Aus"-Symptome);
- psychotische Episoden einschließlich Delirium und von der Realität abweichende Gedankenformen (paranoide Vorstellung);
- Atemprobleme (Dyspnoe);
- Hitzewallungen, Haarausfall (Alopezie), Hautausschlag (Hautausschlag), dunkler Schweiß;
- verschwommene Sicht;
- dunkler Urin;
- Unfähigkeit, dem Drang oder der Versuchung zu widerstehen, Handlungen zu unternehmen, die sich selbst oder anderen schaden könnten, darunter: - starker Drang zu übermäßigem Glücksspiel trotz schwerwiegender persönlicher oder familiärer Konsequenzen; - verändertes oder verstärktes sexuelles Verlangen, das für Sie oder andere von erheblicher Bedeutung ist; - unkontrollierbare Einkäufe oder übermäßige Ausgaben; - zwanghaftes Essen (das Essen großer Nahrungsmengen in kurzer Zeit) oder Bulimie (das Essen von mehr Nahrung als normal und mehr als notwendig ist, um Ihren Hunger zu stillen).
Es wurden Anfälle beobachtet, jedoch ist nicht mit Sicherheit bewiesen, dass die Anfälle durch Sinemet verursacht werden.
Informieren Sie Ihren Arzt, wenn eines dieser Verhaltensweisen auftritt, damit er entscheiden kann, was zu tun ist, um die Symptome zu behandeln oder zu reduzieren.
Die Therapie mit Sinemet (und ähnlichen Medikamenten) kann bei einigen Labortests zu Veränderungen führen:
- Anstieg bestimmter Substanzen im Blut (Lebertransaminasen, LDH, Bilirubin, alkalische Phosphatase, Stickstoff, Kreatinin und Harnsäure);
- positiver Coombs-Test (ein Test zum Nachweis bestimmter Arten von Antikörpern im Blut);
- vermindertes Hämoglobin und Hämatokrit (was zu Anämie führen kann), erhöhter Blutzucker (Hyperglykämie) und weiße Blutkörperchen sowie Blut und Bakterien im Urin;
- falsch positiv für das Vorhandensein bestimmter Substanzen (Ketonkörper) im Urin, wenn ein Streifentest zur Bestimmung der Ketonurie verwendet wird. Diese Reaktion wird durch das Kochen der Urinprobe nicht verändert. Falsche Negativitätstests können auftreten, wenn Glukose-Oxidase-Methoden zum Nachweis von Glukose im Urin verwendet werden.
Andere Nebenwirkungen wurden während der Anwendung von Levodopa-haltigen Arzneimitteln oder mit Levodopa/Carbidopa-Kombinationsarzneimitteln beobachtet und es können potenzielle Nebenwirkungen von Sinemet auftreten:
- Herzkrankheit, erhöhter Blutdruck, Venenentzündung (Phlebitis);
- bitterer Mund, übermäßige Speichelproduktion (Sabbern), Schluckbeschwerden (Dysphagie), unwillkürliche Kontraktion der Kaumuskulatur, die zu übermäßigem Zähneputzen führt (Bruxismus), Schluckauf, Magen-Darm-Blutungen, Blähungen, Brennen in der Zunge, Entwicklung von Verletzungen der Darmwand (Zwölffingerdarmgeschwür);
- Abnahme der weißen Blutkörperchen (Leukopenie und Agranulozytose), der roten Blutkörperchen (hämolytische und nicht-hämolytische Anämie) und der Blutplättchen (Thrombozytopenie);
- Verlust der Muskelkoordination (Ataxie), Taubheitsgefühl, verstärktes Zittern der Hände, Zucken und Entspannen eines oder mehrerer Muskeln (Muskelkrämpfe), erzwungenes und unwillkürliches Schließen der Augenlider (Blepharospasmus), abnorme Kontraktionen der Kiefermuskulatur (Trismus), Aktivierung eines vorbestehenden Horner-Syndroms (eine Augenerkrankung), das mit dem Einsetzen einer Verletzung und Schwierigkeiten beim Bewegen der Augen auftritt;
- Euphorie, Demenz;
- Depression mit Suizidneigung;
- vermehrtes Schwitzen;
- Doppelbilder (Diplopie), erweiterte Pupillen, fixierte Augenposition (okulogyrische Krise);
- Harnverhalt, Harninkontinenz, dunkler Urin, anhaltende, abnorme und schmerzhafte Erektionen (Priapismus);
- Gewichtszunahme, Ödeme, Schwäche, Ohnmacht, Veränderung des normalen Tonfalls (Heiserkeit), Unwohlsein, Hitzegefühl, Erregungsgefühl, unregelmäßiger Atemrhythmus, Hauttumoren (malignes Melanom) (siehe Abschnitt 2 „Sinemet darf nicht eingenommen werden“), Henoch -Schönlein Purpura, die sich mit Gelenkverletzungen und Schmerzen manifestiert;
- Krampfanfälle, obwohl ein kausaler Zusammenhang mit Levodopa oder den Levodopa/Carbidopa-Kombinationen nicht nachgewiesen wurde.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker, einschließlich aller möglichen Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind. Sie können Nebenwirkungen auch direkt über das nationale Meldesystem unter https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse melden. Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
Ablauf und Aufbewahrung
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Bewahren Sie das Arzneimittel vor Licht geschützt auf.
Verwenden Sie dieses Arzneimittel nicht nach dem Verfallsdatum, das auf der Packung nach „EXP“ angegeben ist. Das Ablaufdatum bezieht sich auf den letzten Tag dieses Monats.
Das angegebene Verfallsdatum bezieht sich auf das Arzneimittel in intakter Verpackung, korrekt gelagert.
Entsorgen Sie Arzneimittel nicht im Abwasser oder Haushaltsabfall.
Fragen Sie Ihren Apotheker, wie Arzneimittel zu entsorgen sind, die Sie nicht mehr verwenden.
Dies trägt zum Schutz der Umwelt bei.
Zusammensetzung und Darreichungsform
Was Sinemet enthält
Die Wirkstoffe von Sinemet sind: Levodopa und Carbidopa.
Jede Sinemet 100 mg + 25 mg Tablette enthält: 100 mg Levodopa und 27 mg Carbidopahydrat, entsprechend 25 mg wasserfreiem Carbidopa.
Die sonstigen Bestandteile sind: Eisen(III)-oxid E172, Hydroxypropylcellulose, Copolymer von Polyvinylacetat mit Crotonsäure, Magnesiumstearat.
Jede Tablette Sinemet 200 mg + 50 mg enthält: 250 mg Levodopa und 54 mg Carbidopahydrat, entsprechend 50 mg wasserfreiem Carbidopa.
Die sonstigen Bestandteile sind: Eisenoxid rot E172, Hydroxypropylcellulose, Copolymer von Polyvinylacetat mit Crotonsäure, Magnesiumstearat, E104 Chinolingelb auf hydratisiertem Aluminium.
Beschreibung wie Sinemet aussieht und Inhalt der Packung
Sinemet ist in Tablettenform erhältlich. Die Tabletten sind in Aluminium-/Aluminium-Blisterpackungen verpackt.
Jede Blisterpackung Sinemet 200 mg + 50 mg enthält 30 Tabletten mit veränderter Wirkstofffreisetzung.
Jede Blisterpackung Sinemet 100 mg + 25 mg enthält 50 Tabletten mit veränderter Wirkstofffreisetzung.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu haben, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS
SINEMET MODIFIZIERTE FREIGABETABLETTEN
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
SINEMET 200 mg + 50 mg Tabletten mit veränderter Wirkstofffreisetzung
Eine Tablette enthält 200 mg Levodopa und 54 mg Carbidopahydrat (entsprechend 50 mg wasserfreiem Carbidopa).
SINEMET 100 mg + 25 mg Tabletten mit veränderter Wirkstofffreisetzung
Eine Tablette enthält 100 mg Levodopa und 27 mg Carbidopahydrat (entsprechend 25 mg wasserfreiem Carbidopa).
Die vollständige Auflistung der sonstigen Bestandteile finden Sie in Abschnitt 6.1.
03.0 DARREICHUNGSFORM
Tabletten mit veränderter Wirkstofffreisetzung.
04.0 KLINISCHE INFORMATIONEN
04.1 Anwendungsgebiete
SINEMET mit veränderter Wirkstofffreisetzung ist indiziert zur Behandlung der idiopathischen Parkinson-Krankheit und insbesondere zur Verkürzung der „Off-Phasen“ bei Patienten, die bereits mit Levodopa/Decarboxylase-Hemmern in Kombination oder mit Levodopa allein behandelt wurden und bei denen Schwankungen der motorischen Symptome aufgetreten sind.
Die Erfahrungen mit SINEMET mit veränderter Wirkstofffreisetzung bei Patienten, die zuvor nicht mit Levodopa behandelt wurden, sind begrenzt.
04.2 Dosierung und Art der Anwendung
SINEMET Tabletten mit veränderter Wirkstofffreisetzung enthalten Levodopa und Carbidopa im Verhältnis 4:1 (SINEMET 200 mg + 50 mg veränderte Wirkstofffreisetzung: Levodopa 200 mg / Carbidopa 50 mg pro Tablette, SINEMET 100 mg + 25 mg veränderte Wirkstofffreisetzung: Levodopa 100 mg / Carbidopa 25 mg pro Tablette).
Die Tagesdosis von SINEMET mit veränderter Wirkstofffreisetzung sollte durch „sorgfältige Titration“ bestimmt werden. Die Patienten sollten während der Dosisanpassungsphase überwacht werden; insbesondere sollte auf das Auftreten oder die Verschlechterung von Übelkeit oder abnormalen unwillkürlichen Bewegungen, einschließlich Dyskinesie, Chorea und Dystonie.
SINEMET mit veränderter Wirkstofffreisetzung kann nur als ganze Tabletten verabreicht werden. Die Tabletten dürfen nicht gekaut oder zerdrückt werden, um die Eigenschaften des Produkts mit veränderter Freisetzungscharakteristik nicht zu verändern. Während der Anwendung von SINEMET mit veränderter Wirkstofffreisetzung kann die Therapie mit Standard-Antiparkinson-Arzneimitteln (außer Levodopa allein) fortgesetzt werden, obwohl die Dosierung dieser Arzneimittel angepasst werden sollte. Da Carbidopa den Antagonismus von Pyridoxin auf die Wirkung von Levodopa verhindert, kann SINEMET mit veränderter Wirkstofffreisetzung Patienten mit zusätzlichen Dosen von Pyridoxin (Vitamin B6) verabreicht werden.
Anfangsdosierung
Patienten, die zuvor nicht mit Levodopa . behandelt wurden
SINEMET 100 mg + 25 mg mit veränderter Wirkstofffreisetzung ist in erster Linie für die Anwendung bei Patienten mit früher Erkrankung, die zuvor nicht mit Levodopa behandelt wurden, oder zur Erleichterung der notwendigen Titration bei Patienten indiziert, die SINEMET 200 mg + 50 mg veränderte Wirkstofffreisetzung erhalten Empfohlene Anfangsdosis von SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung ist eine Tablette zwei- oder dreimal täglich. Die empfohlene Anfangsdosis von SINEMET 100 mg + 25 mg mit veränderter Wirkstofffreisetzung beträgt zweimal täglich 1 Tablette. Für Patienten, die höhere Levodopa-Dosen benötigen, eine Tagesdosis von SINEMET 100 mg + 25 mg 1-4 Tabletten 2-mal täglich mit veränderter Wirkstofffreisetzung werden im Allgemeinen gut vertragen.
Gegebenenfalls kann eine Levodopa-Therapie auch mit SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung eingeleitet werden. Die Anfangsdosierung sollte 600 mg / Tag Levodopa nicht überschreiten und sollte nicht in Abständen von weniger als 6 Stunden verabreicht werden.
Patienten, die mit der konventionellen Kombination Levodopa/Decarboxylase-Hemmer behandelt werden
Der Patient sollte eine Dosis von 200 mg SINEMET + 50 mg mit veränderter Wirkstofffreisetzung erhalten, um ungefähr 10 % mehr Levodopa bereitzustellen, als der Patient zuvor eingenommen hat. Abhängig vom klinischen Ansprechen des Patienten kann es dennoch erforderlich sein, eine Dosierung zu erreichen, die bis zu 30 % mehr Levodopa pro Tag liefert (siehe unten – Titration). Das Intervall zwischen den Dosen von SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung sollte 4-8 Stunden während der wachen Stunden betragen.
Nachfolgend finden Sie eine Richttabelle für die Umstellung von herkömmlichen Levodopa/Carbidopa-Kombinationen auf SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung.
Leitfaden zur Einleitung der Umstellung von Levodopa/Decarboxylase-Hemmer auf SINEMET 200 mg + 50 mg
* Dosierungsintervalle, die nicht in der Tabelle aufgeführt sind, siehe Abschnitt 4.2 – Anfangsdosis – Patienten unter konventioneller Levodopa/Decarboxylase-Inhibitor-Kombination.
SINEMET 100 mg + 25 mg mit veränderter Wirkstofffreisetzung ist erhältlich, um die Titration von 100 mg zu erleichtern und das oben angegebene Dosierungsschema einzuhalten.
Patienten, die nur mit Levodopa behandelt werden
Levodopa sollte mindestens 8 Stunden vor Beginn der Behandlung mit SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung abgesetzt werden.Bei Patienten mit leichter oder mittelschwerer Erkrankung beträgt die empfohlene Anfangsdosis 1 SINEMET 200 mg + 50 Tablette zweimal täglich mg mit veränderter Wirkstofffreisetzung .
Titration
Sobald die Therapie begonnen wurde, können die Dosis und die Dosierungsintervalle entsprechend dem therapeutischen Ansprechen erhöht oder verringert werden. Die meisten Patienten wurden angemessen mit 2-8 Tabletten SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung behandelt, die täglich in Abständen von 4-12 Stunden verabreicht wurden. Therapien mit höheren Dosierungen (bis zu 12 Tabletten) in kürzeren Dosierungsintervallen (weniger als 4 Stunden) wurden untersucht, werden jedoch nicht allgemein empfohlen. Wenn die Dosierung von SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung in Abständen von weniger als 4 Stunden verabreicht oder in ungleiche Dosen aufgeteilt wird, wird empfohlen, die niedrigere Dosis am Ende des Tages einzunehmen. Im Vergleich zum normalerweise erhaltenen Ansprechen kann die pharmakologische Wirkung bei einigen Patienten nach Verabreichung der ersten Tagesdosis von SINEMET mit veränderter Wirkstofffreisetzung sogar mit einer Verzögerung von einer Stunde auftreten. Es wird empfohlen, die Dosis in Abständen von mindestens drei Tagen anzupassen.
Erhaltungstherapie
Da sich die Parkinson-Krankheit verschlimmert, werden regelmäßige klinische Untersuchungen empfohlen; außerdem kann eine Dosisanpassung von SINEMET mit veränderter Wirkstofffreisetzung erforderlich sein.
Begleitbehandlung mit anderen Antiparkinson-Arzneimitteln
Anticholinergika, Dopaminagonisten und Amantadin können gleichzeitig mit einer SINEMET-Therapie mit veränderter Wirkstofffreisetzung verabreicht werden. Wenn diese Arzneimittel zu einem bestehenden SINEMET-Behandlungsschema mit veränderter Wirkstofffreisetzung hinzugefügt werden, muss die Dosierung möglicherweise angepasst werden.
Abbruch der Therapie
Patienten sollten engmaschig überwacht werden, wenn eine abrupte Reduzierung oder ein Absetzen der SINEMET-Therapie mit veränderter Wirkstofffreisetzung erforderlich ist, insbesondere wenn der Patient mit Antipsychotika behandelt wird (siehe Abschnitt 4.4). Im Falle einer Vollnarkose sollte die Anwendung von SINEMET mit veränderter Wirkstofffreisetzung nur während des Zeitraums unterbrochen werden, in dem der Patient die orale Therapie nicht einnehmen kann.
Gebrauchsanweisung
SINEMET mit veränderter Wirkstofffreisetzung kann nur als ganze Tabletten verabreicht werden. Die Tabletten dürfen nicht gekaut oder zerdrückt werden.
04.3 Kontraindikationen
SINEMET mit veränderter Wirkstofffreisetzung ist bei Patienten mit Überempfindlichkeit gegen die Wirkstoffe (Levodopa und Carbidopa) oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile kontraindiziert.
SINEMET Tabletten sollten nicht verabreicht werden, wenn die Gabe von sympathomimetischen Aminen kontraindiziert ist. SINEMET mit veränderter Wirkstofffreisetzung ist beim Engwinkelglaukom und in der akuten Phase des Myokardinfarkts kontraindiziert.
Monoaminoxidase-Hemmer (außer niedrig dosierte selektive Monoaminoxidase-B-Hemmer – siehe Abschnitte 4.4 und 4.5) und SINEMET mit veränderter Wirkstofffreisetzung sollten nicht gleichzeitig angewendet werden. Die Therapie mit diesen Inhibitoren sollte mindestens zwei Wochen vor Beginn der Behandlung mit SINEMET mit veränderter Wirkstofffreisetzung abgebrochen werden.
Da Levodopa ein malignes Melanom aktivieren kann, sollte es nicht bei Patienten mit Verdacht auf Hautläsionen angewendet werden, deren Natur nicht geklärt ist, oder bei denen ein Melanom in der Vorgeschichte aufgetreten ist.
SINEMET mit veränderter Wirkstofffreisetzung sollte nicht bei schwangeren und stillenden Patientinnen unter 18 Jahren angewendet werden.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung
SINEMET Tabletten können Patienten verabreicht werden, die bereits mit Levodopa allein behandelt werden; Levodopa allein sollte jedoch mindestens 8 Stunden vor Beginn der Therapie mit SINEMET mit veränderter Wirkstofffreisetzung abgesetzt werden (mindestens 12 Stunden, wenn Levodopa mit verzögerter Wirkstofffreisetzung allein verabreicht wurde).
SINEMET mit veränderter Wirkstofffreisetzung kann gleichzeitig mit der empfohlenen Dosis eines MAO-Hemmers mit Selektivität für MAO Typ B zur Behandlung der Parkinson-Krankheit (z. B. Selegilinhydrochlorid) verabreicht werden (siehe Abschnitte 4.3 und 4.5).
Da Selegilin die Wirkung von Levodopa verstärkt, können Nebenwirkungen von Levodopa verstärkt werden, insbesondere wenn Patienten eine hochdosierte Levodopa-Therapie erhalten. Diese Patienten sollten beobachtet werden. Die Zugabe von Selegilin zur Levodopa-Therapie kann zu unwillkürlichen Bewegungen und/oder Agitiertheit führen Diese Nebenwirkungen verschwinden nach einer Verringerung der Levodopa-Dosis.
Basierend auf dem pharmakokinetischen Profil von SINEMET mit veränderter Wirkstofffreisetzung kann der Wirkungseintritt bei Patienten mit morgendlicher Dyskinesie im Vergleich zur Standardformulierung von SINEMET-Tabletten verlangsamt sein. Bei Patienten mit schweren fluktuierenden motorischen Symptomen ist die Inzidenz von Dyskinesien während der Behandlung mit SINEMET mit veränderter Wirkstofffreisetzung geringfügig höher als mit SINEMET-Tabletten (16,5 % gegenüber 12,2 %). Bei Patienten, die mit Levodopa allein behandelt werden, kann eine Dyskinesie auftreten, die eine Dosisreduktion erforderlich machen kann Wie Levodopa kann SINEMET mit veränderter Wirkstofffreisetzung unwillkürliche Bewegungen und psychische Störungen verursachen in Kombination mit Decarboxylase-Hemmern zu Beginn der Therapie mit SINEMET mit veränderter Wirkstofffreisetzung beobachtet werden.Diese Reaktionen werden auf einen Anstieg des Gehirndopamins nach der Verabreichung von Levodopa zurückgeführt Die Verabreichung von SINEMET mit veränderter Wirkstofffreisetzung kann zu einem Rückfall führen. In diesen Fällen kann eine Dosisreduktion erforderlich sein. Alle Patienten sollten sorgfältig auf die Entwicklung von Depressionen und begleitenden Suizidalitäten überwacht werden. Patienten mit vergangenen oder anhaltenden psychotischen Episoden sollten mit Vorsicht behandelt werden.
SINEMET mit veränderter Wirkstofffreisetzung sollte bei Patienten mit schwerer Herz-Kreislauf- oder Lungenerkrankung, Asthma bronchiale, Nieren-, Leber- oder endokriner Erkrankung oder mit Magengeschwüren oder Krampfanfällen in der Vorgeschichte mit Vorsicht angewendet werden Myokardinfarkt in der Anamnese mit verbleibenden atrialen, nodalen oder ventrikulären Arrhythmien. Bei diesen Patienten sollte die Herzfunktion während der anfänglichen Dosisanpassungsphase besonders sorgfältig überwacht werden. Patienten mit chronischem Offenwinkelglaukom können mit SINEMET mit veränderter Wirkstofffreisetzung mit Vorsicht behandelt werden dass der Augeninnendruck gut kompensiert wird und der Patient während der Therapie sorgfältig auf Veränderungen des Augeninnendrucks überwacht wird. exolar, erhöhte Körpertemperatur, mentale Veränderungen, Anstieg der Serum-Kreatinin-Phosphokinase. Daher sollten Patienten engmaschig überwacht werden, wenn die Dosis von Carbidopa-Levodopa-Kombinationen abrupt reduziert oder abgesetzt wird, insbesondere wenn sie Neuroleptika einnehmen. SINEMET mit veränderter Wirkstofffreisetzung wird nicht zur Behandlung von iatrogenen extrapyramidalen Reaktionen und zur Behandlung von Chorea Huntington empfohlen.
Die Behandlung mit Levodopa-Carbidopa wurde mit Schläfrigkeit und Episoden von plötzlichem Einschlafen in Verbindung gebracht.
Plötzliche Schlafanfälle während der täglichen Aktivität wurden sehr selten berichtet, in einigen Fällen ohne Bewusstsein und ohne Warnzeichen. Patienten, die SINEMET mit veränderter Wirkstofffreisetzung erhalten, sollten über diese Vorkommnisse informiert und angewiesen werden, beim Autofahren oder Autofahren vorsichtig zu sein. Patienten, bei denen Schläfrigkeit und/oder eine plötzliche Schlafepisode aufgetreten sind, sollten auf das Führen von Fahrzeugen und das Bedienen von Maschinen verzichten.Außerdem kann eine Dosisreduktion oder ein Absetzen der Therapie erwogen werden.
Während der Therapiedauer werden regelmäßige Kontrollen der Leber-, Blutbildungs-, Herz-Kreislauf- und Nierenfunktion empfohlen.
Melanom: Epidemiologische Studien haben gezeigt, dass Patienten mit Parkinson-Krankheit ein höheres Melanomrisiko haben (2- bis etwa 6-mal höher) als die Allgemeinbevölkerung. Es ist unklar, ob das beobachtete erhöhte Risiko auf die Parkinson-Krankheit oder auf andere Faktoren, wie die Anwendung von Arzneimitteln zur Behandlung der Krankheit, zurückzuführen ist.
Aus den oben genannten Gründen wird empfohlen, dass Patienten und medizinisches Fachpersonal bei der Anwendung von Sinemet für jede Indikation häufig und regelmäßig zur Melanomprävention überwacht werden.
Idealerweise sollten regelmäßige Hautuntersuchungen von qualifiziertem Personal (zB Dermatologen) durchgeführt werden.
Impulskontrollstörungen
Die Patienten sollten regelmäßig auf die Entwicklung von Impulskontrollstörungen überwacht werden.
Patienten und Pflegepersonal sollten sich bewusst sein, dass bei Patienten, die mit Dopaminagonisten und/oder anderen dopaminergen Behandlungen mit Levodopa einschließlich SINEMET mit veränderter Wirkstofffreisetzung Wenn solche Symptome auftreten, wird eine Neubewertung der Behandlung empfohlen.
Die Sicherheit und Wirksamkeit von SINEMET mit veränderter Wirkstofffreisetzung wurde bei Säuglingen und Kindern nicht nachgewiesen, daher ist die Anwendung bei Patienten unter 18 Jahren kontraindiziert (siehe Abschnitt 4.3).
Labortest
Bei Präparaten auf Basis von Levodopa / Carbidopa und damit bei modifizierter Freisetzung von SINEMET sind folgende Labortestveränderungen aufgetreten: erhöhte Leberfunktionsindizes wie alkalische Phosphatase, SGOT, SGPT, LDH, Bilirubin, Azotämie und positiver Coombs-Test. Carbidopa / Levodopa-Kombinationen können falsch positive Ketonkörper im Urin verursachen, wenn ein Ketonurie-Test verwendet wird. Diese Reaktion wird durch Kochen der Urinprobe nicht verändert. Bei der Messung von Glukosurie mit auf Glukoseoxidase basierenden Methoden können falsch negative Ergebnisse auftreten.
Außerhalb der Reichweite von Kindern aufbewahren.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Seien Sie vorsichtig, wenn SINEMET mit veränderter Wirkstofffreisetzung gleichzeitig mit den folgenden Arzneimitteln angewendet wird:
Antihypertensiva: Eine symptomatische orthostatische Hypotonie trat auf, wenn Levodopa/Carboxylase-Inhibitor-Kombinationen an Patienten verabreicht wurden, die bestimmte blutdrucksenkende Arzneimittel erhielten. Daher kann zu Beginn der Therapie mit SINEMET mit veränderter Wirkstofffreisetzung eine Dosisanpassung des blutdrucksenkenden Arzneimittels erforderlich sein.
AntidepressivaFälle von Nebenwirkungen, einschließlich Hypertonie und Dyskinesie, die auf die gleichzeitige Anwendung von trizyklischen Antidepressiva und Carbidopa/Levodopa-Kombinationen zurückzuführen sind, wurden selten berichtet (für Patienten, die Monoaminoxidase-Hemmer einnehmen, siehe Abschnitt 4.3).
Anticholinergika: Anticholinergika können die Aufnahme des Arzneimittels und damit das Ansprechen des Patienten beeinträchtigen.
Eisen
Studien zeigen eine Verringerung der Bioverfügbarkeit von Carbidopa und/oder Levodopa bei Einnahme mit Eisensulfat oder Eisengluconat.
Andere Medikamente: Antipsychotika können die therapeutische Wirkung von Levodopa verringern. D2-Dopamin-Rezeptor-Antagonisten (z. B. Phenothiazine, Butyrophenone und Risperidon) und Isoniazid können die therapeutische Wirkung von Levodopa verringern Es wurde berichtet, dass die positive Wirkung von Levodopa bei der Parkinson-Krankheit durch Phenytoin und Papaverin entgegengewirkt werden kann SINEMET mit veränderter Wirkstofffreisetzung sollte sorgfältig auf einen Verlust des therapeutischen Ansprechens überwacht werden.
Die Anwendung von SINEMET mit veränderter Wirkstofffreisetzung zusammen mit Dopamin abbauenden Wirkstoffen (z. B. Reserpin und Tetrabenazin) oder mit anderen Arzneimitteln, von denen bekannt ist, dass sie Monoaminspeicher erschöpfen, wird nicht empfohlen.
Die gleichzeitige Behandlung mit Selegilin und Carbidopa-Levodopa kann mit einer schweren orthostatischen Hypotonie einhergehen, die nicht auf Carbidopa-Levodopa allein zurückzuführen ist (siehe Abschnitt 4.3).
Da Levodopa mit einigen Aminosäuren konkurriert, kann seine Resorption bei einigen Patienten, die eine hohe Menge an Nahrungseiweiß zu sich nehmen, beeinträchtigt sein.
Die Wirkung einer gleichzeitigen Anwendung von Antazida und SINEMET mit veränderter Wirkstofffreisetzung auf die Bioverfügbarkeit von Levodopa wurde nicht untersucht.
04.6 Schwangerschaft und Stillzeit
Es liegen keine ausreichenden Daten vor, um den möglichen Schaden abzuschätzen, den dieser Stoff bei Anwendung in der Schwangerschaft verursachen kann. Das Arzneimittel war in Tierstudien schädlich (Skelett- und Eingeweidefehlbildungen bei Kaninchen). Es ist nicht bekannt, ob Carbidopa und Levodopa in die Muttermilch übergehen.
SINEMET mit veränderter Wirkstofffreisetzung sollte während der Schwangerschaft und Stillzeit nicht angewendet werden.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Patienten, die SINEMET mit veränderter Wirkstofffreisetzung einnehmen und Episoden von Somnolenz und/oder plötzlichen Schlafanfällen haben, sollten angewiesen werden, weder Auto zu fahren noch Aktivitäten auszuüben, bei denen eine eingeschränkte Aufmerksamkeit sich selbst oder andere dem Risiko schwerer Verletzungen oder des Todes aussetzen könnte (z von Maschinen), bis diese wiederkehrenden Episoden und die Schläfrigkeit abgeklungen sind (siehe auch Abschnitt 4.4).
04.8 Nebenwirkungen
In kontrollierten klinischen Studien bei Patienten mit mäßigen oder schweren Schwankungen der motorischen Symptome verursachte SINEMET mit veränderter Wirkstofffreisetzung keine Nebenwirkungen, die spezifisch für die Formulierung mit veränderter Wirkstofffreisetzung waren.
Die am häufigsten berichtete Nebenwirkung war Dyskinesie (eine Form von abnormer unwillkürlicher Bewegung).Eine höhere Inzidenz von Dyskinesien wurde bei SINEMET mit veränderter Wirkstofffreisetzung beobachtet als bei SINEMET-Tabletten aufgrund der Substitution der "Off-Phase" (die bei veränderter Wirkstofffreisetzung reduziert wird) SINEMET) mit der "On-Phase" (die manchmal von Dyskinesie begleitet wird).
Andere häufig berichtete Nebenwirkungen (> 2 %) waren: Übelkeit, Halluzinationen, Verwirrtheit, Schwindel, Chorea, Mundtrockenheit.
Weniger häufige Nebenwirkungen (1-2%) waren: Störungen der Traumaktivität, Dystonie, Schläfrigkeit einschließlich sehr selten übermäßiger Tagesschläfrigkeit und Episoden von plötzlichen Schlafanfällen, Schlaflosigkeit, Depression, Asthenie, Erbrechen und Anorexie.
Andere Nebenwirkungen, die in klinischen Studien oder Erfahrungen nach der Markteinführung berichtet wurden, sind:
Körper allgemein: Brustschmerzen, Synkope.
Herz-Kreislauf-Erkrankungen: Herzklopfen, orthostatische Effekte einschließlich hypotensive Episoden.
Gastrointestinale Störungen: Verstopfung, Durchfall, Dyspepsie, Magen-Darm-Schmerzen, dunkler Speichel.
Überempfindlichkeit: Angioödem, Urtikaria, Juckreiz.
Stoffwechsel- und Ernährungsstörungen: Gewichtsverlust.
Erkrankungen des Nervensystems / Psychiatrische Erkrankungen: Malignes neuroleptisches Syndrom (siehe Abschnitt 4.4), Agitiertheit, Angst, verminderte geistige Leistungsfähigkeit, Parästhesie, Desorientierung, Müdigkeit, Kopfschmerzen, extrapyramidale und Bewegungsstörungen, Sturzneigung, Ganganomalien, Muskelkrämpfe, On-Off-Phänomen, psychotische Episoden einschließlich Delirium und paranoide Vorstellung.
Impulskontrollstörungen
Bei Patienten, die mit Dopaminagonisten und/oder anderen Dopamin-Behandlungen, die Levodopa enthalten, einschließlich SINEMET mit veränderter Wirkstofffreisetzung, behandelt werden, können Spielsucht, gesteigerte Libido, Hypersexualität, zwanghaftes Einkaufen oder übermäßige Ausgaben, Bulimie und Essanfälle auftreten (siehe Abschnitt 4.4).
Atemwegserkrankungen: Dyspnoe.
Hautkrankheiten: Flush, Alopezie, Hautausschlag, dunkler Schweiß.
Sinnesorganen: verschwommene Sicht.
Urogenitale Störungen: dunkler Urin.
Andere Nebenwirkungen, die unter Levodopa oder den Levodopa/Carbidopa-Kombinationen berichtet wurden und die potenzielle Nebenwirkungen einer Behandlung mit SINEMET mit veränderter Wirkstofffreisetzung sein könnten, sind wie folgt:
Herz-Kreislauf-Erkrankungen: Herzkrankheit, Bluthochdruck, Venenentzündung.
Gastrointestinale Störungen: bitterer Mund, Speichelfluss, Dysphagie, Bruxismus, Schluckauf, Magen-Darm-Blutungen, Blähungen, Brennen auf der Zunge, Entwicklung eines Zwölffingerdarmgeschwürs.
Hämatologische Störungen: Leukopenie, hämolytische und nicht-hämolytische Anämie, Thrombozytopenie und Agranulozytose.
Erkrankungen des Nervensystems / Psychiatrische Erkrankungen: Ataxie, Taubheit, verstärktes Handzittern, Muskelkrämpfe, Blepharospasmus, Trismus, Aktivierung des latenten Horner-Syndroms, Euphorie und Demenz, suizidale Depression.
Hautkrankheiten: vermehrtes Schwitzen.
Sinnesorganen: Diplopie, erweiterte Pupillen, Augenkrise.
Urogenitale Störungen: Harnverhalt, Harninkontinenz, Priapismus.
Sonstig: Gewichtszunahme, Ödeme, Schwäche, Ohnmacht, Heiserkeit, Unwohlsein, Hitzegefühl, Erregung, unregelmäßiger Atemrhythmus, malignes Melanom (siehe Abschnitt 4.3), Purpura Henoch-Schönlein.
Krämpfe wurden beobachtet; ein kausaler Zusammenhang mit Levodopa oder den Levodopa/Carbidopa-Kombinationen wurde jedoch nicht nachgewiesen.
Diagnosetest:
Labortests mit veränderten Ergebnissen sind: Kreatinin, Harnsäure, alkalische Phosphatase, SGOT, SGPT, LDH, Bilirubin, BUN und Coombs-Test.
Es wurde über Folgendes berichtet: vermindertes Hämoglobin und Hämatokrit, Hyperglykämie, Leukozytose, Bakterien und Blut im Urin.
Carbidopa-Levodopa-Präparate können bei der Verwendung eines Teststreifentests auf Ketonurie eine falsch positive Reaktion auf Ketonkörper im Urin verursachen. Diese Reaktion wird durch das Kochen der Urinprobe nicht beeinflusst. Falsche Negativitätstests können auftreten, wenn Glukose-Oxidase-Methoden zum Nachweis von Glukose im Urin verwendet werden.
Meldung von vermuteten Nebenwirkungen
Die Meldung vermuteter Nebenwirkungen, die nach der Zulassung des Arzneimittels aufgetreten sind, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht. Angehörige von Gesundheitsberufen werden gebeten, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem zu melden. "Adresse https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Überdosierung
Die Behandlung einer akuten Überdosierung von SINEMET mit veränderter Wirkstofffreisetzung ist praktisch die gleiche wie bei einer akuten Überdosierung von Levodopa; Pyridoxin hat jedoch keine antagonistische Wirkung auf die Wirkung von SINEMET mit veränderter Wirkstofffreisetzung.
Es sollte eine elektrokardiographische Überwachung eingeleitet und der Patient sorgfältig auf die mögliche Entwicklung von Arrhythmien überwacht werden; ggf. sollte eine geeignete antiarrhythmische Therapie eingestellt werden.
Die Möglichkeit, dass der Patient andere Arzneimittel zusammen mit SINEMET mit veränderter Wirkstofffreisetzung eingenommen hat, sollte berücksichtigt werden.
Bisher liegen keine Erfahrungen mit der Dialyse vor.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN
05.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Antiparkinson-Medikament, dopaminerge Substanz.
ATC-Code: N04BA02.
SINEMET mit veränderter Wirkstofffreisetzung ist eine "Kombination aus Carbidopa, einem aromatischen Aminosäure-Decarboxylase-Hemmer, und Levodopa, der metabolischen Vorstufe von Dopamin, in einer Tablettenformulierung mit kontrollierter Freisetzung auf Basis einer Polymerstruktur zur Behandlung der Parkinson-Krankheit. .
SINEMET mit veränderter Wirkstofffreisetzung ist besonders nützlich, um die „Off-Phase“ bei Patienten zu verkürzen, die zuvor mit einer konventionellen Levodopa/Decarboxylase-Inhibitor-Kombination behandelt wurden und sich mit Dyskinesie und motorischen Symptomfluktuationen präsentierten.
Patienten mit Parkinson-Krankheit, die mit Levodopa-haltigen Präparaten behandelt werden, können Schwankungen der motorischen Symptome von unzureichender Arzneimitteldosis bis zum „Ende der Dosis“, Arzneimitteldyskinesie und Akinesie im Blut entwickeln.
Die schwere Form der motorischen Symptomoszillation (On-Off-Phänomen) ist durch unvorhersehbare Veränderungen gekennzeichnet, die von der Mobilität bis zur Immobilität reichen.Obwohl die Ursachen der motorischen Symptomoszillationen nicht vollständig verstanden sind, konnte gezeigt werden, dass sie durch eine Behandlung gemildert werden können, die stabile Plasmaspiegel von Levodopa.
Levodopa lindert die Symptome der Parkinson-Krankheit, indem es im Gehirn zu Dopamin decarboxyliert wird.
Carbidopa, das die Blut-Hirn-Schranke nicht durchdringt, hemmt nur die extrazerebrale Decarboxylierung von Levodopa, wodurch mehr Levodopa für den Transport zum Gehirn und die anschließende Umwandlung in Dopamin verfügbar wird. Dies vermeidet im Allgemeinen die Notwendigkeit, hohe Dosen von Levodopa in häufigen Intervallen zu verabreichen.
Die niedrigere Dosierung reduziert oder kann dazu beitragen, gastrointestinale und kardiovaskuläre Nebenwirkungen zu beseitigen, insbesondere solche, die auf Dopamin zurückzuführen sind, das in extrazerebralen Geweben gebildet wird.
SINEMET mit veränderter Wirkstofffreisetzung ist so konzipiert, dass die Freisetzung seiner Wirkstoffe über einen Zeitraum von 4-6 Stunden erfolgt. Bei dieser Formulierung sind die Levodopa-Plasmaspiegel konstanter und der maximale Plasmaspiegel ist 60 % niedriger als bei herkömmlichen SINEMET-Tabletten, wie bei gesunden Probanden nachgewiesen wurde.
In klinischen Studien kam es bei Patienten mit schwankenden motorischen Symptomen zu einer Verkürzung der „Off-Phase“ mit SINEMET mit veränderter Wirkstofffreisetzung im Vergleich zu Patienten, die mit SINEMET-Tabletten behandelt wurden. Nach der Gabe von SINEMET mit veränderter Wirkstofffreisetzung ist die Verringerung der „Off-Phase“ relativ gering (ca. 10 %) im Vergleich zu SINEMET-Standardtabletten und die „Inzidenz von Dyskinesien steigt leicht an. Die allgemeine Verbesserung und Qualität der täglichen Aktivitäten im On- und Off-Bereich“ "waren während der Therapie mit SINEMET mit veränderter Wirkstofffreisetzung besser als mit SINEMET-Tabletten, wie von Arzt und Patient beurteilt. Patienten bewerteten SINEMET mit veränderter Wirkstofffreisetzung als nützlicher bei Schwankungen ihres klinischen Status und bevorzugten es gegenüber SINEMET-Tabletten Bei Patienten ohne Oszillationen der motorischen Symptome , SINEMET mit veränderter Wirkstofffreisetzung bot im Vergleich zu SINEMET-Tabletten den gleichen therapeutischen Nutzen bei kürzeren Dosierungsintervallen.Im Allgemeinen gab es keine weitere Verbesserung der anderen Symptome der Parkinson-Krankheit.
05.2 Pharmakokinetische Eigenschaften
Carbidopa-Stoffwechsel : Nach oraler Gabe von radioaktiv markiertem Carbidopa bei gesunden Probanden und Patienten mit Parkinson-Krankheit wurden die maximalen Plasmaspiegel der Radioaktivität bei gesunden Probanden nach 2-4 Stunden und bei Patienten nach 1,5-5 Stunden erreicht. In beiden Gruppen wurden ungefähr gleiche Mengen mit dem Urin und den Fäzes ausgeschieden. Ein Vergleich der Urinmetaboliten von gesunden Probanden und Patienten zeigte, dass das Arzneimittel in beiden Gruppen auf die gleiche Weise metabolisiert wird. Die Ausscheidung des unveränderten Arzneimittels über den Urin war im Wesentlichen innerhalb von 7 Stunden vollständig und machte 35 % der gesamten Radioaktivität im Urin aus. Danach waren nur noch Metaboliten vorhanden. Es wurde kein Hydrazin gefunden. Unter den Metaboliten, die vom "Menschen" ausgeschieden werden, sind die "α-Methyl-3 -Methoxy-4-hydroxyphenylpropionsäure und α-Methyl-3,4-dihydroxyphenylpropionsäure. Diese machten etwa 14 bzw. 10 % der ausgeschiedenen radioaktiven Metaboliten aus. Es wurden zwei Nebenmetaboliten gefunden. Einer wurde als 3,4-Dihydroxyphenylaceton und der andere vorläufig als N-Methylcarbidopa identifiziert. Sie machten weniger als 5% der Urinmetaboliten aus. Unverändertes Carbidopa ist auch im Urin vorhanden. Sie wurden nicht verheiratet gefunden.
Metabolismus von Levodopa: Levodopa wird schnell aus dem Magen-Darm-Trakt resorbiert und weitgehend metabolisiert. Obwohl mehr als 30 Metaboliten gebildet werden können, wird es hauptsächlich in Dopamin, Adrenalin und Noradrenalin und schließlich in Dihydroxyphenylessigsäure, Homovanillinsäure und Vanylmandelsäure umgewandelt. 3-O-Methyldopa erscheint im Plasma und im Liquor. Seine Bedeutung ist nicht bekannt. Wenn Patienten mit Parkinson-Krankheit Einzeldosen von radioaktivem Levodopa im Nüchternzustand verabreicht werden, werden die maximalen Plasmaspiegel der Radioaktivität nach 0,5 bis 2 Stunden erreicht und sind 4 bis 6 Stunden lang nachweisbar. Bei Spitzenwerten erscheinen etwa 30 % der Radioaktivität als Katecholamine, 15 % als Dopamin und 10 % als Dopa.
Radioaktive Verbindungen werden schnell mit dem Urin ausgeschieden und ein Drittel der Dosis erscheint innerhalb von 2 Stunden. 80-90% der Metaboliten im Urin sind Phenylcarbonsäuren, hauptsächlich Homovanillinsäure, für 24 Stunden sind 1-2% der gewonnenen Radioaktivität Dopamin und weniger als 1% Adrenalin, Noradrenalin und unverändertes Levodopa.
Wirkung von Carbidopa auf den Levodopa-Stoffwechsel: Carbidopa erhöht bei gesunden Probanden die Levodopa-Plasmaspiegel in statistisch signifikanten Mengen, gemessen im Vergleich zu Placebo, deutlich. Dies wurde gezeigt, wenn Carbidopa vor Levodopa gegeben wird und wenn beide Arzneimittel gleichzeitig gegeben werden. In einer Studie erhöhte die Carbidopa-Vorbehandlung die Plasmaspiegel einer Einzeldosis Levodopa um etwa das Fünffache und verlängerte die Dauer der nachweisbaren Plasmakonzentrationen von Levodopa von 4 auf 8 Stunden. In anderen Studien wurden ähnliche Ergebnisse erzielt, wenn die beiden Arzneimittel zusammen verabreicht wurden. In einer Studie, in der Patienten mit Parkinson-Krankheit, die mit Carbidopa vorbehandelt worden waren, eine Einzeldosis von markiertem Levodopa verabreicht wurde, erhöhte sich die Halbwertszeit der gesamten Plasmaradioaktivität von 3 auf 15 Stunden, die von Levodopa stammte Der Anteil der als nicht metabolisiertes Levodopa verbleibenden Radioaktivität erhöhte sich mit Carbidopa um mindestens das Dreifache.
Dopamin und Homovanillinsäure im Plasma und im Urin nahmen beide mit Carbidopa-Vorbehandlung ab.
Die Pharmakokinetik von Levodopa nach Gabe von SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung wurde an gesunden jungen und älteren Freiwilligen untersucht.
Maximale Levodopa-Plasmaspiegel nach SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung wurden in einer durchschnittlichen Zeit von etwa zwei Stunden erreicht, verglichen mit 45 Minuten, die bei SINEMET-Tabletten beobachtet wurden.
Die mittleren maximalen Plasmaspiegel von Levodopa unter SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung waren 60 % niedriger als die mit SINEMET-Tabletten beobachteten.
Die In-vivo-Resorption von Levodopa nach Gabe von SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung war 4-6 Stunden lang kontinuierlich.In diesen Studien schwankten die Plasmakonzentrationen in engeren Bereichen als bei SINEMET-Tabletten.
Da die Bioverfügbarkeit von Levodopa mit SINEMET 200 mg + 50 mg mit veränderter Wirkstofffreisetzung im Vergleich zu SINEMET-Tabletten etwa 70 % beträgt, ist die Tagesdosis von Levodopa mit einer Formulierung mit kontrollierter Freisetzung im Allgemeinen höher als die der herkömmlichen Formulierung. Die Bioverfügbarkeit kann durch Medikamente beeinflusst werden, die die Darmbeweglichkeit beeinträchtigen.
Die Pharmakokinetik von Levodopa nach Gabe von SINEMET 100 mg + 25 mg mit veränderter Wirkstofffreisetzung wurde bei Patienten mit Parkinson-Krankheit untersucht. Eine kontinuierliche zweitägige, offene Dosierung über drei Monate mit SINEMET 100 mg + 25 mg mit veränderter Wirkstofffreisetzung (Bereich: 50 mg Carbidopa, 200 mg Levodopa bis zu 150 mg Carbidopa, 600 mg Levodopa täglich) führte nicht zu einer Akkumulation . Die dosisangepasste Bioverfügbarkeit einer SINEMET 100 mg + 25 mg Tablette mit veränderter Wirkstofffreisetzung entsprach der einer SINEMET 200 mg + 50 mg Tablette mit veränderter Wirkstofffreisetzung. Die mittlere maximale Levodopa-Konzentration nach Verabreichung einer SINEMET 100 mg + 25 mg Tablette mit veränderter Wirkstofffreisetzung betrug mehr als 50 % derjenigen, die nach Einnahme einer SINEMET 200 mg + 50 mg Tablette mit veränderter Wirkstofffreisetzung beobachtet wurde. Die mittlere Zeit bis zum Erreichen der maximalen Plasmaspiegel war bei SINEMET 100 mg + 25 mg mit veränderter Wirkstofffreisetzung etwas kürzer als bei SINEMET 200 mg + 50 mg veränderter Wirkstofffreisetzung.
05.3 Präklinische Sicherheitsdaten
Toxikologie
Die oralen LDs von Carbidopa betragen 1.750 mg/kg bei erwachsenen weiblichen Mäusen und 4.810 bzw. 5.610 mg/kg bei weiblichen bzw. männlichen Ratten.
Die akute orale Toxizität von Carbidopa ist bei juvenilen und erwachsenen Ratten ähnlich, jedoch ist die Verbindung bei neugeborenen Ratten toxischer. Die Anzeichen der Arzneimittelwirkung waren bei Mäusen und Ratten ähnlich und bestanden aus: Ptosis, Ataxie und verminderter Aktivität Geschlechter bei 2.260 mg/kg bei jungen weiblichen Ratten.
Anzeichen für die Wirkung des Arzneimittels waren: Lautäußerung, Reizbarkeit, Erregbarkeit, Ataxie und erhöhte Aktivität, gefolgt von einer verringerten Aktivität innerhalb von ein bis zwei Stunden Die oralen LD50s verschiedener Kombinationen von Carbidopa und Levodopa bei Mäusen reichten von 1.930 mg / kg für ein Verhältnis von 1 : 1 bis 3.270 mg / kg für ein Verhältnis von 1: 3. Diese Mengen sind die Summe der Einzeldosen von Carbidopa und Levodopa, die über 1: 3 getesteten Verhältnisse (1: 4, 1: 5, 1:10) haben sie nicht merklich erreicht ändern den Wert der LD50 im Vergleich zu dem, der mit dem Verhältnis 1:3 gefunden wurde. Die Verhältnisse von 1:3 und höher waren weniger toxisch als die Verhältnisse von 1:1 und 1:2.
Studien zur chronischen oralen Toxizität mit Carbidopa wurden bei Affen ein Jahr lang und bei Ratten 96 Wochen lang durchgeführt, wobei Dosen von 25 bis 135 mg / kg verwendet wurden. Bei Affen wurden keine arzneimittelbedingten Wirkungen beobachtet.
Bei Ratten trat bei einigen Tieren aller Dosisgruppen Schlaffheit auf.
Carbidopa führte bei Hunden zu einem Pyridoxinmangel, der durch die gleichzeitige Gabe von Pyridoxin verhindert wurde. Mit Ausnahme eines Pyridoxinmangels bei Hunden zeigte Carbidopa keine Hydrazin-assoziierte Toxizität.
Drei Dosisverhältnisse von Carbidopa und Levodopa, die 54 Wochen lang an Affen und 106 Wochen lang an Ratten verabreicht wurden, zeigten, dass die wichtigsten physikalischen Wirkungen auf die pharmakologische Wirkung der Verbindungen zurückzuführen waren.Die untersuchten Dosierungen waren (Carbidopa / Levodopa): 10 / 20, 10 /50 und 10/100 mg / kg / Tag. Die Dosis von 10/20 mg / kg / Tag hatte keine offensichtlichen körperlichen Auswirkungen. Hyperaktivität trat bei Affen bei Dosen von 10/50 und 10/100 mg / kg / Tag auf, die fortgesetzt für 32 Wochen mit der höchsten Dosis Mit der Dosis von 10/50 mg / kg / Tag nahm die Hyperaktivität ab; die Studie wurde fortgesetzt und dieses Phänomen wurde nach der 14. Woche nicht mehr beobachtet. Mangelnde Muskelkoordination und Schwäche wurden bis zu 22 Wochen mit der Dosis von 10/100 mg/kg/Tag beobachtet. Pathologische Anatomiestudien zeigten keine morphologischen Veränderungen.
Ratten, die 10/50 und 10/100 mg/kg/Tag erhielten, hatten eine verminderte normale Aktivität und zeigten abnormale Körperhaltungen. Die höhere Dosis führte zu "übermäßigem Speichelfluss. Die Gewichtszunahme nahm ab." Pathologische Anatomiestudien zeigten eine sehr leichte Hypertrophie der Follikelzellen der Unterkieferdrüsen von zwei Ratten, die 26 Wochen lang 10/100 mg / kg / Tag erhalten hatten. Nach 54 oder 106 Wochen wurden bei keiner Dosierung histomorphologische Effekte festgestellt. Bei Ratten wurde eine Hypertrophie der follikulären Speicheldrüsenzellen mit den höheren Dosen der Kombination für kürzere Zeiträume und mit Levodopa allein beobachtet.
Teratogenese und Reproduktionsstudien
Carbidopa zeigte bei Mäusen oder Kaninchen bei Dosen bis zu 120 mg / kg / Tag keine Teratogenität. Levodopa verursachte bei Kaninchen in Dosen von 125 und 250 mg / kg / Tag viszerale und skelettale Missbildungen. Bei den Kombinationen von Carbidopa und Levodopa gab es in Dosierungen von 25/250 bis 100/500 mg/kg/Tag keine Hinweise auf Teratogenität bei Mäusen, aber viszerale und skelettale Missbildungen waren quantitativ und qualitativ ähnlich wie bei Kaninchen Levodopa allein. Kombinationen von Carbidopa und Levodopa in Dosen bis zu 10/100 mg/kg/Tag hatten keine nachteiligen Auswirkungen auf die Fortpflanzungsleistung männlicher oder weiblicher Ratten, noch auf das Wachstum und das Überleben der Nachkommen.
06.0 PHARMAZEUTISCHE INFORMATIONEN
06.1 Hilfsstoffe
SINEMET 200 mg + 50 mg Tabletten mit veränderter Wirkstofffreisetzung: rotes Eisenoxid E172, Hydroxypropylcellulose, Copolymer von Polyvinylacetat mit Crotonsäure, Magnesiumstearat, Chinolingelb auf hydratisiertem Aluminium E104.
SINEMET 100 mg + 25 mg Tabletten mit veränderter Wirkstofffreisetzung: rotes Eisenoxid E172, Hydroxypropylcellulose, Copolymer von Polyvinylacetat mit Crotonsäure, Magnesiumstearat.
06.2 Inkompatibilität
Nicht relevant.
06.3 Gültigkeitsdauer
3 Jahre.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
In der Originalverpackung aufbewahren, um das Arzneimittel vor Licht zu schützen.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks
Die Tabletten sind in Aluminium-/Aluminium-Blisterpackungen enthalten.
SINEMET 100 mg + 25 mg Tabletten mit veränderter Wirkstofffreisetzung: 50 Tabletten mit veränderter Wirkstofffreisetzung.
SINEMET 200 mg + 50 mg Tabletten mit veränderter Wirkstofffreisetzung: 30 Tabletten mit veränderter Wirkstofffreisetzung.
06.6 Gebrauchs- und Handhabungshinweise
Keine besonderen Anweisungen.
07.0 INHABER DER MARKETING-ERLAUBNIS
MSD Italia S.r.l.
Via Vitorchiano, 151 - 00189 Rom
08.0 NUMMER DER MARKETING-ERLAUBNIS
SINEMET 100 mg + 25 mg Tabletten mit veränderter Wirkstofffreisetzung - 50 Tabletten AIC n. 023145042
SINEMET 200 mg + 50 mg Tabletten mit veränderter Wirkstofffreisetzung - 30 Tabletten AIC n. 023145030
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG
Datum der Erstzulassung: SINEMET 100 mg + 25 mg Tabletten mit veränderter Wirkstofffreisetzung - 50 Tabletten, November 1995
SINEMET 200 mg + 50 mg Tabletten mit veränderter Wirkstofffreisetzung - 30 Tabletten, Dezember 1992
Datum der letzten Verlängerung: Juni 2010
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs
Mai 2015