Wirkstoffe: Testosteron (Testosteron-Undecanoat)
NEBID 1000 mg / 4 ml Injektionslösung
Indikationen Warum wird Nebid verwendet? Wofür ist das?
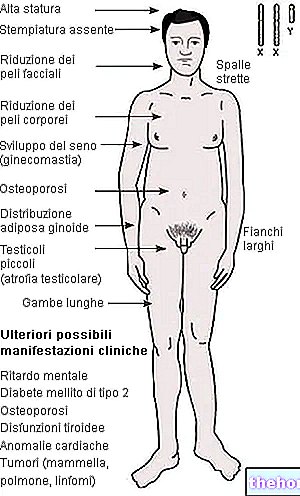
Nebid enthält als Wirkstoff Testosteron, ein männliches Hormon.Nebid wird in einen Muskel injiziert, wo es angesammelt bleibt und aus dem es über einen bestimmten Zeitraum nach und nach freigesetzt wird. Nebid wird verwendet, um Testosteron bei erwachsenen Männern zu ersetzen, zur Behandlung verschiedener gesundheitlicher Probleme aufgrund von Testosteronmangel (männlicher Hypogonadismus). Dieser Zustand muss durch zwei separate Bluttestosteronmessungen bestätigt werden und muss klinische Symptome umfassen wie:
- Impotenz
- Unfruchtbarkeit
- schlechtes sexuelles Verlangen
- Müdigkeit
- depressive Stimmung
- Knochenschwund durch zu niedrige Hormonspiegel.
Kontraindikationen Wenn Nebid nicht angewendet werden sollte
Verwenden Sie Nebid NICHT:
- wenn Sie allergisch gegen Testosteronundecanoat oder einen der sonstigen Bestandteile dieses Arzneimittels sind.
- wenn Sie androgenabhängigen Krebs haben oder Verdacht auf Krebs der Prostata oder der Brustdrüse haben.
- wenn Sie einen Lebertumor haben.
Nebid ist nicht zur Anwendung bei Frauen bestimmt.
Nebid darf bei Kindern und Jugendlichen nicht angewendet werden Es liegen keine Daten zur Anwendung von Nebid bei männlichen Patienten unter 18 Jahren vor.
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Nebido® beachten?
Bitte sprechen Sie mit Ihrem Arzt, bevor Sie Nebid anwenden, wenn Sie an folgenden Erkrankungen leiden oder in der Vergangenheit gelitten haben:
- Epilepsie
- Herz-, Nieren- oder Leberprobleme
- Migräne
- vorübergehende Unterbrechungen der Atmung während des Schlafs (Apnoe), da sie sich verschlimmern können
- Krebs, da der Kalziumspiegel im Blut möglicherweise regelmäßig überprüft werden muss
- Bluthochdruck oder wenn Sie wegen Bluthochdruck behandelt werden, da Testosteron Ihren Blutdruck ansteigen lassen kann
- Veränderungen der Blutgerinnung:
- Blutungsstörungen (d. h. Hämophilie)
- Thrombophilie (eine „Anomalie der Blutgerinnung, die das Risiko einer Thrombose erhöht – Blutgerinnsel in den Venen)
Wenn Sie an einer schweren Herz-, Leber- oder Nierenerkrankung leiden, kann die Behandlung mit Nebid schwerwiegende Komplikationen in Form einer Wasseransammlung im Körper verursachen, die manchmal von einer (kongestiven) Herzinsuffizienz begleitet wird.
Vor und während der Behandlung muss der Arzt folgende Blutuntersuchungen durchführen: Testosteronspiegel im Blut, großes Blutbild.
Wenn Sie Leberprobleme haben
Bei Patienten mit Leberfunktionsstörung wurden keine formalen Studien durchgeführt. Nebid wird Ihnen nicht verschrieben, wenn Sie an Leberkrebs gelitten haben (siehe „Nebid darf nicht angewendet werden“).
Ältere Patienten (65 Jahre oder älter)
Ihr Arzt muss Ihre Dosierung nicht ändern, wenn Sie über 65 Jahre alt sind (siehe "Ärztliche Untersuchungen / Kontrollen")
Muskelaufbau und Dopingtest
Nebid ist nicht zur Förderung des Muskelaufbaus bei Gesunden oder zur Verbesserung der körperlichen Leistungsfähigkeit indiziert.
Doping
Für diejenigen, die sportliche Aktivitäten ausüben: Die Einnahme des Medikaments ohne therapeutische Notwendigkeit stellt Doping dar und kann in jedem Fall positive Anti-Doping-Tests feststellen.
Ärztliche Untersuchungen / Check-ups
Männliche Hormone können das Wachstum von Prostatakrebs und einer vergrößerten Prostata (benigne Prostatahypertrophie) fördern. Vor der Injektion von Nebid wird Ihr Arzt Sie untersuchen, um sicherzustellen, dass Sie kein Prostatakrebs haben.
Ihr Arzt wird Ihre Prostata und Brustdrüsen regelmäßig überprüfen, insbesondere wenn Sie älter sind. Er wird Ihnen auch regelmäßige Bluttests machen.
Nach der Einnahme von hormonellen Substanzen wie Androgenen wurde das Auftreten von gutartigen (nicht krebsartigen) und bösartigen (krebsartigen) Lebertumoren beobachtet.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Nebid® beeinflussen?
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen, kürzlich andere Arzneimittel eingenommen haben oder beabsichtigen andere Arzneimittel einzunehmen, auch wenn es sich um nicht verschreibungspflichtige Arzneimittel handelt.
Ihr Arzt muss möglicherweise Ihre Dosis ändern, wenn Sie eines der folgenden Arzneimittel anwenden:
- das Hormon ACTH oder Kortikosteroide (zur Behandlung verschiedener Erkrankungen wie Rheuma, Arthritis, Allergien und Asthma): Nebid kann das Risiko von Wassereinlagerungen erhöhen, insbesondere wenn Herz und Leber nicht richtig funktionieren
- blutverdünnende Tabletten (Cumarinderivate, orale Antikoagulanzien), da dies das Blutungsrisiko erhöhen kann. Ihr Arzt wird die Dosierung überprüfen.
- Arzneimittel zur Behandlung von Diabetes. Möglicherweise muss die Dosierung Ihres Arzneimittels geändert werden, um Ihren Blutzucker zu senken. Wie andere Androgene kann Testosteron die Wirkung von Insulin verstärken.
Bitte informieren Sie Ihren Arzt, wenn Sie eine Blutgerinnungsstörung haben, da es wichtig ist, dass Ihr Arzt dies weiß, bevor er sich entscheidet, Nebid zu injizieren.
Nebid kann auch die Ergebnisse bestimmter Labortests (z. B. Schilddrüsentests) beeinflussen. Informieren Sie den Arzt oder das Laborpersonal, dass Sie Nebid anwenden.
Warnungen Es ist wichtig zu wissen, dass:
Schwangerschaft und Stillzeit
Nebid ist nicht für die Anwendung bei Frauen indiziert und das Arzneimittel sollte nicht während der Schwangerschaft oder Stillzeit angewendet werden.
Fruchtbarkeit
Eine Behandlung mit hochdosierten Testosteronpräparaten kann in der Regel die Spermienproduktion reversibel blockieren oder reduzieren (siehe auch „Nebenwirkungen“).
Verkehrstüchtigkeit und das Bedienen von Maschinen
Nebid hat keine bekannten Auswirkungen auf die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen.
Dosis, Methode und Zeitpunkt der Verabreichung Wie ist Nebid anzuwenden: Dosierung
Ihr Arzt wird Nebid (1 Ampulle/Durchstechflasche) sehr langsam in einen Muskel injizieren. Sie erhalten alle 10 bis 14 Wochen eine Injektion, die es Ihnen ermöglicht, einen ausreichenden Testosteronspiegel aufrechtzuerhalten, ohne dass es zu einer Ansammlung von Testosteron in Ihrem Blut kommt.
Nebid muss ausschließlich durch intramuskuläre Injektion verabreicht werden. Es wird besonders darauf geachtet, „das Injizieren des Arzneimittels in ein Blutgefäß zu vermeiden (siehe „Hinweise zum Umgang mit der One-Point-Cut-(OPC)-Durchstechflasche“).
Behandlungsbeginn
Vor Beginn der Behandlung und in einem frühen Stadium wird Ihr Arzt Ihren Testosteronspiegel in Ihrem Blut messen. Ihr Arzt kann Ihnen bereits nach sechs Wochen die zweite Injektion verabreichen, um schnell den erforderlichen Testosteronspiegel zu erreichen, abhängig von Ihren Symptomen und dem anfänglichen Testosteronspiegel.
Aufrechterhaltung der Nebid-Spiegel während der Behandlung
Das Intervall zwischen den Injektionen sollte wie empfohlen immer zwischen 10 und 14 Wochen liegen.
Ihr Arzt wird am Ende jeder Injektion regelmäßig Ihren Testosteronspiegel messen, um sicherzustellen, dass er korrekt ist. Wenn die gefundenen Werte zu niedrig sind, kann der Arzt entscheiden, die Häufigkeit der Injektionen zu erhöhen. Sind die Werte hingegen hoch, kann der Arzt entscheiden, die Häufigkeit der Injektionen zu verringern. Verpassen Sie nicht Ihre Injektionstermine, sonst ist es nicht möglich, einen optimalen Testosteronspiegel aufrechtzuerhalten.
Bitte sprechen Sie mit Ihrem Arzt, wenn Sie den Eindruck haben, dass die Wirkung von Nebid zu stark oder zu schwach ist.
Überdosierung Was ist zu tun, wenn Sie zu viel Nebid® eingenommen haben?
Symptome einer Überdosierung von Nebid sind:
- Reizbarkeit
- Nervosität
- Gewichtszunahme
- Verlängerte oder häufige Erektionen Informieren Sie Ihren Arzt, wenn Sie eines dieser Symptome bemerken.
Der Arzt wird die Injektionen verdünnen oder die Behandlung abbrechen.
Nebenwirkungen Was sind die Nebenwirkungen von Nebid
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Die häufigsten Nebenwirkungen sind Akne und Schmerzen an der Injektionsstelle.
Häufige Nebenwirkungen (kann bis zu 1 von 10 Patienten betreffen):
- ungewöhnlich hohe Werte an roten Blutkörperchen
- Gewichtszunahme
- Hitzewallungen
- Akne
- vergrößerte Prostata und damit verbundene Erkrankungen
- unterschiedliche Reaktionen im Bereich der Injektion (z. B. Schmerzen, Blutergüsse oder Reizungen)
Gelegentliche Nebenwirkungen (kann bis zu 1 von 100 Patienten betreffen):
- allergische Reaktion
- gesteigerter Appetit, Veränderungen bei einigen Bluttests (z. B. erhöhter Zucker- oder Fettgehalt im Blut)
- Depression, emotionale Störungen, Schlaflosigkeit, Ruhelosigkeit, Aggression, Reizbarkeit
- Kopfschmerzen, Migräne, Zittern
- Herz-Kreislauf-Erkrankungen, Bluthochdruck, Schwindel
- Bronchitis, Sinusitis, Husten, Atemnot, Schnarchen, Stimmveränderungen
- Durchfall, Übelkeit
- Veränderungen bei Leberfunktionstests
- Haarausfall, verschiedene Hautreaktionen (z. B. Juckreiz, Rötung oder trockene Haut)
- Gelenkschmerzen, Schmerzen in den Extremitäten, Muskelprobleme (z. B. Krämpfe, Schmerzen oder Steifheit) oder ein Anstieg der Kreatinphosphokinase im Blut
- Erkrankungen der Harnwege (z. B. verminderter Harnfluss, Harnverhalt, nächtliches Wasserlassen)
- Prostataerkrankungen (z. B. intraepitheliale Neoplasie der Prostata, Verhärtung oder Entzündung der Prostata), Veränderungen des Sexualtriebs, Schmerzen in den Hoden, schmerzhafte Verhärtung oder Vergrößerung der Brüste, erhöhte männliche und weibliche Hormone
- Müdigkeit, allgemeines Schwächegefühl, übermäßiges Schwitzen, Nachtschweiß
Seltene Nebenwirkungen (kann bis zu 1 von 1000 Behandelten betreffen):
- Nebid, eine ölige Flüssigkeit, kann in die Lunge gelangen (pulmonale Mikroembolie öliger Lösungen) und dies kann in seltenen Fällen Anzeichen und Symptome wie Husten, Atemnot, allgemeines Unwohlsein, übermäßiges Schwitzen, Brustschmerzen, Schwindel, Kribbeln oder Ohnmacht. Diese Reaktionen können während oder kurz nach der Injektion auftreten und sind reversibel.
Fälle von Verdacht auf anaphylaktische Reaktion wurden nach Nebid-Injektion berichtet
Zusätzlich zu den oben aufgeführten Nebenwirkungen wurden nach Behandlung mit Testosteron enthaltenden Präparaten folgende Nebenwirkungen berichtet: Nervosität, Feindseligkeit, kurze Atemaussetzer im Schlaf, verschiedene Hautreaktionen wie Schuppen und fettige Haut, vermehrtes Haar, häufigere und sehr starke Erektionen seltene Fälle von Gelbfärbung der Haut und der Augen (Gelbsucht).
In der Regel unterbricht oder reduziert die Behandlung mit hochdosierten Testosteronpräparaten die Spermienproduktion, die sich jedoch nach Beendigung der Behandlung wieder normalisiert.Eine Testosteronersatztherapie bei eingeschränkter Hodenfunktion (Hypogonadismus) kann in seltenen Fällen zu anhaltenden und schmerzhaften Erektionen (Priapismus) führen Testosteron in hohen Dosen oder über einen längeren Zeitraum kann gelegentlich zu häufigeren Manifestationen von Wassereinlagerungen und Ödemen (Schwellungen durch Flüssigkeitsansammlungen) führen.
Ein allgemeines Risiko für erhöhte Anzahl roter Blutkörperchen, Hämatokrit (Prozentsatz der roten Blutkörperchen im Blut) und Hämoglobin (der sauerstofftransportierende Bestandteil der roten Blutkörperchen) wurde im Allgemeinen bei testosteronhaltigen Produkten durch regelmäßige Blutuntersuchungen beobachtet.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker, einschließlich aller möglichen Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind. Sie können Nebenwirkungen auch direkt über das nationale Meldesystem unter „www.agenziafarmaco.gov.it/it/responsabili“ melden. Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
Ablauf und Aufbewahrung
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Sie dürfen dieses Arzneimittel nach dem auf der Verpackung und dem Etikett nach „EXP“ angegebenen Verfallsdatum nicht mehr verwenden. Das Verfallsdatum bezieht sich auf den letzten Tag dieses Monats.
Werfen Sie Arzneimittel nicht in das Abwasser oder den Hausmüll. Fragen Sie Ihren Apotheker, wie Sie Arzneimittel, die Sie nicht mehr verwenden, entsorgen sollen. Dies trägt zum Schutz der Umwelt bei.
Andere Informationen
Was Nebid enthält
Der Wirkstoff ist Testosteronundecanoat 250 mg/ml (entspricht 157,9 mg Testosteron). Eine Ampulle/Durchstechflasche enthält 1000 mg Testosteronundecanoat (entsprechend 631,5 mg Testosteron).
Die sonstigen Bestandteile sind Benzylbenzoat und raffiniertes Rizinusöl.
Wie Nebid aussieht und Inhalt der Packung
Nebid ist eine klare, gelbliche ölige Flüssigkeit. Das Paket enthält:
1 Durchstechflasche aus Braunglas / 1 Durchstechflasche aus Braunglas mit 4 ml Injektionslösung.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu haben, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS
NEBID 1000 MG / 4 ML LÖSUNG ZUR INJEKTION
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Jeder ml Injektionslösung enthält 250 mg Testosteronundecanoat, entsprechend 157,9 mg Testosteron.
Jede 4 ml Ampulle/Durchstechflasche mit Injektionslösung enthält 1000 mg Testosteronundecanoat entsprechend 631,5 mg Testosteron.
Die vollständige Auflistung der sonstigen Bestandteile finden Sie in Abschnitt 6.1.
03.0 DARREICHUNGSFORM
Injizierbare Lösung.
Klare, gelbliche ölige Lösung.
04.0 KLINISCHE INFORMATIONEN
04.1 Anwendungsgebiete
Testosteronersatztherapie bei männlichem Hypogonadismus, wenn ein Testosteronmangel durch klinisches Bild und biochemische Analyse bestätigt wurde (siehe Abschnitt 4.4).
04.2 Dosierung und Art der Anwendung
Dosierung
Eine Durchstechflasche / Durchstechflasche Nebid (entsprechend 1000 mg Testosteronundecanoat) wird alle 10-14 Wochen injiziert. Injektionen mit dieser Häufigkeit können einen ausreichenden Testosteronspiegel aufrechterhalten, ohne eine Ansammlung zu verursachen.
Behandlungsbeginn
Es wird empfohlen, den Serumtestosteronspiegel vor Beginn und in der Anfangsphase der Behandlung zu messen. Abhängig von den Serumtestosteronspiegeln und den klinischen Symptomen kann das erste Intervall zwischen den Injektionen auf mindestens 6 Wochen verkürzt werden im Vergleich zu „Empfohlenes Intervall von 10 -14 Wochen für die Wartung. Mit dieser Aufsättigungsdosis können schneller ausreichende Steady-State-Testosteronspiegel erreicht werden.
Pflege und Personalisierung der Behandlung
Das Intervall zwischen den Injektionen sollte innerhalb des empfohlenen Bereichs von 10-14 Wochen liegen. Während der Erhaltungstherapie ist eine sorgfältige Überwachung des Serumtestosteronspiegels erforderlich. Es wird empfohlen, den Serumtestosteronspiegel regelmäßig zu messen. Messungen sollten am Ende des Intervalls durchgeführt werden zwischen einer Injektion und der nächsten, zusammen mit der Bewertung der klinischen Symptome. Serumspiegel sollten das untere Drittel des Normbereichs nicht überschreiten. Serumspiegel unter dem Normbereich weisen darauf hin, dass dieser Bereich reduziert werden muss. Bei erhöhten Serumspiegeln besteht die Möglichkeit, das Intervall zwischen den Injektionen zu verlängern.
Besondere Bevölkerungsgruppen
Kinder und Jugendliche
Nebid ist nicht für Kinder und Jugendliche indiziert und wurde bei männlichen Patienten unter 18 Jahren nicht klinisch untersucht (siehe Abschnitt 4.4).
Ältere Patienten
Es liegen keine Daten vor, die auf die Notwendigkeit einer Dosisanpassung bei älteren Patienten hinweisen (siehe Abschnitt 4.4).
Patienten mit eingeschränkter Leberfunktion
Bei Patienten mit Leberfunktionsstörung wurden keine formalen Studien durchgeführt. Die Anwendung von Nebid ist bei Männern mit bestehenden oder früheren Lebertumoren kontraindiziert (siehe Abschnitt 4.3).
Patienten mit eingeschränkter Nierenfunktion
Bei Patienten mit eingeschränkter Nierenfunktion wurden keine formalen Studien durchgeführt.
Art der Verabreichung
Zur intramuskulären Anwendung.
Die Injektionen sollten sehr langsam (über zwei Minuten) verabreicht werden. Nebid muss streng intramuskulär injiziert werden. Achten Sie darauf, Nebid tief in die Glutealstelle zu injizieren und beachten Sie dabei die üblichen Vorsichtsmaßnahmen für die intramuskuläre Verabreichung. Besondere Vorsicht ist geboten, um eine intravaskuläre Injektion zu vermeiden (siehe Abschnitt 4.4 „Verabreichung"). Der Inhalt einer Durchstechflasche / Durchstechflasche sollte unmittelbar nach dem Öffnen intramuskulär injiziert werden. (Für die Durchstechflasche: siehe Abschnitt 6.6 für Anweisungen zum sicheren Öffnen der Durchstechflasche ).
04.3 Kontraindikationen
Die Anwendung von Nebid ist kontraindiziert bei Männern mit:
• androgenabhängiger Krebs der Prostata oder der männlichen Brustdrüse
• vorhandene oder frühere Lebertumore
• Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile (aufgeführt in Abschnitt 6.1).
Die Anwendung von Nebid ist bei Frauen kontraindiziert.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung
Die Anwendung von Nebid bei Kindern und Jugendlichen wird nicht empfohlen.
Nebid sollte nur bei nachgewiesenem Hypogonadismus (hypergonadotrop und hypogonadotrop) und nach Ausschluss anderer für die Symptome verantwortlicher Ätiologien vor Behandlungsbeginn verabreicht werden Körperstruktur, Asthenie, verminderte Libido, erektile Dysfunktion usw.) und durch zwei separate Messungen des Testosteronspiegels im Blut bestätigt.
Ältere Bevölkerung
Es liegen nur begrenzte Erfahrungen zur Sicherheit und Wirksamkeit der Anwendung von Nebid bei Patienten über 65 Jahren vor und es besteht derzeit keine Einigkeit über altersspezifische Referenz-Testosteronwerte. Es muss jedoch berücksichtigt werden, dass der Serumtestosteronspiegel mit zunehmendem Alter physiologisch abnimmt.
Ärztliche Untersuchungen und Laboruntersuchungen
Medizinische Untersuchungen
Vor Beginn der Testosterontherapie müssen sich alle Patienten einer gründlichen Untersuchung unterziehen, um das Risiko eines vorbestehenden Prostatakrebses auszuschließen. Patienten, die eine Testosterontherapie erhalten, müssen sich einer sorgfältigen und regelmäßigen Überwachung der Prostata (rektale Untersuchung und Bestimmung des Serum-PSA) und der Brüste gemäß den empfohlenen Methoden mindestens einmal im Jahr und bei älteren Patienten und Risikopatienten (diese mit klinischen oder familiären Faktoren). Lokale Richtlinien zur Überwachung der Anwendungssicherheit bei der Testosteronersatztherapie sollten berücksichtigt werden.
Labortest
Der Testosteronspiegel sollte zu Studienbeginn und in regelmäßigen Abständen während der Behandlung überwacht werden. Ärzte sollten die Dosis individuell von Patient zu Patient anpassen, um die Aufrechterhaltung des eugonadalen Testosteronspiegels sicherzustellen.
Bei Patienten, die eine Androgen-Langzeittherapie erhalten, sollten auch die folgenden Laborparameter in regelmäßigen Abständen überwacht werden: Hämoglobin und Hämatokrit, Leberfunktionsparameter und Lipidprofil (siehe Abschnitt 4.8).
Aufgrund der Variabilität der Laborergebnisse müssen alle Tests zur Bestimmung von Testosteron im selben Labor durchgeführt werden.
Tumore
Androgene können das Fortschreiten von subklinischem Prostatakrebs und benigner Prostatahyperplasie beschleunigen.
Nebid sollte bei Krebspatienten, bei denen das Risiko einer Hyperkalzämie (und einer damit verbundenen Hyperkalziurie) aufgrund von Knochenmetastasen besteht, mit Vorsicht angewendet werden. Bei diesen Patienten ist eine regelmäßige Überwachung der Serumkalziumkonzentration ratsam.
Bei Anwenderinnen von hormonellen Substanzen wie Androgenen wurden Fälle von gutartigen und bösartigen Lebertumoren berichtet. Wenn bei Männern, die Nebido einnehmen, schwere Oberbauchbeschwerden, Lebervergrößerung oder Anzeichen einer intraabdominalen Blutung auftreten, sollte differenzialdiagnostisch an die Möglichkeit eines Leberkrebses gedacht werden.
Herz-, Leber- oder Nierenversagen
Bei Patienten mit schwerer Herz-, Leber- oder Niereninsuffizienz oder ischämischer Herzerkrankung kann die Behandlung mit Testosteron schwerwiegende Komplikationen hervorrufen, die durch Ödeme mit oder ohne kongestive Herzinsuffizienz gekennzeichnet sind. In diesem Fall muss die Behandlung sofort abgebrochen werden.
Leber- oder Niereninsuffizienz
Es wurden keine Studien zum Nachweis der Wirksamkeit und Sicherheit des Arzneimittels bei Patienten mit eingeschränkter Nieren- oder Leberfunktion durchgeführt, daher sollte eine Testosteronersatztherapie bei diesen Patienten mit Vorsicht angewendet werden.
Herzfehler
Vorsicht ist geboten bei Patienten, die für Ödeme prädisponiert sind, beispielsweise bei schwerer Herz-, Leber- oder Niereninsuffizienz oder ischämischen Herzerkrankungen, da die Behandlung mit Androgenen zu einer erhöhten Natrium- und Wasserretention führen kann oder ohne Herzinsuffizienz sollte die Behandlung sofort abgebrochen werden (siehe Abschnitt 4.8).
Testosteron kann einen Blutdruckanstieg verursachen und Nebid sollte bei Hypertonikern mit Vorsicht angewendet werden.
Gerinnungsstörungen
Als allgemeine Regel gilt, dass die Einschränkungen der Anwendung intramuskulärer Injektionen bei Patienten mit erworbenen oder erblichen Blutungsproblemen immer beachtet werden müssen.
Es wurde berichtet, dass Testosteron und seine Derivate die Aktivität von Cumarin-Derivaten als orale Antikoagulanzien erhöhen (siehe auch Abschnitt 4.5).
Testosteron sollte bei Patienten mit Thrombophilie mit Vorsicht angewendet werden, da es nach Markteinführung Studien und Spontanberichte über thrombotische Ereignisse bei diesen Patienten während einer Testosterontherapie gegeben hat.
Andere Bedingungen
Nebido sollte bei Patienten mit Epilepsie und Migräne mit Vorsicht angewendet werden, da sich diese Zustände verschlimmern können.
Bei mit Androgen behandelten Patienten, die nach einer Substitutionstherapie normale Testosteronspiegel im Plasma erreichen, kann eine erhöhte Insulinsensitivität auftreten.
Bestimmte klinische Anzeichen wie Reizbarkeit, Nervosität, Gewichtszunahme, verlängerte oder häufige Erektionen können auf eine übermäßige Androgenexposition hinweisen, die eine Dosisanpassung erforderlich macht.
Eine bereits bestehende Schlafapnoe kann potenziert werden.
Sportler, die mit Testosteron als Ersatztherapie bei primärem und sekundärem männlichem Hypogonadismus behandelt werden, sollten darüber informiert werden, dass das Arzneimittel einen Wirkstoff enthält, der bei Dopingtests zu positiven Ergebnissen führen kann.
Androgene sind nicht zur Steigerung der Muskelentwicklung bei Gesunden oder zur Steigerung der körperlichen Leistungsfähigkeit indiziert.
Die Anwendung von Nebid sollte dauerhaft abgebrochen werden, wenn während der Behandlung mit der empfohlenen Dosierung die Symptome einer übermäßigen Androgenexposition bestehen bleiben oder wieder auftreten.
Verwaltung
Wie alle öligen Lösungen muss Nebid streng intramuskulär und sehr langsam (über zwei Minuten) injiziert werden. Die Bildung pulmonaler Mikroembolien aus öligen Lösungen kann in seltenen Fällen zu Anzeichen und Symptomen wie Husten, Atemnot, Unwohlsein, Hyperhidrose, Brustschmerzen, Schwindel, Parästhesie oder Synkope führen. Diese Reaktionen können während oder kurz nach der Injektion auftreten und sind reversibel. Der Patient sollte daher während und unmittelbar nach jeder Injektion beobachtet werden, um mögliche Anzeichen und Symptome einer pulmonalen öligen Mikroembolie frühzeitig erkennen zu können. Die Behandlung erfolgt in der Regel unterstützend, bestehend aus beispielsweise bei der Verabreichung von Sauerstoff.
Fälle von Verdacht auf eine anaphylaktische Reaktion wurden nach der Injektion von Nebid berichtet.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Orale Antikoagulanzien
Es wurde beobachtet, dass Testosteron und seine Derivate die Aktivität von Cumarin-Derivaten, oralen Antikoagulanzien, erhöhen.Patienten, die orale Antikoagulanzien einnehmen, erfordern eine engmaschige Überwachung, insbesondere zu Beginn oder am Ende einer Androgentherapie. Eine verstärkte Überwachung der Prothrombinzeit und häufige INR-Bestimmungen werden empfohlen.
Andere Interaktionen
Die gleichzeitige Anwendung von Testosteron und ACTH oder Kortikosteroiden kann die Bildung von Ödemen verstärken, daher sollten diese Wirkstoffe mit Vorsicht angewendet werden, insbesondere bei Patienten mit Herz- oder Lebererkrankungen oder bei Patienten mit einer Prädisposition für Ödeme.
Wechselwirkungen mit Labortests: Androgene können die Thyroxin-bindenden Globulinspiegel senken, wodurch die Gesamt-T4-Spiegel im Serum gesenkt und die Harz-T3- und T4-Aufnahme erhöht werden. Die Spiegel des freien Schilddrüsenhormons bleiben jedoch unverändert und es werden keine klinischen Anzeichen einer Schilddrüsenfunktionsstörung beobachtet.
04.6 Schwangerschaft und Stillzeit
Fruchtbarkeit
Eine Testosteronersatztherapie kann die Spermatogenese reversibel reduzieren (siehe Abschnitte 4.8 und 5.3).
Schwangerschaft und Stillzeit
Nebid ist nicht zur Anwendung bei Frauen indiziert und das Arzneimittel sollte nicht während der Schwangerschaft oder Stillzeit angewendet werden (siehe Abschnitt 4.3).
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Nebid hat keinen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
04.8 Nebenwirkungen
Zusammenfassung des Sicherheitsprofils
Zu Nebenwirkungen im Zusammenhang mit der Anwendung von Androgenen siehe auch Abschnitt 4.4.
Die am häufigsten berichteten Nebenwirkungen während der Behandlung mit Nebido sind Akne und Schmerzen an der Injektionsstelle.
Eine pulmonale Mikroembolie öliger Lösungen kann in seltenen Fällen zu Anzeichen und Symptomen wie Husten, Atemnot, Unwohlsein, Hyperhidrose, Brustschmerzen, Schwindel, Parästhesie oder Synkope führen. Diese Reaktionen können während oder kurz nach der Injektion auftreten und sind reversibel. Fälle von Verdacht auf pulmonale ölige Mikroembolie wurden nach Meinung des berichtenden Unternehmens oder Arztes in klinischen Studien selten (bei ≥ 1/10.000,
Fälle von Verdacht auf eine anaphylaktische Reaktion wurden nach der Injektion von Nebid berichtet.
Androgene können das Fortschreiten von subklinischem Prostatakrebs und benigner Prostatahyperplasie beschleunigen.
Unerwünschte Arzneimittelwirkungen, die nach MedDRA-Systemorgansystemen (MedDRA-SOCs) klassifiziert sind, sind in der folgenden Tabelle aufgeführt (Tabelle 1). Häufigkeiten basieren auf Daten aus klinischen Studien und sind als häufig (≥ 1/100,
Tabelle der Nebenwirkungen
Tabelle 1: Relative Häufigkeit von Männern mit Nebenwirkungen, klassifiziert nach MedDRA SOC, aus gepoolten Daten aus 6 klinischen Studien, N = 422 (100,0 %) davon N = 302 hypogonadale Patienten, die mit IM-Injektionen behandelt wurden von Testosteronundecanoat 250 mg / ml aus 4 ml und N = 120 mit i.m. Injektion behandelt von Testosteron Undecanoat 250 mg / ml von 3 ml
* Die jeweilige Häufigkeit wurde im Zusammenhang mit der Einnahme von testosteronhaltigen Produkten beobachtet.
** Häufigkeit basiert auf der Anzahl der Injektionen
Die Liste enthält den MedDRA-Begriff (Version 11.0), der eine bestimmte Nebenwirkung am besten beschreibt. Verwandte Symptome oder Zustände sind nicht aufgeführt, sollten aber berücksichtigt werden.
1 Hautausschlag, einschließlich papulöser Hautausschlag
2 Muskelerkrankungen: Muskelkrämpfe, Muskelrisse und Myalgie
3 Verschiedene Arten von Reaktionen an der Injektionsstelle: Schmerzen an der Injektionsstelle, Beschwerden an der Injektionsstelle, Juckreiz an der Injektionsstelle, Erythem an der Injektionsstelle, Hämatom an der Injektionsstelle, Reizung an der Injektionsstelle „Injektion, Reaktion an der Injektionsstelle“.
4Hyperhidrose: Hyperhidrose und Nachtschweiß
Beschreibung ausgewählter Nebenwirkungen
Eine pulmonale Mikroembolie öliger Lösungen kann in seltenen Fällen zu Anzeichen und Symptomen wie Husten, Atemnot, Unwohlsein, Hyperhidrose, Brustschmerzen, Schwindel, Parästhesie oder Synkope führen. Diese Reaktionen können während oder kurz nach der Injektion auftreten und sind reversibel. Fälle von Verdacht auf pulmonale ölige Mikroembolie wurden nach Meinung des berichtenden Unternehmens oder Arztes in klinischen Studien selten berichtet (bei ≥ 1/10.000,
Zusätzlich zu den oben genannten Nebenwirkungen wurden während der Behandlung mit Testosteron enthaltenden Präparaten folgende Nebenwirkungen berichtet: Nervosität, Feindseligkeit, Schlafapnoe, verschiedene Hautreaktionen einschließlich Seborrhoe, Hypertrichose, erhöhte Häufigkeit von Erektionen und in sehr seltenen Fällen Gelbsucht.
Die Therapie mit hochdosierten Testosteron-Präparaten unterbricht oder reduziert in der Regel die Spermatogenese reversibel und führt zu einer Verkleinerung der Hoden; Testosteronersatztherapie des Hypogonadismus kann in seltenen Fällen anhaltende und schmerzhafte Erektionen (Priapismus) verursachen.Die Gabe von Testosteron in hohen Dosen oder über einen längeren Zeitraum kann gelegentlich zu häufigeren Manifestationen von Wassereinlagerungen und Ödemen führen.
Meldung von vermuteten Nebenwirkungen
Die Meldung vermuteter Nebenwirkungen, die nach der Zulassung des Arzneimittels aufgetreten sind, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht. Angehörige von Gesundheitsberufen werden gebeten, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem zu melden .agenziafarmaco.gov.it/it/responsabili".
04.9 Überdosierung
Nach einer Überdosierung sind außer einer Unterbrechung der medikamentösen Therapie oder einer Dosisreduktion keine besonderen therapeutischen Maßnahmen erforderlich.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN
05.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Androgene, 3-Oxoandrosten-Derivate
ATC-Code: G03B-A03
Testosteronundecanoat ist ein Ester des natürlich vorkommenden Androgens Testosteron.Die aktive Form, Testosteron, wird durch Eliminierung der Seitenkette gebildet.
Testosteron ist das wichtigste männliche Androgen, das hauptsächlich in den Hoden und in geringerem Maße in der Nebennierenrinde synthetisiert wird.
Testosteron ist verantwortlich für die Ausprägung männlicher Merkmale während der fetalen Entwicklung, der frühen Kindheit und der Pubertät und damit für den Erhalt des männlichen Phänotyps und der androgenabhängigen Funktionen (zB Spermatogenese, akzessorische Geschlechtsdrüsen) , zB Haut, Muskel, Skelett, Niere , Leber, Knochenmark und Zentralnervensystem.
Je nach Zielorgan ist die Testosteronaktivität überwiegend androgen (zB Prostata, Samenbläschen, Nebenhoden) oder proteinanabol (Muskel, Knochen, Hämatopoese, Niere, Leber).
Die Wirkungen von Testosteron in einigen Organen treten nach der peripheren Umwandlung von Testosteron in Östradiol auf, das an Östrogenrezeptoren im Kern von Zielzellen wie Hypophyse, Fett, Gehirn- und Knochenzellen und Leydig-Zellen des Hodens bindet.
05.2 Pharmakokinetische Eigenschaften
Absorption
Nebid ist eine Depotform von Testosteronundecanoat mit langsamer Freisetzung zur intramuskulären Verabreichung, die den First-Pass-Effekt vermeidet. Nach der intramuskulären Injektion von Testosteronundecanoat in Form einer öligen Lösung wird die Verbindung nach und nach freigesetzt und fast vollständig gespalten durch Serumesterasen in Testosteron und Undecansäure. Einen Tag nach der Verabreichung kann ein Anstieg der Serumtestosteronspiegel über die Basalwerte beobachtet werden.
Gleichgewichtsbedingungen (Steady-State)
Nach der ersten intramuskulären Injektion von 1000 mg Testosteronundecanoat bei hypogonadalen männlichen Patienten wurden nach 7 Tagen mittlere Cmax-Werte von 38 nmol/l (11 ng/ml) erhalten. Die zweite Dosis wurde 6 Wochen nach der ersten Injektion verabreicht und es wurden maximale Testosteronkonzentrationen von ca. 50 nmol/l (15 ng/ml) erreicht. Ein konstantes Dosierungsintervall von 10 Wochen wurde über die 3 nachfolgenden Verabreichungen aufrechterhalten und Gleichgewichtsbedingungen wurden zwischen der dritten und fünften Verabreichung erreicht. Die mittleren Cmax- und Cmin-Werte von Testosteron im Steady-State betrugen 37 (11 ng/ml) bzw. 16 nmol/l (5 ng/ml). Die mediane intra- und interindividuelle Variabilität (Variationskoeffizient, %) der Cmin-Werte betrug 22 % (Spanne: 9-28 %) bzw. 34 % (Spanne: 25-48 %).
Verteilung
Im Serum männlicher Patienten sind etwa 98 % des zirkulierenden Testosterons an Sexualhormon-bindendes Globulin (SHBG) und Albumin gebunden. Nur die freie Fraktion von Testosteron gilt als biologisch aktiv. Nach intravenöser Infusion von Testosteron bei männlichen Patienten. eine "Testosteron-Eliminationshalbwertszeit von ungefähr eins" wurde beobachtet und ein scheinbares Verteilungsvolumen von ungefähr 1,0 l/kg wurde beobachtet.
Biotransformation
Testosteron, das durch Esterspaltung aus Testosteronundecanoat entsteht, wird wie körpereigenes Testosteron metabolisiert und ausgeschieden, undecansäure wird wie andere aliphatische Carbonsäuren durch β-Oxidation metabolisiert. Die wichtigsten aktiven Metaboliten von Testosteron sind Östradiol und Dihydrotestosteron.
Beseitigung
Testosteron wird weitgehend in der Leber und extrahepatisch metabolisiert. Nach Verabreichung von radioaktiv markiertem Testosteron erscheinen etwa 90 % der Radioaktivität im Urin in Form von Glucuron- und Schwefelsäure-Konjugaten, während 6 % in den Fäzes erscheinen, nachdem sie einem enteropathischen Kreislauf unterzogen wurden.Urinprodukte sind Androsteron und Ethiocolanolon: Nach intramuskulärer Verabreichung dieser "Depot"-Formulierung ist die Freisetzungsrate durch eine "Halbwertszeit von 90 ± 40 Tagen" gekennzeichnet.
05.3 Präklinische Sicherheitsdaten
Toxikologische Studien zeigten keine anderen Wirkungen als die, die anhand des Hormonprofils von Nebid erklärbar waren.
Testosteron erwies sich in vitro unter Verwendung des Mutationsreversionsmodells (Ames-Test) oder von Hamster-Eierstockzellen als nicht mutagen. In Studien an Labortieren wurde ein Zusammenhang zwischen einer androgenen Behandlung und bestimmten Krebsarten festgestellt.Experimentelle Daten an Ratten zeigten eine erhöhte Inzidenz von Prostatakrebs nach Behandlung mit Testosteron.
Es ist bekannt, dass Sexualhormone die Entwicklung einiger Krebsarten begünstigen, die durch bekannte Karzinogene verursacht werden.Die klinische Relevanz der letztgenannten Beobachtung ist nicht bekannt.
Fertilitätsstudien an Nagetieren und Primaten haben gezeigt, dass eine Testosteronbehandlung die Fertilität beeinträchtigen kann, indem die Spermatogenese dosisabhängig unterdrückt wird.
06.0 PHARMAZEUTISCHE INFORMATIONEN
06.1 Hilfsstoffe
Benzylbenzoat
Raffiniertes Rizinusöl
06.2 Inkompatibilität
Da keine Kompatibilitätsstudien durchgeführt wurden, darf das Arzneimittel nicht mit anderen Arzneimitteln gemischt werden.
06.3 Gültigkeitsdauer
5 Jahre
Das Arzneimittel sollte sofort nach dem ersten Öffnen verwendet werden
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks
Phiole
5 ml Braunglas (Typ I) Durchstechflaschen mit 4 ml Lösung.
Verpackung: 1 Fläschchen mit 4 ml
Phiole
6 ml Durchstechflasche aus braunem (Typ I) Glas mit einem grauen Brombutylstopfen (ETFE-Liner) zur Injektion und einer umrandeten Kappe, die 4 ml Lösung enthält.
Verpackung: 1 Fläschchen mit 4 ml
06.6 Gebrauchs- und Handhabungshinweise
Die Injektionslösung sollte vor der Anwendung visuell überprüft werden; es sollten nur klare Lösungen ohne suspendierte Partikel verwendet werden.
Das Arzneimittel ist nur zur einmaligen Anwendung bestimmt; Nicht verwendete Lösung muss gemäß den geltenden örtlichen Vorschriften entsorgt werden.
Phiole
Hinweise zur Handhabung des One-Point Cut (OPC)-Fläschchens:
Unterhalb des farbigen Punktes hat die Durchstechflasche einen Vorschnitt, der das Öffnen mit einer Bügelsäge überflüssig macht Vor dem Öffnen sicherstellen, dass die im oberen Teil der Durchstechflasche vorhandene Lösung auf den Boden gefallen ist. Verwenden Sie beide Hände zum Öffnen; Halten Sie den unteren Teil der Durchstechflasche mit einer Hand fest und ziehen Sie mit der anderen den oberen Teil entgegen der Richtung des farbigen Punktes ab.
Phiole
Die Durchstechflasche ist nur zum einmaligen Gebrauch bestimmt. Der Inhalt der Durchstechflasche sollte unmittelbar nach dem Aufsaugen in die Spritze intramuskulär injiziert werden.Nach dem Entfernen der Kunststoffkappe den Metallring oder die Schraubkappe nicht entfernen.
07.0 INHABER DER MARKETING-ERLAUBNIS
Bayer S.p.A. - Viale Certosa, 130 - 20156 Mailand
08.0 NUMMER DER MARKETING-ERLAUBNIS
1 Durchstechflasche mit 4 ml AIC 037051012
1 Durchstechflasche mit 4 ml AIC 037051024
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG
Datum der Erstzulassung: 25. Oktober 2006
Datum der letzten Verlängerung: 25. November 2008
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs
11/2016