Wirkstoffe: Eperison-Hydrochlorid
EXPOSIEREN 50 mg Filmtabletten
EXPOSE 100 mg Filmtabletten
Indikationen Warum wird Expose verwendet? Wofür ist das?
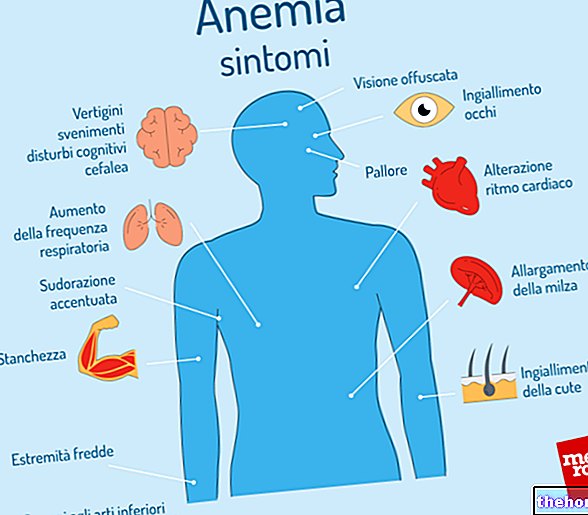
Expose enthält Eperisonhydrochlorid, einen Wirkstoff aus der Kategorie der Muskelrelaxantien, der zur Behandlung von Muskelkontraktionen, damit verbundenen Schmerzen und unwillkürlichen Muskelkontraktionen (Spastizität) verwendet wird.
Exposesi Verwendung für:
- Muskelkontrakturen aufgrund von Erkrankungen der Knochen, Gelenke und Muskeln (Zervixarthritis, Schultergelenkarthritis, Lumbosciatalgie, Muskelschmerzen allgemein)
- unwillkürliche Muskelkontraktionen (Spastizität) bei einer Krankheit namens Plaque-Sklerose
- Spastik bei Erkrankungen des Rückenmarks infektiöser, degenerativer, traumatischer oder krebsartiger Natur
- Spastik zerebralen Ursprungs
Sprechen Sie mit Ihrem Arzt, wenn Sie sich nach der verordneten Behandlungsdauer nicht besser oder schlechter fühlen.
Kontraindikationen, wenn Expose nicht verwendet werden sollte
Nehmen Sie kein Exposé
- wenn Sie allergisch gegen Eperisonhydrochlorid oder einen der sonstigen Bestandteile dieses Arzneimittels sind
- in Schwangerschaft und Stillzeit
- wenn Sie eine schwere Lebererkrankung haben (schweres Leberversagen)
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Expose® beachten?
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Expose einnehmen.
Informieren Sie Ihren Arzt
- wenn Sie an einer Leber- und/oder Nierenerkrankung leiden oder in der Vergangenheit gelitten haben
- wenn Sie abnormale Leber- und/oder Nierenfunktionswerte (Labortests) haben, weil er Ihnen erklären wird, was zu tun ist und welche Kontrollen Sie durchführen müssen
Kinder
Exposition wird nicht für die Anwendung bei Kindern empfohlen
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Expose verändern?
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen, kürzlich andere Arzneimittel eingenommen haben oder beabsichtigen andere Arzneimittel einzunehmen.
Besondere Vorsicht und Wachsamkeit des Arztes wird bei gleichzeitiger Anwendung mit folgenden Arzneimitteln empfohlen:
- Salicylate (z. B. Aspirin), da deren Blutspiegel gesenkt werden
- Calciumantagonisten, da deren blutdrucksenkende Wirkung verstärkt werden kann.
Warnungen Es ist wichtig zu wissen, dass:
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Einnahme dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Während der Schwangerschaft und Stillzeit sollte Expose nicht eingenommen werden.Wenn Expose eingenommen werden soll, sollte das Stillen abgebrochen werden.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Exposé könnte die Aufmerksamkeit reduzieren. Besondere Vorsicht ist geboten, wenn Sie Fahrzeuge führen oder andere Maschinen bedienen müssen
Dosierung und Art der Anwendung Wie ist Expose anzuwenden: Dosierung
Nehmen Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker ein. Fragen Sie im Zweifelsfall Ihren Arzt oder Apotheker.
Die empfohlene Dosis beträgt:
Erwachsene
Zur Behandlung von Muskelkontrakturen aufgrund von Erkrankungen der Knochen, Gelenke und Muskeln beträgt die empfohlene Dosierung je nach Schwere der Symptome 150-300 mg pro Tag:
- 1 Tablette mit 50 mg oder 100 mg 3-mal täglich nach den Mahlzeiten.
Zur Behandlung von Spastik beträgt die empfohlene Dosierung 300 mg pro Tag:
- 1 Tablette mit 100 mg 3-mal täglich nach den Mahlzeiten.
Senioren
Bei älteren Patienten mit Leber- und/oder Nierenerkrankungen sollte die Dosis unter enger ärztlicher Überwachung reduziert werden.
Es wird empfohlen, die Tagesdosis von 150 mg nicht zu überschreiten.
Anwendung bei Kindern
Die Anwendung bei Kindern wird nicht empfohlen.
Überdosierung Was ist zu tun, wenn Sie eine Überdosis von Expose® eingenommen haben?
Wenn Sie versehentlich eine Überdosis des Arzneimittels eingenommen haben, fragen Sie Ihren Arzt um Rat oder gehen Sie in das nächste Krankenhaus.
Im Falle einer versehentlichen Überdosierung kann es zu einer Verringerung des Muskeltonus (Hypotonie) mit möglicher Beteiligung der Muskeln, die die Atmung regulieren, kommen, obwohl in der Literatur keine derartigen Wirkungen beschrieben wurden.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker
Nebenwirkungen Was sind die Nebenwirkungen von Expose
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Schwere Nebenwirkungen
Die folgenden Symptome können Anzeichen schwerer Hautreaktionen sein, wie z. B. okulo-mukokutanes Syndrom (Steven-Johnson-Syndrom) oder Hautzelltod (Lyell-Syndrom). Brechen Sie die Einnahme von Expose sofort ab und suchen Sie Ihren Arzt auf, wenn Sie eines dieser Symptome bemerken:
- Rötung
- jucken
- allergische Hautreaktionen (Nesselsucht)
- Schwellung (Ödem) des Gesichts oder anderer Teile
- Schwierigkeiten beim Atmen (Dyspnoe)
- Fieber
- Hautreizung (Erythem)
- Vesikel
- erhöhte und/oder erschwerte Durchblutung des Auges (Augenstauung)
- Entzündung der Mundschleimhaut (Stomatitis)
Die mit der Exposition verbundenen Nebenwirkungen wurden nach Häufigkeit nach folgendem Schema klassifiziert:
Sehr häufige Nebenwirkungen (kann mehr als 1 von 10 Behandelten betreffen):
- Schläfrigkeit, Kopfschmerzen, verwirrter Geist
- Magenschmerzen, Durchfall, Übelkeit, Erbrechen, Verstopfung, Magenbeschwerden, Verdauungsstörungen
- plötzliche rote Flecken oder Schwellungen auf der Haut (Hautausschlag)
- verminderter Appetit (Anorexie)
- Schwächegefühl, Müdigkeit
- Schlaflosigkeit
Häufige Nebenwirkungen (kann bis zu 1 von 10 Behandelten betreffen):
- Ergebnisse von Bluttests mit erhöhten Leberenzymwerten (AST, ALT und alkalische Phosphatase)
- erhöhte Wahrnehmung des Herzschlags (Palpitationen)
- Schwindel, Gleichgewichtsverlust (Schwindel), Stimmungsschwankungen, Zittern in Armen oder Beinen, verminderte Empfindung
- Entzündung der Mundschleimhäute, Schwellung des Magens
- Schwierigkeiten beim Wasserlassen, Unfähigkeit, Urin zu halten
- Juckreiz, übermäßiges Schwitzen
- Muskelsteifheit, Verringerung des Muskeltonus
- Hitzewallungen
- Flüssigkeitsansammlung im Gewebe (Ödem), Durst
Gelegentliche Nebenwirkungen (kann bis zu 1 von 100 Behandelten betreffen):
- anormale Bluttestergebnisse (erhöhter Harnstoffstickstoffspiegel), Mangel an roten Blutkörperchen (Anämie)
- das Gefühl, dass Sie Ihre Blase nicht vollständig entleert haben
- Ergebnisse von Urintests, die Protein zeigen (Proteinurie)
Sehr seltene Nebenwirkungen (kann bis zu 1 von 10.000 Behandelten betreffen):
- schwere Hautreaktionen (okulomukokutanes Syndrom, Steven-Johnson-Syndrom), Absterben von Hautzellen (Lyell-Syndrom)
- Schock und schwere allergische Reaktionen (Überempfindlichkeit)
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker, einschließlich aller möglichen Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind. Sie können Nebenwirkungen auch direkt über das Yellow Card Scheme unter www.mhra.gov.it/it/responsabili melden.Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
Ablauf und Aufbewahrung
Unter 30 °C lagern.
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Verwenden Sie dieses Arzneimittel nicht nach dem auf der Packung angegebenen Verfallsdatum.
Das Ablaufdatum bezieht sich auf den letzten Tag dieses Monats.
Verwenden Sie dieses Arzneimittel nicht, wenn die Packung geöffnet oder beschädigt wurde.
Werfen Sie Arzneimittel nicht in das Abwasser oder den Hausmüll. Fragen Sie Ihren Apotheker, wie Sie Arzneimittel, die Sie nicht mehr verwenden, entsorgen sollen. Dies trägt zum Schutz der Umwelt bei.
Was enthüllen
EXPOSITION 50 mg Filmtabletten:
- Der Wirkstoff ist Eperisonhydrochlorid 50 mg
- Die sonstigen Bestandteile sind: Maisstärke, mikrokristalline Cellulose, vernetzte Natriumcarboxymethylcellulose, Hydroxypropylcellulose, Calciumstearat.
- Filmüberzug: Hydroxypropylmethylcellulose, Polyethylenglycol 6000, Titandioxid, Dimethicon, Talkum.
EXPOSE 100 mg Filmtabletten
- Der Wirkstoff ist 100 mg Eperisonhydrochlorid
- Die sonstigen Bestandteile sind: Maisstärke, mikrokristalline Cellulose, vernetzte Natriumcarboxymethylcellulose, Hydroxypropylcellulose, Calciumstearat.
- Filmüberzug: Hydroxypropylmethylcellulose, Polyethylenglycol 6000, Titandioxid, Dimethicon, Talkum.
Darstellungsbeschreibung und Packungsinhalt freilegen
Karton: 30 Filmtabletten zu 50 mg zur oralen Anwendung
Karton: 30 Filmtabletten zu 100 mg zum Einnehmen
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu haben, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS
AUFDECKEN
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Jede 50 mg Filmtablette enthält:
Kern
Wirkprinzip
Eperisonhydrochlorid 50 mg
Jede 100 mg Filmtablette enthält:
Kern
Wirkprinzip
Eperisonhydrochlorid 100 mg
Die vollständige Auflistung der sonstigen Bestandteile finden Sie in Abschnitt 6.1.
03.0 DARREICHUNGSFORM
Filmtabletten
04.0 KLINISCHE INFORMATIONEN
04.1 Anwendungsgebiete
Spastik bei Multipler Sklerose und Spastik bei Rückenmarkserkrankungen infektiöser, degenerativer, traumatischer oder neoplastischer Natur. Spastik zerebralen Ursprungs.
Muskelkontrakturen infolge osteoarthromuskulärer Pathologien (Zervikalarthrose, Schulterblatt-Humerus-Periarthritis, Lumbosciatalgie, Myalgie im Allgemeinen).
04.2 Dosierung und Art der Anwendung
Erwachsene :
Zur Behandlung von Spastik beträgt die empfohlene Dosierung 300 mg pro Tag:
• 1 Tablette mit 100 mg 3-mal täglich nach den Mahlzeiten.
Zur Behandlung von osteoarthromuskulären Erkrankungen beträgt die empfohlene Dosierung je nach Schwere der Symptome 150-300 mg pro Tag:
• 3-mal täglich 1 Tablette zu 50 mg oder 100 mg nach den Mahlzeiten.
Senioren
Bei älteren Patienten sollten bei Vorliegen einer eingeschränkten Leber- und/oder Nierenfunktion therapeutische Maßnahmen wie eine Dosisreduktion unter engmaschiger Überwachung ergriffen werden.
Es wird empfohlen, die Tagesdosis von 150 mg nicht zu überschreiten.
Kinder
Die Anwendung von Expose bei Kindern wird aufgrund fehlender klinischer Daten zur Festlegung der Anwendungsmodalitäten im pädiatrischen Bereich nicht empfohlen.
04.3 Kontraindikationen
Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile.
Schwangerschaft und Stillzeit. Schwere Leberinsuffizienz.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung
Bei Leber- und/oder Nierenpatienten wird empfohlen, die Leber- und/oder Nierenfunktion zu überwachen.
Obwohl beim Menschen keine signifikanten Veränderungen der hämatologischen Parameter und der Leberfunktion beobachtet wurden, wird es dennoch als sinnvoll erachtet, bei Langzeittherapien regelmäßige Kontrollen durchzuführen.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Besondere Vorsicht und Wachsamkeit des Arztes wird bei gleichzeitiger Therapie mit Salicylaten empfohlen, da deren Blutspiegel durch die gleichzeitige Gabe von Eperison gesenkt werden. Ähnliche Vorsicht ist bei gleichzeitiger Behandlung mit Calciumkanalblockern geboten, deren blutdrucksenkende Wirkung verstärkt werden kann.
04.6 Schwangerschaft und Stillzeit
Auch wenn der Komplex der an Tieren durchgeführten Studien kein spezifisches teratogenes Potenzial von Eperison hervorhebt, ist das Medikament während der Schwangerschaft und Stillzeit kontraindiziert.
Wenn Expose eingenommen werden soll, muss das Stillen beendet werden.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Besondere Vorsicht wird bei Patienten empfohlen, die Fahrzeuge oder andere Maschinen lenken, da das Arzneimittel die Aufmerksamkeit verringern kann.
04.8 Nebenwirkungen
Da Schocks und anaphylaktoide Reaktionen auftreten können, sollten die Patienten engmaschig überwacht werden. Bei Symptomen wie Rötung, Juckreiz, Nesselsucht, Ödemen des Gesichts oder anderer Teile und Atemnot sollte die Behandlung abgebrochen und geeignete Maßnahmen ergriffen werden.
Es können schwerwiegende Hauterkrankungen wie das okulo-mukokutane Syndrom (Steven-Johnson-Syndrom) oder die toxische epidermale Nekrolyse (Lyell-Syndrom) auftreten. Bei Symptomen wie Fieber, Erythem, Blasen, Juckreiz, Augenstau oder Stomatitis usw. sollte die Behandlung abgebrochen und geeignete Maßnahmen ergriffen werden.
Die Nebenwirkungen im Zusammenhang mit Expose, die in klinischen Studien und nach der Markteinführung bei über 12.000 Patienten berichtet wurden, wurden nach Organsystem und Häufigkeit nach folgendem Schema klassifiziert:
sehr häufig > 1/10
üblich > 1/100
ungewöhnlich > 1 / 1.000
selten> 1 / 10.000
sehr selten
Diagnosetest
Häufig: Erhöhte Blutspiegel von AST, ALT und alkalischer Phosphatase
Gelegentlich: Erhöhte Harnstoff-Stickstoffspiegel im Blut
Herzerkrankungen
Häufig: Herzklopfen
Erkrankungen des Blut- und Lymphsystems
Gelegentlich: Anämie
Erkrankungen des Nervensystems
Sehr häufig: Somnolenz, Kopfschmerzen, Verwirrung
Häufig: Schwindel, Schwindel, Stimmungsschwankungen, Zittern (in den Gliedmaßen), Hypästhesie
Gastrointestinale Störungen
Sehr häufig: Bauchschmerzen, Durchfall, Übelkeit, Erbrechen, Verstopfung, Magenbeschwerden, Dyspepsie
Häufig: Stomatitis, Bauchschwellung
Nieren- und Harnwegserkrankungen
Häufig: Harninkontinenz, Harnverhalt
Gelegentlich: Gefühl von Restharn, Proteinurie
Erkrankungen der Haut und des Unterhautzellgewebes
Sehr häufig: Hautausschlag
Häufig: Pruritus, Hyperhidrose
Sehr selten: Okulo-mukokutanes Syndrom (Steven-Johnson-Syndrom), toxische epidermale Nekrolyse (Lyell-Syndrom),
Muskel-Skelett- und Bindegewebserkrankungen
Häufig: Muskelsteifheit, Hypotonie
Stoffwechsel- und Ernährungsstörungen
Sehr häufig: Anorexie
Gefäßpathologien
Häufig: Hitzewallungen
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Sehr häufig: Asthenie, Müdigkeit
Häufig: Ödeme, Durst
Störungen des Immunsystems
Sehr selten: Schock und anaphylaktoide Reaktionen
Psychische Störungen
Sehr häufig: Schlaflosigkeit
Die mit Expose verbundenen Nebenwirkungen sind im Allgemeinen vorübergehend und erfordern keine spezielle Behandlung.
04.9 Überdosierung
Im Falle einer versehentlichen Überdosierung kann es zu Muskelhypotonie kommen, die auch die Atemmuskulatur betreffen kann, obwohl solche Wirkungen in der Literatur nicht beschrieben sind.
Da keine spezifischen Gegenmittel bekannt sind, ist es ratsam, die am besten geeigneten Gegenmaßnahmen wie Magenspülung und Kontrolle der Atem- und Herzfunktion zu ergreifen.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN
05.1 Pharmakodynamische Eigenschaften
Eperison-Hydrochlorid ist ein Mehrzweck-Muskelrelaxans, das einen völlig neuen Mechanismus zur Behandlung von Spastik, Muskelkontraktur und damit verbundenen Schmerzen bietet.
Seine Wirkung wird durch eine Reihe von synergistischen Aktionen ausgedrückt:
• Hemmung der spontanen Entladung spinaler Motoneuronen durch direktes Eingreifen in die Mechanismen, die für die Regulierung des Muskeltonus verantwortlich sind;
• erhöhter Blutfluss in Bereichen mit Muskelhypertonus durch eine Wirkung auf spannungsabhängige Calciumkanäle und auf Calmodulin auf der Ebene der glatten Muskelzellen;
• analgetische Aktivität dank seiner Wirkung als Antagonist der Substanz P auf Wirbelsäulenebene.
05.2 Pharmakokinetische Eigenschaften
Eperison wird schnell aus dem Magen-Darm-Trakt resorbiert und erreicht eine Cmax nach 1,6-2 Stunden mit einer Plasmahalbwertszeit von 1,59 Stunden.
Eperison wird in der Leber in verschiedene inaktive Metaboliten umgewandelt, die zu 76,6 % über die Nieren und zu 23,4 % über den Stuhl ausgeschieden werden.
Bei älteren Menschen ist die Kinetik mit einer Plasmahalbwertszeit von 2,57 Stunden langsamer.
Bei Patienten mit Leberzirrhose beträgt die Plasmahalbwertszeit 6,6 Stunden, bei Patienten mit schwerer Niereninsuffizienz (Kreatinin größer als 2 mg/100 ml) betrug die Halbwertszeit 6,56 Stunden.
Diese Daten sollten bei der Dosisanpassung bei längerer Behandlung bei älteren Patienten und bei Patienten mit Leberzirrhose und Niereninsuffizienz berücksichtigt werden.
05.3 Präklinische Sicherheitsdaten
Akute, subakute und chronische Toxizitätsstudien wurden an Ratten, Mäusen und Hunden bis zu höheren Dosierungen als den pharmakodynamisch wirksamen durchgeführt. Die durchgeführten histopathologischen Untersuchungen ergaben keine nennenswerten Veränderungen. Bei Dosen bis zum 10-fachen der beim Menschen angewendeten Höchstdosis wurde keine teratogene Wirkung gezeigt, Mutagenitätstests waren negativ.
06.0 PHARMAZEUTISCHE INFORMATIONEN
06.1 Hilfsstoffe
Maisstärke, mikrokristalline Cellulose, vernetzte Natriumcarboxymethylcellulose, Hydroxypropylcellulose, Calciumstearat.
Filmüberzug: Hydroxypropylmethylcellulose, Polyethylenglycol 6000, Titandioxid, Dimethicone, Talkum.
06.2 Inkompatibilität
Keine bekannt
06.3 Gültigkeitsdauer
2 Jahre.
Das angegebene Verfallsdatum bezieht sich auf das Produkt in intakter Verpackung, richtig gelagert.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
100 mg Filmtabletten aussetzen:
Bei einer Temperatur von nicht mehr als 30 ° C lagern.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks
100 mg Filmtabletten aussetzen
PVC / PE / PVDC- Al Blister
Schachtel mit 30 Filmtabletten von 100 mg
50 mg Filmtabletten aussetzen
Blister aus bernsteinfarbenem Al / PVC / PVDC gekoppeltem Material.
Schachtel mit 30 Filmtabletten von 50 mg
06.6 Gebrauchs- und Handhabungshinweise
Keine besonderen Anweisungen.
07.0 INHABER DER MARKETING-ERLAUBNIS
EISAI s.r.l.
Via dell Unione Europea 6 / B - San Donato Milanese (MI)
Händler zu verkaufen
Alfa Wassermann S.p.A
Via Enrico Fermi, 1 - 65020 Alanno (PE)
08.0 NUMMER DER MARKETING-ERLAUBNIS
30 Filmtabletten 50 mg A.I.C. n. 028631012
30 Filmtabletten 100 mg A.I.C. n. 028631024
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG
Erstzulassung: 12. April 2000
Erneuerung der Zulassung: 20. Mai 2005
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs
April 2009