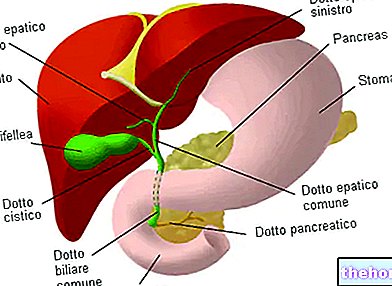
Wirkstoffe: Nimodipin
NIMOTOP 30 mg überzogene Tabletten
NIMOTOP 30 mg / 0,75 ml Tropfen zum Einnehmen, Lösung
Nimotop Packungsbeilagen sind erhältlich für Packungsgrößen: - NIMOTOP 30 mg Dragees, NIMOTOP 30 mg / 0,75 ml Tropfen zum Einnehmen, Lösung
- NIMOTOP 10 mg / 50 ml Lösung zur intravenösen Infusion
Indikationen Warum wird Nimotop verwendet? Wofür ist das?
Pharmakotherapeutische Gruppe
Selektiver Kalziumkanalblocker; Dihydropyridin-Derivat
Therapeutische Hinweise
Prävention und Therapie ischämischer neurologischer Defizite im Zusammenhang mit zerebralem Vasospasmus.
Kontraindikationen Wenn Nimotop nicht verwendet werden sollte
Nimotop darf während der Schwangerschaft oder Stillzeit sowie bei Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile nicht angewendet werden.
Nimotop sollte nicht gleichzeitig mit Rifampicin angewendet werden, da die gleichzeitige Anwendung von Rifampicin die Wirksamkeit von Nimodipin signifikant verringern kann (siehe Abschnitt „Wechselwirkungen“).
Eine stark eingeschränkte Leberfunktion und insbesondere eine Leberzirrhose können aufgrund einer Abnahme des First-Pass-Effekts und der metabolischen Clearance zu einer Erhöhung der Bioverfügbarkeit von Nimodipin führen.Aus diesem Grund sollte Nimotop nicht bei Patienten mit Leberfunktion angewendet werden (zB Leberzirrhose).
Die gleichzeitige Behandlung mit oralem Nimodipin und Antiepileptika wie Phenobarbital, Phenytoin oder Carbamazepin ist kontraindiziert, da die gleichzeitige Anwendung dieser Arzneimittel die Wirksamkeit von Nimodipin signifikant verringern kann (siehe „Wechselwirkungen“).
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Nimotop® beachten?
Bei sehr älteren Patienten mit multiplen Erkrankungen, bei stark eingeschränkter Nierenfunktion (glomeruläre Filtration <20 ml/min) und bei Patienten mit stark eingeschränkter kardiovaskulärer Funktion ist die Notwendigkeit einer Behandlung mit Nimotop mit Vorsicht abzuwägen und der Patient sollte regelmäßig kontrolliert werden.
Obwohl es keine Hinweise darauf gibt, dass die Behandlung mit Nimotop mit einer Erhöhung des Hirndrucks einhergeht, wird in diesen Fällen oder bei Zuständen, die durch einen deutlichen Anstieg des Wassergehalts des Hirngewebes (generalisiertes Hirnödem) gekennzeichnet sind, eine sorgfältige Überwachung empfohlen.
Nimotop sollte auch bei hypotensiven Patienten (systolischer Blutdruck < 100 mmHg) mit Vorsicht angewendet werden.
Bei Patienten mit instabiler Angina pectoris oder in den ersten 4 Wochen nach einem akuten Myokardinfarkt sollte der Arzt das potenzielle Risiko (verminderte Koronarperfusion und Myokardischämie) im Verhältnis zum erwarteten Nutzen (verbesserte zerebrale Perfusion) abwägen.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Nimotop® beeinflussen?
Informieren Sie Ihren Arzt (oder Apotheker), wenn Sie vor kurzem andere nicht verschreibungspflichtige Arzneimittel eingenommen haben.
Auswirkungen anderer Medikamente auf Nimodipin
Nimodipin wird über das Cytochrom P450 3A4-System metabolisiert, das sich sowohl in der Darmschleimhaut als auch in der Leber befindet. Arzneimittel, von denen bekannt ist, dass sie dieses Enzymsystem hemmen oder induzieren, können daher den First-Pass-Effekt (nach oraler Gabe) oder die Clearance von Nimodipin verändern (siehe „Dosis, Art und Zeitpunkt der Anwendung“).
Das Ausmaß und die Dauer dieser Wechselwirkung sollten berücksichtigt werden, wenn Nimodipin gleichzeitig mit den folgenden Arzneimitteln angewendet wird:
Rifampicin
Erfahrungen mit anderen Calciumkanalblockern deuten darauf hin, dass Rifampicin den Stoffwechsel von Nimodipin durch einen Enzyminduktionsprozess beschleunigt.
Daher könnte die Wirksamkeit von Nimodipin bei gleichzeitiger Anwendung mit Rifampicin signifikant reduziert werden.
Die Anwendung von Nimodipin mit Rifampicin ist daher kontraindiziert (siehe „Gegenanzeigen“).
Antiepileptika, die das Cytochrom P450 3A4-System induzieren, wie Phenobarbital, Phenytoin oder Carbamazepin
Eine vorangegangene chronische Therapie mit den Antiepileptika Phenobarbital, Phenytoin oder Carbamazepin reduziert die Bioverfügbarkeit von oral verabreichtem Nimodipin deutlich. Daher ist eine gleichzeitige Behandlung mit diesen Arzneimitteln und oralem Nimodipin kontraindiziert (siehe „Gegenanzeigen“).
Inhibitoren des Cytochrom P450 3A4-Systems
Bei gleichzeitiger Anwendung mit den folgenden Inhibitoren des Cytochrom-P450-3A4-Systems sollte der Blutdruck überwacht und gegebenenfalls eine Reduzierung der Nimodipin-Dosis in Erwägung gezogen werden (siehe „Dosis, Art und Zeitpunkt der Anwendung“).
Makrolid-Antibiotika (z. B. Erythromycin)
Es wurden keine Wechselwirkungsstudien zwischen Makrolid-Antibiotika und Nimodipin durchgeführt. Einige Makrolid-Antibiotika sind bekannte Inhibitoren des Cytochrom-P450-3A4-Systems und die Möglichkeit einer Interaktion auf dieser Ebene kann nicht ausgeschlossen werden. Daher sollten Makrolid-Antibiotika nicht in Kombination mit Nimodipin angewendet werden (siehe „Warnhinweise“).
Obwohl Azithromycin strukturell mit der Makrolidklasse von Antibiotika verwandt ist, ist es kein Inhibitor des Cytochrom-CYP 3A4-Systems.
HIV-Proteasehemmer (z. B. Ritonavir)
Es wurden keine vollwertigen Studien durchgeführt, um die potenzielle Wechselwirkung zwischen Nimodipin und Anti-HIV-Protease-Inhibitoren zu untersuchen. Von bestimmten Arzneimitteln dieser Klasse wurde berichtet, dass sie starke Inhibitoren des Cytochrom-P450-3A4-Systems sind. Aus diesem Grund kann die Möglichkeit eines deutlichen und klinisch relevanten Anstiegs der Plasmakonzentration von Nimodipin bei gleichzeitiger Verabreichung mit einem dieser Arzneimittel nicht ausgeschlossen werden (siehe "Besondere Warnhinweise").
Azol-Antimykotika (z. B. Ketoconazol)
Es wurden keine vollwertigen Studien durchgeführt, um die potenzielle Wechselwirkung zwischen Nimodipin und Ketoconazol zu untersuchen. Es ist bekannt, dass Azol-Antimykotika das Cytochrom P450 3A4-System hemmen, und für andere Dihydropyridin-Calciumkanalblocker wurden verschiedene Wechselwirkungen berichtet. Daher kann bei gleichzeitiger Anwendung mit oralem Nimodipin eine erhebliche Erhöhung der systemischen Bioverfügbarkeit nicht ausgeschlossen werden Abnahme des First-Pass-Metabolismus (siehe „Besondere Warnhinweise“).
Nefazodon
Es wurden keine vollwertigen Studien durchgeführt, um die potenzielle Wechselwirkung zwischen Nimodipin und Nefazodon zu untersuchen. Dieses Antidepressivum ist als potenter Inhibitor des Cytochrom-P450-3A4-Systems bekannt. Daher kann bei gleichzeitiger Anwendung von Nefazodon mit Nimodipin ein erheblicher Anstieg der Plasmakonzentration von Nimodipin nicht ausgeschlossen werden (siehe „Warnhinweise und Vorsichtsmaßnahmen“).
Fluoxetin
Die gleichzeitige Anwendung von Nimodipin mit dem Antidepressivum Fluoxetin im Steady State führte zu einem Anstieg der Plasmaspiegel von Nimodipin um etwa 50 %. Die Konzentration von Fluoxetin war deutlich verringert, während die Konzentration seines aktiven Metaboliten Norfluoxetin nicht beeinflusst wurde (siehe „Besondere Warnhinweise“ ").
Quinupristin / Dalfopristin
Basierend auf den Erfahrungen mit dem Calciumkanalblocker Nifedipin kann die gleichzeitige Anwendung von Nimodipin und Quinupristin/Dalfopristin zu erhöhten Plasmakonzentrationen von Nimodipin führen (siehe „Warnhinweise“).
Cimetidin
Die gleichzeitige Anwendung von Nimodipin und Cimetidin (einem H2-Antagonisten) kann zu einem Anstieg der Plasmakonzentration von Nimodipin führen (siehe „Warnhinweise“).
Valproinsäure
Die gleichzeitige Anwendung von Nimodipin und Valproinsäure (ein Antikonvulsivum) kann zu einem Anstieg der Plasmakonzentration von Nimodipin führen (siehe „Warnhinweise“).
Weitere Interaktionen
Nortriptyline
Die gleichzeitige Anwendung von Nimodipin und Nortriptylin im Steady State führte zu einer leichten Abnahme der Nimodipin-Konzentration, ohne die Plasmaspiegel von Nortriptylin zu beeinflussen.
Auswirkungen von Nimodipin auf andere Medikamente
Antihypertensiva
Nimodipin kann die blutdrucksenkende Wirkung gleichzeitig verabreichter blutdrucksenkender Arzneimittel verstärken, wie zum Beispiel:
- Diuretika
- β-Blocker
- ACE-Hemmer
- A1-Antagonisten
- andere Kalziumkanalblocker
- α-Blocker
- PDE5-Hemmer
- α-Methyldopa
Ist ein solcher Zusammenhang unvermeidbar, ist eine besonders sorgfältige Patientenüberwachung erforderlich.
Zidovudin
In einer Studie an Affen führte die gleichzeitige intravenöse Verabreichung des Anti-HIV-Medikaments Zidovudin und des Bolus Nimodipin zu einem signifikanten Anstieg der AUC von Zidovudin mit einer signifikanten Verringerung seines Verteilungsvolumens und seiner Clearance.
Wechselwirkungen mit Lebensmitteln
Grapefruitsaft
Grapefruitsaft hemmt das Cytochrom P450 3A4-System.
Die gleichzeitige Einnahme von Grapefruitsaft und Diiprodipyridin-Calciumkanalblockern erhöht deren Plasmakonzentration und Wirkungsdauer aufgrund einer Verminderung ihres First-Pass-Metabolismus oder ihrer Clearance, wodurch die blutdrucksenkende Wirkung von Nimodipin verstärkt werden kann . Dieses Phänomen kann nach der letzten Einnahme von Grapefruitsaft noch mindestens 4 Tage andauern. Die Einnahme von Grapefruit oder Grapefruitsaft sollte daher während der Behandlung mit Nimodipin vermieden werden (siehe „Dosis, Art und Zeitpunkt der Anwendung“).
Fälle, in denen eine Interaktion nicht hervorgehoben wurde
Haloperidol
Die gleichzeitige Anwendung von Nimodipin im Steady-State an Patienten unter Langzeitbehandlung mit Haloperidol zeigte kein Potenzial für gegenseitige Wechselwirkungen.
Die gleichzeitige Anwendung von oralem Nimodipin und Diazepam, Digoxin, Glibenclamid, Indomethacin, Ranitidin und Warfarin zeigte keine potenziellen gegenseitigen Wechselwirkungen.
Warnungen Es ist wichtig zu wissen, dass:
Nimodipin wird über das Cytochrom P450 3A4-System metabolisiert. Arzneimittel, von denen bekannt ist, dass sie dieses Enzymsystem hemmen oder induzieren, können daher den First-Pass-Effekt oder die Clearance von Nimodipin verändern (siehe „Wechselwirkungen“ und „Dosis, Art und Zeitpunkt der Anwendung“).
Arzneimittel, von denen bekannt ist, dass sie das Cytochrom P450 3A4-System hemmen und daher einen Anstieg der Plasmakonzentration von Nimodipin verursachen können, sind zum Beispiel:
- Makrolid-Antibiotika (z. B. Erythromycin)
- HIV-Proteasehemmer (z. B. Ritonavir)
- Azol-Antimykotika (z. B. Ketoconazol)
- die Antidepressiva Nefazodon und Fluoxetin
- Quinupristin / Dalfopristin
- Cimetidin
- Valproinsäure.
Bei gleichzeitiger Anwendung mit diesen Arzneimitteln sollte der Blutdruck überwacht und gegebenenfalls eine Reduzierung der Nimodipin-Dosis in Erwägung gezogen werden.
Zusätzlich für Nimodipin Lösung zum Einnehmen:
Nimotop 30 mg / 0,75 ml Tropfen zum Einnehmen enthält 48,06 Vol.-% Ethanol (Alkohol), was 4,3 g pro Tagesdosis (9 ml) entspricht. Dies kann für alkoholkranke oder alkoholstoffwechselgestörte Personen schädlich sein und sollte auch bei Schwangeren oder Stillenden, Kindern und Risikogruppen wie Patienten mit Lebererkrankungen oder Epilepsie berücksichtigt werden dieses Arzneimittel kann die Wirkung anderer Arzneimittel verändern (siehe „Wechselwirkungen“) sowie die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen (siehe „Fahrtüchtigkeit und die Fähigkeit zum Bedienen von Maschinen“). Dieses Arzneimittel enthält auch hydriertes mehrwertiges Rizinusöl, das Magenverstimmung und Durchfall verursachen kann.
Schwangerschaft und Stillzeit
Fragen Sie vor der Einnahme von Arzneimitteln Ihren Arzt oder Apotheker um Rat.
Schwangerschaft
Es liegen keine ausreichend kontrollierten Studien bei Schwangeren vor. Wenn die Anwendung von Nimotop während der Schwangerschaft als notwendig erachtet wird, sollten der erwartete Nutzen und die potenziellen Risiken in Abhängigkeit vom Schweregrad des klinischen Bildes sorgfältig abgewogen werden.
Fütterungszeit
Es wurde gezeigt, dass Nimodipin und seine Metaboliten in einer Konzentration in der gleichen Größenordnung wie im mütterlichen Plasma in die Muttermilch ausgeschieden werden Müttern wird empfohlen, während der Einnahme des Arzneimittels nicht zu stillen.
Fruchtbarkeit
In Einzelfällen der In-vitro-Fertilisation wurden Calciumkanalblocker mit reversiblen biochemischen Veränderungen im Spermienkopf in Verbindung gebracht, die möglicherweise zu einer Beeinträchtigung der Spermienfunktion führten. Die Relevanz dieses Befundes für die Kurzzeitbehandlung ist nicht bekannt
Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Grundsätzlich kann die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durch das mögliche Auftreten von Schwindel beeinträchtigt sein.
Zusätzlich für Nimotop Tropfen zum Einnehmen, Lösung:
Die Alkoholmenge in diesem Arzneimittel kann Ihre Verkehrstüchtigkeit und Ihre Fähigkeit zum Bedienen von Maschinen beeinträchtigen (siehe „Warnhinweise“).
Für Sportbegeisterte:
Die Anwendung von ethylalkoholhaltigen Arzneimitteln kann positive Dopingtests in Bezug auf die von einigen Sportverbänden angegebenen Grenzwerte für die Alkoholkonzentration ergeben.
Dosierung und Art der Anwendung Wie ist Nimotop anzuwenden: Dosierung
Dosierung
Sofern nicht anders verordnet, beträgt die durchschnittliche Tagesdosis 30 mg x 3-mal (1 Tablette x 3-mal oder 0,75 ml Lösung x 3-mal).
Bei Nimotop 30 mg / 0,75 ml Tropfen zum Einnehmen, Lösung entsprechen 0,75 ml Lösung 30 mg Nimodipin und entsprechen dem bis zur Markierung gefüllten Tropfer.
Bei Patienten, bei denen Nebenwirkungen auftreten, sollte die Dosis nach Bedarf reduziert oder die Behandlung abgebrochen werden.
Bei gleichzeitiger Anwendung mit Inhibitoren oder Induktoren des CYP 3A4-Systems kann eine Dosisanpassung erforderlich sein (siehe „Wechselwirkungen“).
Bei der Prophylaxe und Behandlung von ischämischen neurologischen Defiziten infolge eines durch eine Subarachnoidalblutung induzierten zerebralen Vasospasmus wird empfohlen, nach einer parenteralen Therapie die orale Gabe von Nimodipin etwa 7 Tage lang fortzusetzen (60 mg - 2 Tabletten à 30 mg oder 1,5 ml .). Lösung entsprechend 2 bis zur Marke gefüllten Tropfer - 6-mal täglich in 4-Stunden-Intervallen
Besondere Bevölkerungsgruppen
Die Sicherheit und Wirksamkeit von Nimotop bei Patienten unter 18 Jahren ist nicht erwiesen.
Patienten mit eingeschränkter Leberfunktion
Eine stark eingeschränkte Leberfunktion, insbesondere eine Leberzirrhose, kann aufgrund einer Abnahme des First-Pass-Effekts und der metabolischen Clearance zu einer Erhöhung der Bioverfügbarkeit von Nimodipin führen.Pharmakologische Wirkungen und Nebenwirkungen wie Blutdrucksenkung können bei diesen Patienten stärker ausgeprägt sein.
In diesen Fällen sollte die Dosis reduziert oder, falls erforderlich, ein Absetzen der Behandlung in Erwägung gezogen werden.
Patienten mit eingeschränkter Nierenfunktion
Bei Patienten mit stark eingeschränkter Nierenfunktion (glomeruläre Filtration <20 ml/min) sollte die Notwendigkeit einer Behandlung mit Nimotop mit Vorsicht betrachtet und der Patient regelmäßig überwacht werden.
Bei schwerer Nierenfunktionsstörung können Nebenwirkungen wie Blutdrucksenkung stärker ausgeprägt sein, in diesen Fällen sollte gegebenenfalls die Dosis reduziert oder die Behandlung abgebrochen werden.
Art der Verabreichung
Nimotop sollte zwischen den Mahlzeiten eingenommen werden, wobei die Tabletten mit etwas Flüssigkeit und den Tropfen in etwas Wasser verdünnt eingenommen werden.
Nicht zusammen mit Grapefruitsaft einnehmen (siehe „Wechselwirkungen“).
Tauchen Sie die Pipette nicht in Wasser und spülen Sie sie nicht aus.
Nachdem Sie die Tropfen in das Wasser gegeben haben, geben Sie die Pipette wieder in die Flasche.
Das Intervall zwischen den einzelnen Verabreichungen sollte nicht weniger als 4 Stunden betragen.
Überdosierung Was ist zu tun, wenn Sie zu viel Nimotop® eingenommen haben?
Vergiftungssymptome:
Akute Überdosierungssymptome, die berücksichtigt werden müssen, sind: ausgeprägte Hypotonie, Tachykardie oder Bradykardie; Magen-Darm-Störungen und Übelkeit.
Behandlung von Vergiftungen
Im Falle einer akuten Überdosierung sollte die Gabe von Nimodipin sofort abgebrochen werden. Sofortmaßnahmen müssen darauf abzielen, die Symptome zu beseitigen.
Als Notfallmaßnahme kann eine Magenspülung unter Zusatz von Aktivkohle in Betracht gezogen werden. Bei schwerer Hypotonie können Dopamin oder Noradrenalin intravenös verabreicht werden. Da kein spezifisches Antidot bekannt ist, sollte die Behandlung von Nebenwirkungen darauf abzielen, die Hauptsymptome zu beseitigen.
Im Falle einer versehentlichen Einnahme / Einnahme einer übermäßigen Dosis von Nimotop benachrichtigen Sie sofort Ihren Arzt oder begeben Sie sich in das nächste Krankenhaus.
KONTAKTIEREN SIE IHREN ARZT ODER APOTHEKER, WENN SIE ZWEIFEL ÜBER DIE VERWENDUNG VON NIMOTOP HABEN.
Nebenwirkungen Was sind die Nebenwirkungen von Nimotop
Wie alle Arzneimittel kann Nimotop Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Tabelle 1 listet die Nebenwirkungen, die mit Nimodipin in klinischen Studien mit Nimodipin berichtet wurden, unter der Indikation „Prävention und Therapie ischämischer neurologischer Defizite im Zusammenhang mit cerebralem Vasospasmus induziert durch Subarachnoidalblutung“ auf, sortiert nach Häufigkeitskategorien nach CIOMS III Studien 703 Patienten wurden mit Nimodipin und 692 mit Placebo behandelt, in den unkontrollierten Studien wurden 2.496 Patienten mit Nimodipin behandelt, Stand 31.08.2005).
Innerhalb jeder Häufigkeitsklasse werden Nebenwirkungen in absteigender Reihenfolge ihres Schweregrades berichtet.
Die Frequenzen sind wie folgt definiert:
sehr häufig (≥ 1/10)
häufig (≥ 1/100 bis < 1/10),
gelegentlich (≥ 1 / 1.000 bis < 1/100),
selten (≥ 1 / 10.000 bis < 1 / 1.000),
sehr selten (<1 / 10.000).
Tabelle 1: Unerwünschte Arzneimittelwirkungen, die bei Patienten in klinischen Studien unter der Indikation „Prävention und Behandlung ischämischer neurologischer Defizite im Zusammenhang mit zerebralem Vasospasmus“ berichtet wurden.
Tabelle 2 listet die Nebenwirkungen, die mit Nimodipin in klinischen Studien mit Nimodipin unter der Indikation „Behandlung ischämischer neurologischer Defizite (impaired brain function in the senior, IBFO)“ und unter „Post-Marketing-Erfahrungen“ berichtet wurden, auf, sortiert nach Häufigkeitskategorien nach zu CIOMS III (in den placebokontrollierten Studien wurden 1.594 Patienten mit Nimodipin und 1.558 mit Placebo behandelt; in den unkontrollierten Studien wurden 8.049 Patienten mit Nimodipin behandelt; Stand 20.10.2005).
Innerhalb jeder Häufigkeitsklasse werden Nebenwirkungen in absteigender Reihenfolge ihres Schweregrades berichtet.
Die Frequenzen sind wie folgt definiert:
häufig (≥ 1/100 bis < 1/10),
gelegentlich (≥ 1 / 1.000 bis < 1/100),
selten (≥ 1 / 10.000 bis < 1 / 1.000),
sehr selten (<1 / 10.000).
Tabelle 2: Nebenwirkungen, die bei Patienten in klinischen Studien zur „Behandlung von ischämischen neurologischen Defiziten (beeinträchtigte Gehirnfunktion bei älteren Menschen, IBFO)“ berichtet wurden
Die Einhaltung der Anweisungen in der Packungsbeilage verringert das Risiko von Nebenwirkungen.
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker, wenn Sie Nebenwirkungen bemerken, die nicht in dieser Packungsbeilage aufgeführt sind.
Ablauf und Aufbewahrung
Verfallsdatum: siehe das auf der Verpackung aufgedruckte Verfallsdatum.
Das Verfallsdatum bezieht sich auf das Produkt in intakter Verpackung, richtig gelagert.
Achtung: Verwenden Sie das Arzneimittel nicht nach dem auf der Packung angegebenen Verfallsdatum.
Das Ablaufdatum bezieht sich auf den letzten Tag des Monats.
Besondere Vorsichtsmaßnahmen für die Lagerung
Tabletten: keine
Tropfen zum Einnehmen, Lösung: vor Licht schützen / nicht kühlen
Arzneimittel dürfen nicht über das Abwasser oder den Hausmüll entsorgt werden. Fragen Sie Ihren Apotheker, wie Arzneimittel zu entsorgen sind, die Sie nicht mehr verwenden. Dies trägt zum Schutz der Umwelt bei.
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Komposition
NIMOTOP 30 mg überzogene Tabletten
eine überzogene Tablette enthält:
Wirkstoff: Nimodipin 30 mg.
Sonstige Bestandteile: mikrogranuläre Cellulose, Povidon, Crospovidon, Magnesiumstearat, Maisstärke, Hypromellose, Macrogol 4000, Titandioxid, gelbes Eisenoxid.
NIMOTOP 30 mg / 0,75 ml Tropfen zum Einnehmen, Lösung
0,75 ml Nimotop Tropfen zum Einnehmen enthalten:
Wirkstoff: Nimodipin 30 mg.
Hilfsstoffe: gehärtetes mehrwertiges Rizinusöl, Ethylalkohol.
Darreichungsform und Inhalt
36 überzogene Tabletten von 30 mg
1 Flasche 25 ml Tropfen zum Einnehmen mit Tropfer.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu erhalten, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS
NIMOTOP
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
NIMOTOP 30 mg überzogene Tabletten Eine überzogene Tablette enthält:
Wirkstoff: Nimodipin 30 mg.
NIMOTOP 30 mg / 0,75 ml Tropfen zum Einnehmen, Lösung 0,75 ml Lösung enthalten:
Wirkstoff: Nimodipin 30 mg.
Die vollständige Auflistung der sonstigen Bestandteile finden Sie in Abschnitt 6.1.
03.0 DARREICHUNGSFORM
Beschichtete Tablette. Tropfen zum Einnehmen, Lösung.
04.0 KLINISCHE INFORMATIONEN
04.1 Anwendungsgebiete
Prävention und Therapie ischämischer neurologischer Defizite im Zusammenhang mit zerebralem Vasospasmus.
04.2 Dosierung und Art der Anwendung
Besondere Bevölkerungsgruppen
Die Sicherheit und Wirksamkeit von Nimotop bei Patienten unter 18 Jahren ist nicht erwiesen.
Dosierung
Sofern nicht anders verordnet, beträgt die empfohlene Tagesdosis 30 mg x 3-mal (1 Tablette oder 0,75 ml Lösung x 3-mal). 0,75 ml Lösung entsprechen 30 mg Nimodipin und entsprechen einer bis zur Markierung gefüllten Pipette.
Bei Patienten, bei denen Nebenwirkungen auftreten, sollte die Dosis nach Bedarf reduziert oder die Behandlung abgebrochen werden.
Bei gleichzeitiger Anwendung mit Inhibitoren oder Induktoren des CYP 3A4-Systems kann eine Dosisanpassung erforderlich sein (siehe Abschnitt 4.5).
Bei der Prophylaxe und Behandlung von ischämischen neurologischen Defiziten infolge eines durch eine Subarachnoidalblutung induzierten zerebralen Vasospasmus wird empfohlen, nach einer parenteralen Therapie die orale Gabe von Nimodipin etwa 7 Tage lang fortzusetzen (60 mg - 2 Tabletten à 30 mg oder 1,5 ml .). Lösung, entsprechend 2 bis zur Marke gefüllten Tropfer - 6-mal täglich in 4-Stunden-Intervallen).
Patienten mit eingeschränkter Leberfunktion
Eine stark eingeschränkte Leberfunktion und insbesondere eine Leberzirrhose können aufgrund einer Abnahme des First-Pass-Effekts und der metabolischen Clearance zu einer Erhöhung der Bioverfügbarkeit von Nimodipin führen bei diesen Patienten.
In diesen Fällen sollte die Dosis reduziert oder, falls erforderlich, ein Absetzen der Behandlung in Erwägung gezogen werden.
Patienten mit eingeschränkter Nierenfunktion
Bei Patienten mit stark eingeschränkter Nierenfunktion (glomeruläre Filtration
Bei schwerer Nierenfunktionsstörung können Nebenwirkungen wie Blutdrucksenkung stärker ausgeprägt sein, in diesen Fällen sollte gegebenenfalls die Dosis reduziert oder die Behandlung abgebrochen werden.
Art der Verabreichung
Nimotop sollte zwischen den Mahlzeiten eingenommen werden, die Tabletten mit etwas Flüssigkeit, die Tropfen in etwas Wasser verdünnt.
Nicht zusammen mit Grapefruitsaft einnehmen (siehe Abschnitt 4.5).
Tauchen Sie die Pipette nicht in das Wasser und spülen Sie sie nicht aus. Nachdem Sie die Tropfen in das Wasser gegeben haben, geben Sie die Pipette in die Flasche zurück.
Das Intervall zwischen den einzelnen Verabreichungen sollte nicht weniger als 4 Stunden betragen.
04.3 Kontraindikationen
Nimotop darf während der Schwangerschaft oder Stillzeit sowie bei Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile nicht angewendet werden.
Die gleichzeitige Anwendung von Nimodipin mit Rifampicin ist kontraindiziert, da die gleichzeitige Anwendung von Rifampicin die Wirksamkeit von Nimodipin signifikant verringern kann (siehe Abschnitt 4.5).
Die gleichzeitige Behandlung mit oralem Nimodipin und Antiepileptika wie Phenobarbital, Phenytoin oder Carbamazepin ist kontraindiziert, da die gleichzeitige Anwendung dieser Arzneimittel die Wirksamkeit von Nimodipin signifikant verringern kann (siehe Abschnitt 4.5).
Eine stark eingeschränkte Leberfunktion und insbesondere eine Leberzirrhose können aufgrund einer Abnahme des First-Pass-Effekts und der metabolischen Clearance zu einer Erhöhung der Bioverfügbarkeit von Nimodipin führen bei diesen Patienten.
In diesen Fällen sollte die Dosis reduziert oder, falls erforderlich, ein Absetzen der Behandlung in Erwägung gezogen werden.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung
Bei sehr älteren Patienten mit multiplen Pathologien, bei stark eingeschränkter Nierenfunktion (glomeruläre Filtration
Obwohl es keine Hinweise darauf gibt, dass die Behandlung mit Nimotop mit einer Erhöhung des Hirndrucks einhergeht, wird in diesen Fällen oder bei Zuständen, die durch eine Erhöhung des Wassergehalts des Hirngewebes (generalisiertes Hirnödem) gekennzeichnet sind, eine sorgfältige Überwachung empfohlen.
Nimotop sollte auch bei hypotensiven Patienten (systolischer Blutdruck .) mit Vorsicht angewendet werden
Bei Patienten mit instabiler Angina pectoris oder in den ersten 4 Wochen nach einem akuten Myokardinfarkt sollte der Arzt das potenzielle Risiko (verminderte Koronarperfusion und Myokardischämie) im Verhältnis zum erwarteten Nutzen (verbesserte zerebrale Perfusion) abwägen.
Nimodipin wird über das Cytochrom P450 3A4-System metabolisiert. Arzneimittel, von denen bekannt ist, dass sie dieses Enzymsystem hemmen oder induzieren, können daher den First-Pass-Effekt oder die Clearance von Nimodipin verändern (siehe Abschnitte 4.2 und 4.5).
Arzneimittel, von denen bekannt ist, dass sie das Cytochrom P450 3A4-System hemmen und daher einen Anstieg der Plasmakonzentration von Nimodipin verursachen können, sind zum Beispiel:
- Makrolid-Antibiotika (z. B. Erythromycin)
- Anti-HIV-Protease-Hemmer (z. B. Ritonavir)
- Azol-Antimykotika (z. B. Ketoconazol)
- die Antidepressiva Nefazodon und Fluoxetin
- Quinupristin / Dalfopristin
- Cimetidin
- Valproinsäure.
Bei gleichzeitiger Anwendung dieser Arzneimittel sollte der Blutdruck überwacht und gegebenenfalls eine Reduzierung der Nimodipin-Dosis in Erwägung gezogen werden.
Zusätzlich für Nimodipin Lösung zum Einnehmen: Nimotop 30 mg / 0,75 ml Tropfen zum Einnehmen enthält 48,06 Vol.-% Ethanol (Alkohol), was bis zu 4,3 g pro Tagesdosis (9 ml) entspricht. Dies kann für alkoholkranke oder alkoholstoffwechselgestörte Personen schädlich sein und sollte auch bei Schwangeren oder Stillenden, Kindern und Risikogruppen wie Patienten mit Lebererkrankungen oder Epilepsie berücksichtigt werden Dieses Arzneimittel kann die Wirkung anderer Arzneimittel (siehe Abschnitt 4.5) sowie die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen verändern (siehe Abschnitt 4.7). Dieses Arzneimittel enthält auch hydriertes mehrwertiges Rizinusöl, das Magenverstimmung und Durchfall verursachen kann.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Auswirkungen anderer Medikamente auf Nimodipin
Nimodipin wird über das Cytochrom P450 3A4-System metabolisiert, das sich sowohl in der Darmschleimhaut als auch in der Leber befindet. Arzneimittel, von denen bekannt ist, dass sie dieses Enzymsystem hemmen oder induzieren, können daher den First-Pass-Effekt oder die Clearance von Nimodipin verändern (siehe Abschnitt 4.2).„Patienten mit eingeschränkter Leberfunktion“).
Das Ausmaß und die Dauer dieser Wechselwirkung sollten berücksichtigt werden, wenn Nimodipin gleichzeitig mit den folgenden Arzneimitteln angewendet wird:
Rifampicin
Erfahrungen mit anderen Calciumkanalblockern deuten darauf hin, dass Rifampicin den Stoffwechsel von Nimodipin durch einen Enzyminduktionsprozess beschleunigt. Daher könnte die Wirksamkeit von Nimodipin bei gleichzeitiger Anwendung mit Rifampicin signifikant reduziert werden.
Die Anwendung von Nimodipin zusammen mit Rifampicin ist daher kontraindiziert (siehe Abschnitt 4.3).
Antiepileptika, die das Cytochrom P450 3A4-System induzieren, wie Phenobarbital, Phenytoin oder Carbamazepin.
Eine vorangegangene chronische Therapie mit den Antiepileptika Phenobarbital, Phenytoin oder Carbamazepin reduziert die Bioverfügbarkeit von oral verabreichtem Nimodipin deutlich. Daher ist eine gleichzeitige Behandlung mit diesen Arzneimitteln und oralem Nimodipin kontraindiziert (siehe Abschnitt 4.3).
Inhibitoren des Cytochrom P450 3A4-Systems
Bei gleichzeitiger Anwendung mit den folgenden Inhibitoren des Cytochrom-P450-3A4-Systems sollte der Blutdruck überwacht und gegebenenfalls eine Dosisreduktion von Nimodipin in Erwägung gezogen werden (siehe Abschnitt 4.2).
Makrolid-Antibiotika (z. B. Erythromycin)
Es wurden keine Wechselwirkungsstudien zwischen Makrolid-Antibiotika und Nimodipin durchgeführt. Einige Makrolid-Antibiotika sind bekannte Inhibitoren des Cytochrom-P450-3A4-Systems und die Möglichkeit einer Interaktion auf dieser Ebene kann nicht ausgeschlossen werden. Daher sollten Makrolid-Antibiotika nicht in Kombination mit Nimodipin angewendet werden (siehe Abschnitt 4.4).
Obwohl Azithromycin strukturell mit der Makrolidklasse von Antibiotika verwandt ist, ist es kein Inhibitor des Cytochrom-CYP 3A4-Systems.
HIV-Proteasehemmer (z. B. Ritonavir)
Es wurden keine vollwertigen Studien durchgeführt, um die potenzielle Wechselwirkung zwischen Nimodipin und Anti-HIV-Protease-Inhibitoren zu untersuchen. Von einigen Arzneimitteln dieser Klasse wurde berichtet, dass sie starke Inhibitoren des Cytochrom-P450-3A4-Systems sind. Aus diesem Grund kann die Möglichkeit eines deutlichen und klinisch relevanten Anstiegs der Plasmakonzentration von Nimodipin bei gleichzeitiger Anwendung mit einem dieser Arzneimittel nicht ausgeschlossen werden (siehe Abschnitt 4.4).
Azol-Antimykotika (z. B. Ketoconazol)
Es wurden keine vollwertigen Studien durchgeführt, um die potenzielle Wechselwirkung zwischen Nimodipin und Ketoconazol zu untersuchen. Es ist bekannt, dass Azol-Antimykotika das Cytochrom-P450-3A4-System hemmen, und für andere Dihydropyridin-Calciumkanalblocker wurden verschiedene Wechselwirkungen berichtet. Daher kann bei gleichzeitiger Anwendung mit oralem Nimodipin ein wesentlicher Anstieg der systemischen Bioverfügbarkeit von Nimodipin aufgrund einer Abnahme des First-Pass-Metabolismus nicht ausgeschlossen werden (siehe Abschnitt 4.4).
Nefazodon
Es wurden keine vollwertigen Studien durchgeführt, um die potenzielle Wechselwirkung zwischen Nimodipin und Nefazodon zu untersuchen. Dieses Antidepressivum ist als potenter Inhibitor des Cytochrom-P450-3A4-Systems bekannt. Daher kann bei gleichzeitiger Anwendung von Nefazodon mit Nimodipin ein erheblicher Anstieg der Plasmakonzentration von Nimodipin nicht ausgeschlossen werden (siehe Abschnitt 4.4).
Fluoxetin
Die gleichzeitige Anwendung von Nimodipin mit dem Antidepressivum Fluoxetin im Steady State führte zu einem Anstieg der Plasmaspiegel von Nimodipin um etwa 50 % Die Konzentration von Fluoxetin war deutlich verringert, während die Konzentration seines aktiven Metaboliten Norfluoxetin nicht beeinflusst wurde (siehe Abschnitt 4.4). .
Quinupristin / Dalfopristin
Basierend auf den Erfahrungen mit dem Calciumkanalblocker Nifedipin kann die gleichzeitige Anwendung von Nimodipin und Quinupristin/Dalfopristin zu erhöhten Plasmakonzentrationen von Nimodipin führen (siehe Abschnitt 4.4).
Cimetidin
Die gleichzeitige Anwendung von Nimodipin und Cimetidin (einem H2-Antagonisten) kann zu einem Anstieg der Plasmakonzentration von Nimodipin führen (siehe Abschnitt 4.4).
Valproinsäure
Die gleichzeitige Anwendung von Nimodipin und Valproinsäure (ein Antikonvulsivum) kann zu einem Anstieg der Plasmakonzentration von Nimodipin führen (siehe Abschnitt 4.4).
Weitere Interaktionen
Nortriptyline
Die gleichzeitige Anwendung von Nimodipin und Nortriptylin im Steady State führte zu einer leichten Abnahme der Nimodipin-Konzentration, ohne die Plasmaspiegel von Nortriptylin zu beeinflussen.
Auswirkungen von Nimodipin auf andere Medikamente
Antihypertensiva
Nimodipin kann die blutdrucksenkende Wirkung gleichzeitig verabreichter blutdrucksenkender Arzneimittel verstärken, wie zum Beispiel:
- Diuretika
- Betablocker
- ACE-Hemmer - A1-Antagonisten
- andere Kalziumkanalblocker
- α-Blocker
- PDE5-Hemmer
- α-Methyldopa
Ist ein solcher Zusammenhang unvermeidbar, ist eine besonders sorgfältige Patientenüberwachung erforderlich.
Zidovudin
In einer Studie an Affen führte die gleichzeitige intravenöse Verabreichung des Anti-HIV-Medikaments Zidovudin und des Bolus Nimodipin zu einem signifikanten Anstieg der AUC von Zidovudin mit einer signifikanten Verringerung seines Verteilungsvolumens und seiner Clearance.
Wechselwirkungen mit Lebensmitteln
Grapefruitsaft
Grapefruitsaft hemmt das Cytochrom P450 3A4-System. Die gleichzeitige Einnahme von Grapefruitsaft und Diiprodipyridin-Calciumkanalblockern erhöht deren Plasmakonzentration und Wirkungsdauer aufgrund einer Verminderung ihres First-Pass-Metabolismus oder ihrer Clearance, wodurch die blutdrucksenkende Wirkung von Nimodipin verstärkt werden kann . Dieses Phänomen kann nach der letzten Einnahme von Grapefruitsaft noch mindestens 4 Tage andauern. Die Einnahme von Grapefruit oder Grapefruitsaft sollte daher während der Behandlung mit Nimodipin vermieden werden (siehe Abschnitt 4.2).
Fälle, in denen eine Interaktion nicht hervorgehoben wurde
Haloperidol
Die gleichzeitige Anwendung von Nimodipin im Steady-State an Patienten unter Langzeitbehandlung mit Haloperidol zeigte kein Potenzial für gegenseitige Wechselwirkungen.
Die gleichzeitige Anwendung von oralem Nimodipin und Diazepam, Digoxin, Glibenclamid, Indomethacin, Ranitidin und Warfarin zeigte keine potenziellen gegenseitigen Wechselwirkungen.
04.6 Schwangerschaft und Stillzeit
Schwangerschaft
Es liegen keine ausreichend kontrollierten Studien bei Schwangeren vor.
Wenn die Anwendung von Nimotop während der Schwangerschaft als notwendig erachtet wird, sollten der erwartete Nutzen und die potenziellen Risiken in Abhängigkeit vom Schweregrad des klinischen Bildes sorgfältig abgewogen werden.
Fütterungszeit
Es wurde gezeigt, dass Nimodipin und seine Metaboliten in einer Konzentration in der gleichen Größenordnung wie im mütterlichen Plasma in die Muttermilch übergehen. Müttern wird geraten, während der Einnahme des Arzneimittels nicht zu stillen.
Fruchtbarkeit
In Einzelfällen der In-vitro-Fertilisation wurden Calciumkanalblocker mit reversiblen biochemischen Veränderungen im Spermienkopf in Verbindung gebracht, die möglicherweise zu einer Beeinträchtigung der Spermienfunktion führten. Die Relevanz dieses Befundes für die Kurzzeitbehandlung ist nicht bekannt.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Grundsätzlich kann die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen in Verbindung mit dem möglichen Auftreten von Schwindel beeinträchtigt sein.
Zusätzlich für Nimotop Tropfen zum Einnehmen, Lösung:
Die Alkoholmenge in diesem Arzneimittel kann die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen beeinträchtigen (siehe Abschnitt 4.4).
04.8 Nebenwirkungen
Tabelle 1 listet die Nebenwirkungen, die mit Nimodipin in klinischen Studien mit Nimodipin berichtet wurden, unter der Indikation „Prävention und Therapie ischämischer neurologischer Defizite im Zusammenhang mit cerebralem Vasospasmus induziert durch Subarachnoidalblutung“ auf, sortiert nach Häufigkeitskategorien nach CIOMS III Studien 703 Patienten wurden mit Nimodipin und 692 mit Placebo behandelt, in den unkontrollierten Studien wurden 2.496 Patienten mit Nimodipin behandelt, Stand 31.08.2005).
Innerhalb jeder Häufigkeitsklasse werden Nebenwirkungen in absteigender Reihenfolge ihres Schweregrades berichtet.
Die Häufigkeiten sind definiert als: sehr häufig (≥ 1/10), häufig (≥ 1/100,
Tabelle 1: Unerwünschte Arzneimittelwirkungen, die bei Patienten in klinischen Studien unter der Indikation „Prävention und Behandlung ischämischer neurologischer Defizite im Zusammenhang mit zerebralem Vasospasmus“ berichtet wurden.
Tabelle 2 listet die Nebenwirkungen auf, die mit Nimodipin in klinischen Studien mit Nimodipin zum „Indikationsgebiet“ berichtet wurden.Behandlung von ischämischen neurologischen Defiziten (beeinträchtigte Hirnfunktion bei „älteren Menschen, IBFO)“ und berichtet aus Erfahrungen nach Markteinführung, sortiert nach Häufigkeitskategorien gemäß CIOMS III (in den placebokontrollierten Studien wurden 1.594 Patienten mit Nimodipin und 1.558 mit Placebo behandelt; in unkontrollierten Studien wurden 8.049 Patienten mit Nimodipin behandelt (Stand 20.10.2005).
Innerhalb jeder Häufigkeitsklasse werden Nebenwirkungen in absteigender Reihenfolge ihres Schweregrades berichtet.
Frequenzen sind wie folgt definiert: häufig (≥ 1/100,
Tabelle 2: Nebenwirkungen, die bei Patienten in klinischen Studien berichtet wurden, Indikation "Behandlung ischämischer neurologischer Defizite (beeinträchtigte Gehirnfunktion bei älteren Menschen, IBFO)".
Meldung von vermuteten Nebenwirkungen
Die Meldung vermuteter Nebenwirkungen, die nach der Zulassung des Arzneimittels aufgetreten sind, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht. Angehörige von Gesundheitsberufen werden gebeten, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem zu melden. "Adresse https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Überdosierung
Vergiftungssymptome:
Akute Überdosierungssymptome, die berücksichtigt werden müssen, sind: ausgeprägte Hypotonie, Tachykardie oder Bradykardie; Magen-Darm-Störungen und Übelkeit.
Behandlung von Vergiftungen
Im Falle einer akuten Überdosierung sollte die Gabe von Nimodipin sofort abgebrochen werden. Sofortmaßnahmen müssen darauf abzielen, die Symptome zu beseitigen.
Als Notfallmaßnahme kann eine Magenspülung unter Zusatz von Aktivkohle in Betracht gezogen werden. Bei schwerer Hypotonie können Dopamin oder Noradrenalin intravenös verabreicht werden. Da kein spezifisches Antidot bekannt ist, sollte die Behandlung von Nebenwirkungen darauf abzielen, die Hauptsymptome zu beseitigen.
Meldung von vermuteten Nebenwirkungen
Die Meldung vermuteter Nebenwirkungen, die nach der Zulassung des Arzneimittels aufgetreten sind, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht. Angehörige von Gesundheitsberufen werden gebeten, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem zu melden
www.aifa.gov.it/responsabili
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN
05.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Selektiver Calciumkanalblocker, Dihydropyridin-Derivat.
ATC-Code: C08CA06.
Nimodipin ist ein Calciumantagonist aus der Klasse der 1,4-Dihydropyridine, der sich von anderen Calciumantagonisten durch seine ausgeprägte Wirkungsselektivität im Gehirnbereich unterscheidet.
Dank seiner hohen Lipophilie durchdringt Nimodipin leicht die Blut-Hirn-Schranke. In Tierstudien wurde gezeigt, dass Nimodipin mit hoher Affinität und Selektivität an L-Typ Ca ++ -Kanäle bindet und dadurch den intrazellulären Calciumeinstrom durch die Membran blockiert.
Nimodipin schützt Neuronen und stabilisiert ihre Funktionalität, fördert den zerebralen Blutfluss und erhöht die Widerstandsfähigkeit gegen Ischämie durch eine Wirkung auf neuronale und zerebrovaskuläre Rezeptoren, die mit Kalziumkanälen verbunden sind.
Bei pathologischen Zuständen, die mit einer Zunahme des intrazytoplasmatischen Einstroms von Calcium in Nervenzellen verbunden sind, beispielsweise während einer zerebralen Ischämie, wird angenommen, dass Nimodipin die Stabilität und Funktionsfähigkeit dieser zellulären Elemente verbessert.
Die selektive Blockade von Kalziumkanälen in einigen Hirnarealen, wie dem Hippocampus und dem Kortex, könnte vielleicht die positive Wirkung von Nimodipin auf Lern- und Gedächtnisdefizite erklären, die in mehreren Tiermodellen beobachtet wurden.
Der gleiche molekulare Mechanismus liegt wahrscheinlich der gefäßerweiternden Wirkung im Gehirn und der Durchblutungsförderung von Nimodipin zugrunde, die bei Tieren und Menschen beobachtet werden.
Seine therapeutischen Eigenschaften hängen mit der Fähigkeit zusammen, die durch Calciumionen induzierte Kontraktion der glatten Muskelzelle zu hemmen.
Durch die Anwendung von Nimodipin können in vitro durch verschiedene vasoaktive Substanzen (wie Serotonin, Prostaglandine, Histamin) induzierte Vasokonstriktionen und durch das Blut oder dessen Abbauprodukte verursachte Vasokonstriktionen verhindert bzw. behoben werden.Nimodipin übt auch neuro- und psychopharmakologische Wirkungen aus.Forschung durchgeführt bei Patienten mit akuten zerebrovaskulären Erkrankungen, haben gezeigt, dass Nimodipin die Hirngefäße erweitert und die Hirndurchblutung steigert, die in den verletzten und unterperfundierten Hirnarealen meist konsequenter gesteigert wird als in den gesunden Arealen führt nicht zu stehlenden Phänomenen.Mit der Anwendung von Nimodipin wird eine signifikante Reduzierung der ischämischen neurologischen Defizite und der Mortalität aufgrund von Vasospasmen aufgrund einer subarachnoidalen Blutung aneurysmatischen Ursprungs erreicht.
Die Verbesserung ist nur bei Patienten mit Subarachnoidalblutung, zerebralem Vasospasmus, signifikant. Im Liquor von Patienten, die wegen einer Subarachnoidalblutung behandelt wurden, wurden Konzentrationen von Nimodipin bis zu 12,5 ng/ml nachgewiesen.
Es wurde klinisch gezeigt, dass Nimodipin Gedächtnis- und Konzentrationsstörungen bei Patienten mit eingeschränkter Gehirnfunktion verbessert.
Auch andere typische Symptome werden günstig beeinflusst, wie die Bewertung des klinischen Gesamteindrucks, die Bewertung einzelner Störungen, Verhaltensbeobachtungen und psychometrische Tests zeigen.
05.2 „Pharmakokinetische Eigenschaften
Absorption
Der oral verabreichte Wirkstoff Nimodipin wird praktisch vollständig resorbiert.
Der unveränderte Wirkstoff und seine First-Pass-Metaboliten werden bereits 10-15 Minuten nach Einnahme der Tablette im Plasma nachgewiesen.
Nach mehreren oralen Dosen (3 x 30 mg / Tag) betragen die maximalen Plasmakonzentrationen (Cmax) bei älteren Menschen 7,3–43,2 ng/ml und werden nach 0,6–1,6 h (tmax) erreicht.
Einzeldosen von 30 mg und 60 mg bei jungen Probanden erreichen mittlere Plasmaspitzenkonzentrationen von 16 8 ng/ml bzw. 31 12 ng/ml.
Die maximale Plasmakonzentration und die Fläche unter der Konzentrations-Zeit-Kurve erhöhen sich proportional zur Dosis bis zur untersuchten Höchstdosis (90 mg).
Mittlere Steady-State-Plasmakonzentrationen von 17,6 - 26,6 ng/ml werden nach i.v. kontinuierlich von 0,03 ng / kg / h. Nach i.v.-Bolus die Plasmakonzentrationen von Nimodipin nehmen biphasisch ab, mit Halbwertszeiten von 5-10 Minuten und ungefähr 60 Minuten. Das berechnete Verteilungsvolumen (Vss im Zwei-Kompartiment-Modell) für i.v. Ergebnisse von 0,9 - 1,6 l / kg Körpergewicht. Die systemische Gesamtclearance beträgt 0,6 - 1,9 l / h / kg.
Proteinbindung und -verteilung
Nimodipin ist zu 97-99% an Plasmaproteine gebunden.
Bei dem mit 14C-markiertem Nimodipin behandelten Versuchstier passiert die Radioaktivität die Plazentaschranke.
Auch bei Frauen ist eine ähnliche Verteilung wahrscheinlich, allerdings fehlen diesbezüglich experimentelle Belege.
Bei Ratten treten Nimodipin und/oder seine Metaboliten in der Milch in einer viel höheren Konzentration auf als im mütterlichen Plasma. Bei Frauen erscheint das unveränderte Arzneimittel in der Milch in Konzentrationen in der gleichen Größenordnung wie im mütterlichen Plasma.
Nach oraler und intravenöser Verabreichung kann Nimodipin in Konzentrationen, die etwa 0,5 % der im Plasma gefundenen Konzentrationen entsprechen, in die Zerebrospinalflüssigkeit dosiert werden.
Diese entsprechen etwa den Konzentrationen an freiem Wirkstoff im Plasma.
Stoffwechsel, Ausscheidung und Ausscheidung
Die Verstoffwechselung von Nimodipin erfolgt über das Cytochrom P450 3A4-System, hauptsächlich durch Dehydrierung des Dihydropyridinrings und oxidative Entesterung des Esters, die mit der Hydroxylierung der Ethylgruppen 2 und 6 und der Glucuronidierung einen der weiteren wichtigen Stoffwechselschritte darstellt.
Die drei im Plasma auftretenden Primärmetaboliten besitzen eine therapeutisch unbedeutende oder keine "Restaktivität".
Die Auswirkungen der Induktion und Hemmung auf Leberenzyme sind nicht bekannt. Beim Menschen werden ca. 50 % der Metaboliten über die Nieren und 30 % über die Galle ausgeschieden.
Die Eliminationskinetik ist linear. Die Halbwertszeit von Nimodipin liegt zwischen 1,1 und 1,7 Std. Die terminale Halbwertszeit von 5-10 Std. ist für die Bestimmung des Dosisintervalls nicht relevant.
Mittlere Plasmakonzentrationskurven von Nimodipin nach oraler Gabe von 30 mg in der Tablettenformulierung und nach i.v. von 0,015 mg / kg für 1 h (n = 24 ältere Freiwillige).
Bioverfügbarkeit
Nach dem relevanten First-Pass-Metabolismus (ca. 85-95 %) beträgt die absolute Bioverfügbarkeit 5-15 %.
05.3 Präklinische Sicherheitsdaten
Präklinische Daten lassen auf der Grundlage konventioneller Studien zu keine besonderen Gefahren für den Menschen erkennen Sicherheitspharmakologie, Toxizität bei wiederholter Gabe, Genotoxizität, kanzerogenes Potenzial, Reproduktionstoxizität. Bei Ratten hemmten Dosen von 30 mg / kg / Tag oder höher, die während der Schwangerschaft verabreicht wurden, das fetale Wachstum, was zu einer Abnahme des fetalen Gewichts führte. Eine Dosis von 100 mg / kg / Tag war für den Fötus tödlich. Es gab keine Hinweise auf Teratogenität. Bei Kaninchen wurden bis zu einer Dosis von 10 mg/kg/Tag keine Embryotoxizität und Teratogenität beobachtet. In einer peri-postnatalen Studie an Ratten wurden Mortalität und Verzögerung der körperlichen Entwicklung bei Dosen von 10 mg/kg/Tag oder mehr beobachtet. Diese Ergebnisse wurden durch nachfolgende Studien nicht bestätigt.
Akute Toxizität
Tisch 3
Der Unterschied zwischen den LD50-Werten nach oraler und intravenöser Gabe zeigt an, wie nach der Gabe hoher Dosen einer oralen Suspensionsformulierung die Resorption des Wirkstoffs unvollständig oder verzögert ist.
Vergiftungssymptome nach oraler Verabreichung wurden nur bei Mäusen und Ratten beobachtet und äußern sich in leichter Zyanose, stark verminderter Motilität und Dyspnoe.
Nach intravenöser Verabreichung wurden diese mit tonisch-klonischen Anfällen verbundenen Vergiftungserscheinungen bei allen untersuchten Tierarten beobachtet.
Subchronische Verträglichkeitsstudien
Studien an Hunden mit einer oralen Dosis von 10 mg / kg führten zu einem verringerten Körpergewicht, verringertem Hämatokrit, Hämoglobin und Erythrozyten; erhöhte Herzfrequenz und Veränderungen des Blutdrucks.
Studien zur chronischen Verträglichkeit
Orale Dosierungen bis ca. 90 mg/kg/Tag über zwei Jahre wurden von der Maus gut vertragen.
In einer 1-Jahres-Studie an Hunden wurde die systemische Verträglichkeit von Nimodipin-Dosen bis zu 6,25 mg/kg/Tag untersucht.
Dosierungen bis 2,5 mg/kg erwiesen sich als unbedenklich, während 6,25 mg/kg elektrokardiographische Veränderungen durch Störungen des myokardialen Blutflusses verursachten. Bei dieser Dosierung wurden jedoch keine histopathologischen Veränderungen des Herzens gefunden.
Studien zur Reproduktionstoxizität
Fruchtbarkeitsstudien an der Ratte
Dosierungen bis zu 30 mg / kg / Tag hatten keinen Einfluss auf die Fertilität männlicher und weiblicher Ratten oder der nachfolgenden Generationen.
Embryotoxizitätsstudien
Die Verabreichung von 10 mg / kg / Tag an die weibliche Ratte während der Embryogenese zeigte keine schädlichen Wirkungen, während Dosierungen von 30 mg / kg / Tag und mehr das Wachstum hemmten, was zu einem reduzierten fetalen Gewicht führte, und bei 100 mg / kg / Tag induzierten eine Zunahme der intrauterinen embryonalen Todesfälle.
Embryotoxizitätsstudien an Kaninchen mit oralen Dosen von bis zu 10 mg / kg / Tag zeigten keine teratogenen oder embryotoxischen Wirkungen.
Perinatale und postnatale Entwicklung bei Ratten
Um die perinatale und postnatale Entwicklung zu bewerten, wurden Studien an Ratten mit Dosen bis zu 30 mg / kg / Tag durchgeführt.
In einer Studie mit 10 mg/kg/Tag und mehr wurde ein Anstieg sowohl der perinatalen als auch der postnatalen Mortalität sowie eine verzögerte körperliche Entwicklung beobachtet. Diese Ergebnisse wurden durch nachfolgende Studien nicht bestätigt.
Spezifische Verträglichkeitsstudien
Karzinogenese
In einer Lebenszeitstudie an Ratten, die 2 Jahre lang mit Dosierungen von bis zu 1800 ppm (ca. 90 mg/kg/Tag) im Futter behandelt wurden, wurde kein onkogenes Potenzial gezeigt.
Ähnliche Ergebnisse wurden bei 21 Monaten in einer Langzeitstudie mit 500 mg/kg/Tag oral behandelten Mäusen erhalten.
Mutagenese
Nimodipin wurde in zahlreichen Mutagenitätsstudien validiert, die keine signifikanten mutagenen Wirkungen, Geninduktion und Chromosomenmutationen zeigten.
06.0 PHARMAZEUTISCHE INFORMATIONEN
06.1 Hilfsstoffe
Dragees
mikrogranuläre Cellulose, Povidon, Crospovidon, Magnesiumstearat, Maisstärke, Hypromellose, Macrogol 4000, Titandioxid (E171), gelbes Eisenoxid (E172)
Tropfen zum Einnehmen, Lösung
hydriertes mehrwertiges Rizinusöl, Ethylalkohol
06.2 Inkompatibilität
Keine bekannt.
06.3 Gültigkeitsdauer
Überzogene Tabletten: 5 Jahre.
Tropfen zum Einnehmen, Lösung: 5 Jahre.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Überzogene Tabletten: Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich
Tropfen zum Einnehmen, Lösung: vor Licht schützen / nicht kühlen
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks
Tablets:
36 Tabletten
PVC / Aluminium oder PVC-PVDC / Aluminium oder PP Blister
Tropfen zum Einnehmen, Lösung:
Tropfen zum Einnehmen, Lösung: 25 ml Flasche Braunglasflasche mit Schraubverschluss und Glastropfer
06.6 Gebrauchs- und Handhabungshinweise
Keine besonderen Anweisungen
07.0 INHABER DER MARKETING-ERLAUBNIS
Bayer S.p.A. - Viale Certosa, 130 - Mailand
08.0 NUMMER DER MARKETING-ERLAUBNIS
NIMOTOP 30 mg überzogene Tabletten
AIC 026403016
NIMOTOP 30 mg / 0,75 ml Tropfen zum Einnehmen, Lösung
AIC 026403055
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG
Erstzulassung: 27.07.87 (im Handel seit Oktober 1987)
Genehmigungserneuerung: Juni 2010