Wirkstoffe: Fluocortolonpivalat, Fluocortoloncaproat, Cincocainhydrochlorid
Ultraproct Rektumsalbe
Ultraproct Packungsbeilagen sind für Packungsgrößen erhältlich:- Ultraproct Rektalsalbe
- Ultraproct-Zäpfchen
Indikationen Warum wird Ultraproct verwendet? Wofür ist das?
Ultraproct enthält zwei Wirkstoffe: Fluocortolon (als Pivalat und als Caproat) und Cincocainhydrochlorid.
Fluocortolon (Pivalat und Caproat) gehört zur Kategorie der Arzneimittel, die als Kortikosteroide, entzündungshemmende Arzneimittel, bezeichnet werden.
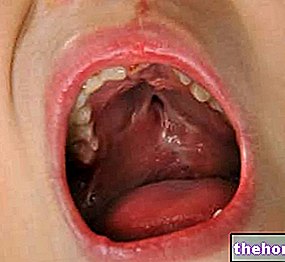
Cincocainhydrochlorid gehört zu der Kategorie von Arzneimitteln, die als Lokalanästhetika bezeichnet werden. Ultraproct ist indiziert zur Behandlung von inneren und äußeren Hämorrhoiden (geschwollene und entzündete Venen im Analkanal und um den After), Analfissuren (kleine Wunden am Rand des Afters) und Proktitis (Entzündung des Rektums).
Sprechen Sie mit Ihrem Arzt, wenn Sie sich nicht besser oder schlechter fühlen.
Kontraindikationen Wenn Ultraproct nicht verwendet werden sollte
Verwenden Sie kein Ultraproct
- wenn Sie allergisch gegen Fluocortolonpivalat, Fluocortoloncaproat oder Cincocainhydrochlorid oder einen der in Abschnitt 6 genannten sonstigen Bestandteile dieses Arzneimittels sind;
- wenn tuberkulöse, luetische (durch Syphilis) oder virale Läsionen (Pocken, Windpocken, Impfpusteln) im zu behandelnden Gebiet vorhanden sind.
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Ultraproct® beachten?
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Ultraproct anwenden.
Den Kontakt mit den Augen vermeiden.
Waschen Sie sich nach der Anwendung des Arzneimittels gründlich die Hände.
Wenn im zu behandelnden Bereich eine Mykose (Pilzinfektion) vorliegt, wird Ihr Arzt ein lokales Antimykotikum in Kombination verschreiben.
Die Anwendung, insbesondere bei längerer Anwendung der Produkte zur lokalen Anwendung, kann zu Sensibilisierungserscheinungen (Allergie) führen.Beenden Sie in diesem Fall die Behandlung und wenden Sie sich an Ihren Arzt, um eine geeignete Therapie festzulegen.
Bei lokaler Anwendung auf großen Flächen, auf geschädigter Haut oder in Gegenwart eines Okklusivverbandes können Kortikosteroide in solchen Mengen resorbiert werden, dass aus der Ferne unerwünschte Wirkungen auftreten.
Die Behandlungsdauer sollte nach Möglichkeit 4 Wochen nicht überschreiten.
Für diejenigen, die sportliche Aktivitäten ausüben: Die Einnahme des Medikaments ohne therapeutische Notwendigkeit stellt Doping dar und kann in jedem Fall positive Anti-Doping-Tests feststellen.
Kinder
In der sehr frühen Kindheit sollte das Medikament in dringenden Fällen unter direkter Aufsicht des Arztes verabreicht werden.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Ultraproct® verändern
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen, kürzlich andere Arzneimittel eingenommen haben oder beabsichtigen andere Arzneimittel einzunehmen.
Warnungen Es ist wichtig zu wissen, dass:
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Wenden Sie Ultraproct nicht während des ersten Schwangerschaftstrimesters an, es sei denn, der Nutzen rechtfertigt die potenziellen Risiken für das Baby.
Wenn Sie schwanger sind, verwenden Sie das Arzneimittel, wenn dies unbedingt erforderlich ist und unter direkter Aufsicht Ihres Arztes.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Ultraproct hat keinen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Ultraproct enthält Rizinusöl
Dieses Arzneimittel enthält Rizinusöl, das Hautreaktionen verursachen kann.
Dosis, Methode und Zeitpunkt der Anwendung Wie ist Ultraproct anzuwenden: Dosierung
Wenden Sie dieses Arzneimittel immer genau wie in dieser Packungsbeilage beschrieben bzw. genau nach Anweisung Ihres Arztes oder Apothekers an. Fragen Sie im Zweifelsfall Ihren Arzt oder Apotheker.
Tragen Sie eine dünne Schicht Rektumsalbe auf.
Während des ersten Tages werden auch 3-4 Anwendungen des Präparats empfohlen, um ein schnelleres Verschwinden der Symptome zu erreichen; danach genügen 2 Anwendungen pro Tag.
Um Rückfälle zu vermeiden, sollte die Behandlung nach dem vollständigen Verschwinden der Beschwerden noch einige Tage mit einer Anwendung pro Tag fortgesetzt werden.
Die intrarektale Einführung der Salbe kann mit der der Packung beiliegenden Spezialkanüle erfolgen, wobei darauf zu achten ist, dass die Anwendung nach der Stuhlentleerung erfolgt.
Überdosierung Was ist zu tun, wenn Sie eine Überdosis Ultraproct® eingenommen haben?
Bei versehentlicher oraler Aufnahme können Symptome wie Krämpfe, Hemmung oder Stillstand der Atemfunktion und Herz-Kreislauf-Störungen (Depression oder Stillstand der Herzfunktion) auftreten.
Wenn Sie versehentlich eine Überdosis Ultraproct eingenommen haben, benachrichtigen Sie sofort Ihren Arzt oder begeben Sie sich in das nächste Krankenhaus.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
Nebenwirkungen Was sind die Nebenwirkungen von Ultraproct
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Seltene Fälle von lokaler Reizung mit Brennen und Fällen von Allergien wurden bei Personen mit einer Prädisposition gegenüber einem oder mehreren Bestandteilen des Arzneimittels, insbesondere Cincocainhydrochlorid, berichtet.
In seltenen Fällen können allergische Hautreaktionen auftreten.
Bei längerer Behandlung (mehr als 4 Wochen) können lokale Symptome wie Hautatrophie (Hautverdünnung) auftreten.
Die geringen Dosen der im Arzneimittel enthaltenen Wirkstoffe machen das Auftreten von sekundären Phänomenen aus der Ferne unwahrscheinlich, von der Aufnahme in den Körper. Sollten diese auftreten, hätten sie den allgemeinen Charakter der klassischen Sekundärwirkungen von Kortikosteroiden, wenn auch von sehr geringer Größe.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker, einschließlich aller möglichen Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind. Sie können Nebenwirkungen auch direkt über das nationale Meldesystem unter www.agenziafarmaco.it/it/responsabili melden.Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
Ablauf und Aufbewahrung
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Verwenden Sie dieses Arzneimittel nicht nach dem auf der Packung angegebenen Verfallsdatum.
Das Verfallsdatum bezieht sich auf den letzten Tag des Monats Das angegebene Verfallsdatum bezieht sich auf das Produkt in intakter Verpackung, korrekt gelagert.
Gültigkeit nach dem ersten Öffnen: 3 Monate.
Unter 25 °C lagern.
Werfen Sie Arzneimittel nicht in das Abwasser oder den Hausmüll. Fragen Sie Ihren Apotheker, wie Sie Arzneimittel, die Sie nicht mehr verwenden, entsorgen sollen. Dies trägt zum Schutz der Umwelt bei.
Andere Informationen
Was Ultraproct
- Die Wirkstoffe sind: Fluocortolonpivalat, Fluocortoloncaproat, Cincocainhydrochlorid. 1 g Rektalsalbe enthält: 0,918 mg Fluocortolonpivalat, 0,945 mg Fluocortoloncaproat, 5 mg Cincocainhydrochlorid.
- Die sonstigen Bestandteile sind: Polyethylenglycol-400-monoricinoleat, hydriertes Rizinusöl, 2-Octyldodecanol, Rizinusöl, Citrus Rose Duftöl.
Beschreibung wie Ultraproct aussieht und Inhalt der Packung
Rektumsalbe, 30 g Tube + 1 Kanüle.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu haben, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS
ULTRAPROCT
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Jedes Zäpfchen enthält 0,612 mg Fluocortolonpivalat, 0,630 mg Fluocortoloncaproat und 1 mg Cincocainhydrochlorid.
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
Jedes Gramm Rektalsalbe enthält 0,918 mg Fluocortolonpivalat, 0,945 mg Fluocortoloncaproat, 5 mg Cinchocainhydrochlorid.
Sonstige Bestandteile mit bekannter Wirkung: Hydriertes Rizinusöl.
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
03.0 DARREICHUNGSFORM
Zäpfchen, rektale Salbe.
04.0 KLINISCHE INFORMATIONEN
04.1 Anwendungsgebiete
Die im Ultraproct enthaltene Assoziation ermöglicht die polysymptomatische Behandlung des anorektalen Varikose-Syndroms.
Die Verfügbarkeit von Zäpfchen und Rektalsalbe ermöglicht es, gleichzeitig die inneren und äußeren Venenbereiche zu erreichen, die am Krampfaderphänomen beteiligt sein können.
Innere und äußere Hämorrhoiden, Analfissuren, Proktitis.
04.2 Dosierung und Art der Anwendung
•Zäpfchen
Ein Zäpfchen pro Tag ist in der Regel ausreichend.
Nach dem vollständigen Verschwinden der Störungen wird empfohlen, die Behandlung für eine weitere Woche mit der Anwendung von 1 Zäpfchen alle 2 Tage fortzusetzen.
Es ist ratsam, das Zäpfchen nach dem Stuhlgang einzuführen.
• Rektumsalbe
Eine dünne Schicht Rektalsalbe wird normalerweise zweimal täglich aufgetragen. Am ersten Tag werden auch 3-4 Anwendungen des Präparats empfohlen, um ein schnelleres Verschwinden der Symptome zu erreichen.
Um Rückfälle zu vermeiden, sollte die Behandlung nach dem vollständigen Verschwinden der Beschwerden noch einige Tage mit einer Anwendung pro Tag fortgesetzt werden.
Die intrarektale Einführung der Rektalsalbe kann mit der der Packung beiliegenden Spezialkanüle erfolgen, wobei darauf zu achten ist, dass diese nach der Stuhlentleerung appliziert wird.
Die Behandlungsdauer sollte nach Möglichkeit vier Wochen nicht überschreiten.
Pädiatrische Patienten: In der sehr frühen Kindheit sollte das Tierarzneimittel in dringenden Fällen unter direkter Aufsicht des Arztes verabreicht werden.
04.3 Kontraindikationen
Überempfindlichkeit gegen die Wirkstoffe, insbesondere Cincocain, oder einen der sonstigen Bestandteile.
Tuberkulöse und luetische Prozesse in der zu behandelnden Region, Pocken, Windpocken, Impfpusteln.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung
Bei Mykosen im zu behandelnden Areal sind topische Antimykotika indiziert.
Die Anwendung von Produkten zur topischen Anwendung, insbesondere bei längerer Dauer, kann zu Sensibilisierungsphänomenen führen.
In diesem Fall ist es notwendig, die Behandlung zu unterbrechen und eine geeignete Therapie einzuleiten.
Bei topischer Anwendung auf großen Flächen, auf geschädigter Haut oder in Gegenwart eines Okklusivverbandes können Kortikosteroide in solchen Mengen resorbiert werden, dass systemische Nebenwirkungen auftreten.
Den Kontakt mit den Augen vermeiden. Es wird empfohlen, nach Gebrauch gründlich die Hände zu waschen.
Wenn die Zäpfchen durch die Hitze weich geworden sind, müssen sie vor dem Öffnen der Verpackung in kaltes Wasser getaucht werden, bis sie wieder eine ausreichende Konsistenz haben.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Es wird angenommen, dass die gleichzeitige Behandlung mit CYP3A-Inhibitoren, einschließlich Arzneimitteln, die Cobicistat enthalten, das Risiko systemischer Nebenwirkungen erhöht. Die Kombination sollte vermieden werden, es sei denn, der Nutzen überwiegt das erhöhte Risiko systemischer Nebenwirkungen durch Kortikosteroide. In diesem Fall sollten die Patienten auf das Fehlen systemischer Nebenwirkungen durch Kortikosteroide überwacht werden.
04.6 Schwangerschaft und Stillzeit
Schwangerschaft
Tierexperimentelle Studien mit Kortikosteroiden haben eine Reproduktionstoxizität gezeigt. Einige epidemiologische Studien deuten darauf hin, dass bei Säuglingen von Frauen, die im ersten Schwangerschaftstrimester mit systemischen Kortikosteroiden behandelt werden, ein erhöhtes Risiko für eine Gaumenspalte besteht.
Ultraproct sollte während des ersten Schwangerschaftstrimesters nicht angewendet werden, es sei denn, der Nutzen rechtfertigt das potenzielle Risiko für den Fötus.
Fütterungszeit
Es liegen keine Daten zum Übergang von Stoffen in die Muttermilch vor, fragen Sie daher vor der Anwendung Ihren Arzt.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Ultraproct hat keinen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
04.8 Nebenwirkungen
Seltene Fälle von lokaler Reizung mit Brennen.
Fälle von Sensibilisierung bei prädisponierten Personen gegenüber einem oder mehreren Bestandteilen des Tierarzneimittels, insbesondere Cincocain.
Die im Produkt enthaltenen niedrigen Wirkstoffdosen machen ein leichtes Auftreten sekundärer systemischer Phänomene durch Resorption nicht plausibel.
Treten diese auf, könnten sie auf die klassischen Nebenwirkungen von Kortikosteroiden zurückgeführt werden, wenn auch von sehr geringer Größe.
Bei längerer Behandlung (mehr als 4 Wochen) können lokale Symptome wie Hautatrophie auftreten.
In seltenen Fällen können allergische Hautreaktionen auftreten.
Meldung von vermuteten Nebenwirkungen
Die Meldung von vermuteten Nebenwirkungen, die nach der Zulassung des Arzneimittels aufgetreten sind, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem www .agenziafarmaco.gov . zu melden .it / es / verantwortlich.
04.9 Überdosierung
Es sind keine Fälle einer Ultraproct-Überdosierung bekannt.
In Übereinstimmung mit den Ergebnissen von Studien zur akuten Toxizität, die mit Fluocortolon-Estern durchgeführt wurden, ist nach einmaliger rektaler oder perianaler Anwendung von Ultraproct kein Vergiftungsrisiko zu erwarten, auch nicht nach einer unfreiwilligen Überdosierung.
Bei versehentlicher oraler Aufnahme können die dosisabhängigen systemischen Wirkungen durch den anästhetisch wirkenden Wirkstoff Cincocain verursacht werden und sich mit Symptomen, die das ZNS betreffen (Krämpfe, Hemmung oder Stillstand der Atemfunktion) und Herz-Kreislauf-Erkrankungen ( Depression oder Stillstand der Herzfunktion).
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN
05.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Substanzen zur Behandlung von Hämorrhoiden und Analfissuren zur topischen Anwendung.
ATC-Code: C05AA08.
Im „Ultraproct“ befinden sich zwei Wirkstoffe, deren Assoziation die einzelnen pharmakologischen Eigenschaften nicht verändert, sondern deren Einsatz in Wirksynergie ermöglicht.
Das entzündungshemmende Fluocortolon sowohl als Pivalat als auch als Caproat kombiniert die mit verschiedenen Tests nachgewiesene Wirksamkeit mit einer großen Sicherheitsspanne gegen systemische und lokale Nebenwirkungen. Cincocainhydrochlorid ist als hochwirksames Lokalanästhetikum bekannt, das die Anwendung sehr niedriger Dosen ermöglicht.
Die Anwesenheit dieser Wirkstoffe verleiht dem Ultraproct eine entzündungshemmende, juckreizstillende und lokalanästhetische Wirkung.
05.2 Pharmakokinetische Eigenschaften
Untersuchungen mit radioaktiven Isotopen bei Tieren und Menschen haben gezeigt, dass nach 24-stündiger Hautapplikation unter Okklusivverband nur 1/5 der applizierten Dosen in den 3 Tagen untersuchten Fäzes und Urin wiedergefunden werden. Die Resorption von Fluocortoloncaproat ist wesentlich langsamer als die von Pivalat, wodurch eine zweiphasige Wirkung des Präparats gewährleistet ist (schnelle Anfangswirkung und verlängerte Wirkung im Laufe der Zeit).
Insbesondere der Metabolismus und die Pharmakokinetik von Fluocortolon wurden nach oraler Gabe untersucht.
Die Halbwertszeit betrug etwa 50 Minuten.
Das Nierenemunktorium ist der wichtigste Eliminationsweg.
05.3 Präklinische Sicherheitsdaten
Studien zur Embryotoxizität und Teratogenität haben zu für Kortikosteroide typischen Ergebnissen geführt, wie zum Beispiel embryoletale Wirkung und teratogene Wirkung in entsprechenden Tests.
06.0 PHARMAZEUTISCHE INFORMATIONEN
06.1 Hilfsstoffe
Rektumsalbe: Polyethylenglycol-400-monoricinoleat; hydriertes Rizinusöl; 2-Octyldodecanol; Rizinusöl; Duftöl der Zitrusrose.
Zäpfchen: Glyceride gesättigter Fettsäuren.
06.2 Inkompatibilität
Unverträglichkeiten mit anderen Arzneimitteln sind weder bekannt noch absehbar.
06.3 Gültigkeitsdauer
Rektumsalbe: 2 Jahre.
Zäpfchen: 3 Jahre.
Salbe: nach dem ersten Öffnen 3 Monate
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Rektumsalbe: unter 25 ° C lagern.
Zäpfchen: im Kühlschrank lagern (2 ° C - 8 ° C).
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks
Rektumsalbe
Reinaluminium-Tube mit Epoxidlack beschichtet mit Polyethylen-Kappe Die Packung enthält auch eine Polypropylen-Kanüle.
30g Tube.
Zäpfchen
Schachtel mit 2 Streifen x 6 Zäpfchen, verpackt in transparenten PVC-Hüllen.
Schachtel mit 12 Zäpfchen.
06.6 Gebrauchs- und Handhabungshinweise
Keine besonderen Anweisungen
07.0 INHABER DER MARKETING-ERLAUBNIS
Bayer S.p.A. - Viale Certosa, 130 - 20156 Mailand
08.0 NUMMER DER MARKETING-ERLAUBNIS
Rektumsalbe 30 g Tube A.I.C. n. 021122080
Zäpfchen 12 Zäpfchen A.I.C. n. 021122066
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG
Rektalsalbe 30 g Tube 15.10.1971 / 01.06.2010
Zäpfchen 12 Supp. 26.07.1968 / 01.06.2010
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs
04/2017